فسفر
فسفر -ولی؛ متر [از یونانی. Phōphoros یک عنصر شیمیایی نور (P) است که نقش مهمی در زندگی حیوانات و گیاهان ایفا می کند (در برخی از مواد معدنی، در استخوان های حیوانی، در حیوانات و بافت های گیاهی موجود است). قرمز f سیاه f. در ماهی بسیاری از فسفر. F. نیاز به تقویت استخوان ها. سفید f. (قابل اشتعال و درخشان در ماده تاریک). دریا افتخار می کند، فسفر می درخشد (درخشان در شب با نور سبز به دلیل فراوانی میکروارگانیسم ها).
◁ فسفر (نگاه کنید به).
فسفر(لات فسفر)، عنصر شیمیایی گروه V سیستم دوره ای. نام از یونانی phōsphóros - نور لمسی. چند اصلاحیه - فسفر سفید (تراکم 1.828 گرم در سانتی متر، t. PL 44.14 درجه سانتی گراد)، فسفر قرمز (2،31 گرم / سانتی متر تراکم 3، t. PL 593 درجه سانتیگراد)، و غیره فسفر سفید به راحتی خود پیشنهاد، درخشش در تاریکی (از این رو نام)، سمی؛ قرمز کمتر فعال شیمیایی، سمی است. معدن از آپاتیت ها و فسفات ها. مصرف کننده ارشد - کشاورزی (کود فسفریک)؛ این در تولید مطابقت، متالورژی (Deoxidizer و مولکول برخی از آلیاژها)، در سنتز آلی و غیره استفاده می شود.
فسفرفسفر (LAT. - فسفوپوس)، P (PE)، عنصر شیمیایی با عدد اتمی 15، وزن اتمی 30،973762. واقع در گروه VA در 3 سیستم دوره ای. این یک پیکربندی پایدار 31 R. پیکربندی یک لایه خارجی خارجی 3 است s. 2
r 3
. درجه اکسیداسیون در ترکیبات از -3 تا +5 وجود دارد. Valence از III به V. پایدار ترین درجه اکسیداسیون در اتصالات +5 است.
شعاع اتم خنثی P 0.134 نانومتر، شعاع یون: P 3-0.186 NM، P 3+ 0.044 نانومتر (هماهنگی شماره 6) و P 5+ - 0.017 نانومتر (تعداد هماهنگی 4) و 0.038 نانومتر (هماهنگی شماره 6). انرژی یونیزاسیون متوالی اتم خنثی برابر با 10.486، 19.76، 30.16، 51.4 و 65 EV برابر است. ارتباط الکترون 0.6 EV. برق توسط pauling (سانتی متر. paulong linaus) 2.10 غیر فلز.
افتتاح تاریخ
اولین بار در حالت آزاد فسفر دریافت شده در سال 1669 هامبورگ Alchemik H. نام تجاری (اطلاعاتی وجود دارد که ماده ای شبیه به خواص در قرن 12 توسط Behil Alchemist عربی دریافت شد). در جستجوی سنگ فلسفی (سانتی متر. الیکسیر) این در یک رطوبت بسته، باقی مانده خشک از تبخیر ادرار با شن و ماسه رودخانه و زغال چوب بود. پس از کالکسیون، کشتی با واکنشگرها شروع به درخشندگی در تاریکی با نور سفید (این توسط فسفر بازسازی شده از ترکیبات آن موجود در ادرار).
در سال 1680، فسفر درخشان در تاریکی (از یونانی "فسفر" - یک پایه نور) دریافت انگلیسی R. Boyle. (سانتی متر. بول رابرت) در سال های بعد، مشخص شد که فسفر نه تنها در ادرار، بلکه در بافت های مغز، در استخوان های اسکلت قرار دارد. ساده ترین روش به دست آوردن فسفر توسط کلسیم خاکستر استخوان با زغال سنگ در 1771 K. shelele پیشنهاد شد (سانتی متر. Scheel Karl Wilhelm). ماهیت ابتدایی فسفر در پایان قرن 18th Century A. Lavauzier نصب شد. (سانتی متر. Lavoisier Antoine Laurent)
پیدا کردن در طبیعت
محتوا در پوسته زمین 0.105٪ وزن است که به طور قابل توجهی بیش از محتوای، به عنوان مثال، نیتروژن (سانتی متر. نیتروژن). در آب دریا 0.07 میلی گرم / لیتر. در یک فرم آزاد در طبیعت، فسفر یافت نشد، اما بخشی از 200 مواد معدنی مختلف است. معروف ترین فسفر (سانتی متر. فسفر) کلسیم Ca 3 (PO 4) 3، تطابق (سانتی متر. تاسف) (فلوروپاتیت 3AS 3 (PO 4) 3 · CAF 2، یا CA 5 (PO 4) 3 F)، Monazit (سانتی متر. مونکوت),
فیروزه (سانتی متر. فیروزه). فسفر بخشی از همه موجودات زنده است.
به دست آوردن
تولید فسفر توسط بهبود الکتروترمال از فسفات ها و آپاتیت ها در 1400-1600 درجه سانتیگراد با کک در حضور سیلیکا انجام می شود:
2S 3 (PO 4) 2 + 6SIO 2 + 10C \u003d P 4 + 6CASIO 3 + 10CO
4AS 5 (PO 4) 3 F + 21SIO 2 + 30C \u003d 3P 4 + 20CASIO 3 + 30CO + SIF 4
جفت های برجسته P 4 بیشتر با بخار آب گرم شده برای به دست آوردن حرارتی درمان می شوند اسید فسفریک H 3 PO 4:
P 4 + 14N 2 O \u003d 4H 3 PO 4 + 8H 2
در طول desublimations بخارات R 4، فسفر سفید شکل گرفته است. آن را به یک فسفر قرمز با حرارت دادن بدون دسترسی به هوا در دمای 200-300 درجه سانتیگراد در راکتورها مجهز به پیچشی پیچ از جرم واکنش پردازش می شود.
ویژگی های ساختار تغییرات آلوتروپیک و خواص فیزیکی آنها
فسفر ابتدایی در چندین اصلاحات آلوتروپیک وجود دارد، اصلی ترین آنها عبارتند از: سفید (فسفر III)، قرمز (فسفر II) و سیاه (فسفر I).
فسفر سفید یک موم، ماده شفاف، با بوی مشخص است. این شامل مولکول های تتراکتیل P 4 است که می تواند آزادانه چرخش کند. فسفر سفید دارای یک نوع شبکه مولکولی کریستال مکعب، پارامتر سلول است ولی \u003d 1.851 نانومتر تراکم 1.828 کیلوگرم / دسامبر 3. نقطه ذوب 44،14 درجه سانتی گراد، نقطه جوش 287 درجه سانتی گراد. دو فرم وجود دارد فسفر سفید: A-modification، با یک شبکه کریستال مکعبی، در -76.9 درجه سانتیگراد به تغییرات B منتقل می شود، شبکه کریستال که نصب نشده است و هیچ چرخش آزاد مولکول های P 4 وجود ندارد. دی الکتریک حل شده در الکل اتیلیک، بنزول، CS 2 سروو کربن.
گرمایش فسفر سفید بدون دسترسی به هوا در 250-300 درجه سانتیگراد توسط فسفر قرمز به دست می آید. سدیم، ید و ناخالصی های سلنیوم و اشعه های UV، انتقال یک اصلاح را به دیگری افزایش می دهند.
آمورفین فسفر قرمز، رنگ از قرمز به قهوه ای تیره و بنفش دارد. چندین فرم کریستالی با خواص مختلف وجود دارد. فسفر کریستال قرمز (نیم فسفوروفوس) با خنک کننده اشباع شده در دمای 600 درجه سانتیگراد محلول فسفر قرمز در سرب مذاب به دست می آید. این یک شبکه مونوکلینیک، پارامترهای سلول های ابتدایی است ولی \u003d 1.02 نانومتر که در\u003d 0.936 نانومتر از جانب \u003d 2.51 نانومتر، زاویه B 118.8 درجه. تراکم فسفر قرمز 2.0-2.4 کیلوگرم / دسامبر 3. دی الکتریک هنگامی که گرم شد، فسفر قرمز به شکل مولکول های P 4 تبخیر می شود، تراکم آن منجر به تشکیل فسفر سفید می شود.
هنگام گرم کردن فسفر سفید به 200-220 درجه سانتیگراد تحت فشار 1.2 GPA، فسفر سیاه کریستالی شکل گرفته است. مشبک از لایه های فیبری با آرایش هرمی اتم ساخته شده است. پایدار ترین تنوع فسفر سیاه دارای یک پنجره مشبک Orthorhombic، پارامترهای ولی \u003d 0.3314 نانومتر که در\u003d 0.4376 نانومتر، C \u003d 1،0478 نانومتر. تراکم فسفر سیاه 2.702 کیلوگرم / دسامبر 3 است. خارجی شبیه به گرافیت؛ نیمه هادی، دیامغناطیس. هنگامی که به 560-580 درجه سانتیگراد گرم می شود، به یک فسفر قرمز تبدیل می شود. فسفر سیاه کم موثر است، با مشکل قابل اشتعال.
خواص شیمیایی
فسفر در اتصالات به طور عمده Covalen است. فسفر دارای Orbitals 3D آزاد است که منجر به تشکیل روابط کمک کننده کمک کننده می شود. فعال ترین فسفر سفید. این در هوا اکسید شده است. اکسیداسیون با توجه به مکانیزم واکنش های زنجیره ای رخ می دهد و با Chemolyuminescence همراه است. هنگامی که فسفر سوختن بیش از اکسیژن، P 2 O 5 به دست می آید، که دیمرهای P 4 O 10 و Tetramera P 8 O 20 را تشکیل می دهند. با کمبود اکسیژن، P 2 O 3 به دست می آید. به علت گرما آزاد شده در هنگام اکسیداسیون، خود را در هوا قرار دهید. فسفر قرمز در هوا به آرامی اکسید شده است، نه خودپرداخت. فسفر سیاه در هوا اکسیداسیون نمی کند.
اکسید فسفر (V) - اکسید اسید. آن را با آب با مقدار زیادی از گرما واکنش نشان می دهد. در همان زمان، پلیمر متافسفات اسید (HRO 3) N برای اولین بار تشکیل شده است. هنگام پردازش آب گرم، آن را به یک اسید ارتوپرفیک سه محور از نیروی متوسط \u200b\u200bH 3 PO 4 تبدیل می شود:
P 4 O 10 + 2n 2 O \u003d (HRO 3) 4؛ (NRA 3) 4 + 4n 2 O \u003d 4N 3 PO 4
یا P 2 O 5 + 3n 2 O \u003d 2n 3 PO 4
فسفر با هالوژن ها با مقدار زیادی گرما ارتباط برقرار می کند. C F، CL، BR فرم تریالیز و پنتاگلینز، با I - فقط RI 3 Triodid. تمام هالید های فسفر به راحتی هیدرولیز شده اند به Orthophofforfors H 3 PO 4، فسفر H 3 PO 3 و هیدروچیک های های سلولی:
RSL 5 + 4N 2 O \u003d H 3 PO 4 + 5NSL
PI 3 + 3H 2 O \u003d H 3 PO 3 + 3HI
تریالیدس فسفر یک هرم مثلثی است که در پایه اتم های هالوژن قرار دارد و بالا یک اتم فسفر است. مولکول پنتاگالیید دو هرم مثلثی است که دارای لبه مشترک هستند. Oxygaloids فسفر ROF 3، ROSL 3 و ROBR 3 به دست آمد.
با فسفر خاکستری، سولفید P 4 S 3، P 4 S 5، P 4 S 7، P 4 S 10. شناخته شده فسفرس اکسیولفید ها: P 2 O 3 S 2، P 2 O 2 S 3، P 4 O 4 S 3، P 6 O 10 S 5، P 4 O 4 S 3. فسفر با SE و TE واکنش نشان می دهد، ترکیبات فرم های Si و C (PC 3).
با هیدروژن، به طور مستقیم به واکنش وارد نمی شود. هنگامی که تعامل با یک محلول رقیق شده از هیدروکسید پتاسیم، یک فسفین گاز PH 3 تشکیل شده است:
4P + 3KONE + 3H 2 O \u003d 3KN 2 PO 2 + PH 3
به عنوان ناخالصی، دی فسفراین P 2 H 4 نیز تشکیل شده است. هر دو فسفین دارای بوی مشخصی از ماهی های فاسد هستند.
فسفین pH 3 خواص شیمیایی آمونیاک NH 3 را یادآوری می کند، اما کمتر پایدار است.
فسفر هنگام خوردن با فلزات واکنش نشان می دهد. با استفاده از قلیایی زمین های قلیایی، فسفید های یونیک M 3 P 2، زمانی که در تماس با آب قرار می گیرند، تجزیه می شوند:
Mg 3 P 2 + 6H 2 O \u003d 3mg (OH) 2 + 2PH 3،
CA 3 P 2 + 6N 2 O \u003d 3A (OH) 2 + 2rn 3
با انتقال فلزات، فسفر فسفات فلزی مانند Mn 3 P، FEP، Ni 2 P.
فسفر بخشی از اسیدهای معدنی است. این اسید ارتوفیسفریک H 3 PO 4 (نمکهای آن - Orthophosphates، Monohydrophosphates، Na 2 HPO 4 و دی هیدروفسفات، CA (H 2 PO 4) 2)؛ اسید متافسفوریک (HRO 3) n. (نمک های آن - متافسفات)، اسید فسفریک تک محور H 3 PO 2 (نمک آن - هیپوفسفوس، نان 2 PO 2)، اسید فسفر دو محور H 3 PO 3 (نمک - فسفیت، Na 2 HPO 3).
فسفر بخشی از استرها ارگانیک، الکل ها و اسیدها: فسفین RRP (O) OH، فسفونی Rh 2 Po 2 و فسفونیوم RP (O) (OH) 2، جایی که R و R رادیکال های آلی هستند.
کاربرد
فسفر سفید در تولید اسید فسفریک H 3 PO 4 (برای به دست آوردن فسفات غذا و مواد شوینده مصنوعی) استفاده می شود. این در تولید پوسته های آتش سوزی و دود، بمب استفاده می شود.
فسفر قرمز در تولید استفاده می شود کود معدنی، تولید مطابقت. فسفر در تولید آلیاژهای غیر آهنی فلزات به عنوان یک اکسیدا کننده استفاده می شود، به عنوان یک افزودنی دوپینگ عمل می کند. در هنگام تولید فسفات های نیمه هادی، در تولید آلیاژهای مغناطیسی استفاده می شود. ترکیبات فسفر به عنوان مواد اولیه برای تولید داروها خدمت می کنند.
محتویات بدن
فسفر در سلول های زنده در شکل اسیدهای ارتوپدی و پریروفسفریک وجود دارد، در ترکیب نوکلئوتید، اسیدهای نوکلئیک، فسفوپروپروتئین ها، فسفولیپید ها، کمانزیم ها، آنزیم ها گنجانده شده است. استخوان های یک فرد شامل هیدروکسیلاپاتیت 3AS 3 (PO 4) 3 · CAF 2. ترکیب مینای دندانپزشکی وارد فلوروپاتیت می شود. نقش اصلی در تبدیل ترکیبات فسفر در بدن انسان و حیوان، کبد را بازی می کند. تبادل اتصالات فسفریک او توسط هورمون ها و ویتامین D تنظیم می شود. نیاز روزانه یک فرد در فسفر 1-2، با کمبود فسفر در بدن، بیماری های مختلف استخوان توسعه می یابد.
عمل فیزیولوژیکی
ترکیبات فسفر سمی هستند. دوز کشنده فسفر سفید - 50-150 میلی گرم. گرفتن پوست، فسفر سفید باعث سوختگی های سنگین می شود. مواد مسمومیت رزمی زرین، زون، تابون، ترکیبات فسفر هستند. فسفر مسمومیت حاد با سوزاندن در دهان و معده، سردرد، ضعف، استفراغ ظاهر می شود. پس از 2-3 روز، زردی توسعه می یابد. برای اشکال مزمن، نقض تبادل کلسیم، آسیب به قلب و عروق و سیستم های عصبی. کمک های اولیه برای مسمومیت حاد شستشو معده، ملین، پاک کننده های پاک کننده، محلول های گلوکز داخل وریدی است. در صورت سوختگی پوست برای درمان مناطق آسیب دیده با راه حل های مس یا سودا. PDC بخار فسفر در هوا 0.03 mg / m 3. گرد و غبار قرمز فسفر، سقوط به ریه ها، باعث ایجاد پنومونی می شود.
دیکشنری دایره المعارف. 2009 .
مترادف:سازمان دیده بان "فسفر" در سایر واژه نامه ها:
- (یونانی، از نور Phos، و حامل فوروس). یک بدن ساده، رنگ زرد، به راحتی قابل اشتعال و درخشان در تاریکی است. یک فرهنگ لغت از کلمات خارجی موجود در زبان روسی. Chudinov A.N.، 1910. فسفر یونانی. فسفر، از Phos، جنس. پد ... ... ... فرهنگ لغت کلمات خارجی زبان روسی
فسفر - فسفر، شیمی. عنصر (نماد R) با در. که در. 31.02 متعلق به گروه V و ردیف سوم سیستم Mendeleev دوره ای (شماره توالی 15). F. گسترده در طبیعت، اما تنها در قالب ترکیبات اکسیژن: خاک شامل آن است به شکل نمک ... ... دایره المعارف پزشکی بزرگ
فسفر - این جامد، خفیف و پلاستیک در سازگاری است که به دست آمده از طریق درمان فسفات های طبیعی مخلوط با شن و ماسه و کربن، در یک کوره الکتریکی. دو نوع اصلی فسفر وجود دارد: الف) فسفر سفید، ... ... اصطلاحات رسمی
- (نماد P)، عنصر شیمیایی گروه پنجم جدول تناوبی، که ابتدا در سال 1669 کشف شد. این در قالب فسفات در مواد معدنی، منبع اصلی آپاتیت فسفر است. این عنصر برای تولید اسید فسفریک استفاده می شود ... ... دیکشنری دانشنامه علمی و فنی
- (فسفر)، P، عنصر شیمیایی گروه V گروه دوره ای، تعداد اتمی 15، وزن اتمی 30،97376؛ سفید غیر فلزی (درخشان در هوا، شیر 44،14Scc)، قرمز (ضربه بزنید 593SCC) یا سیاه و سفید (TPL 1000SHC) رنگ. استفاده از فسفر در ... ... دایره المعارف مدرن
- (لات فسفر) P، عنصر شیمیایی گروه V از سیستم Mendeleev دوره ای، تعداد اتمی 15، وزن اتمی 30،97376. نام از یونانی. فسفر درخشان. چندین تغییر فسفر سفید (تراکم 1،828 گرم در سانتی متر و Sup3، TP ... ... دیکشنری دایره المعارف بزرگ
فسفر - (فسفر)، P، عنصر شیمیایی گروه V گروه دوره ای، تعداد اتمی 15، وزن اتمی 30،97376؛ Nonmetall White (درخشان در هوا، TPL 44،14 درجه سانتیگراد)، قرمز (TPL 593 ° C) یا سیاه (شیر 1000 درجه سانتیگراد) رنگ ها. استفاده از فسفر در ... ... دیکشنری دایره المعارف نشان داده شده است
فسفر - a، m فسفور M.gr. Phos Light + Foros Carrier. یک عنصر شیمیایی معمولی که نقش مهمی در فعالیت حیاتی حیوانات و گیاهان ایفا می کند. سفید، قرمز، فسفر سیاه. باس 1. فسفر های طبیعی و مصنوعی وجود دارد ... فرهنگ لغت تاریخی Glicalism زبان روسی
P (لات فسفر * a. فسفر؛ فسفر N. فسفر؛ فسفور؛ و fosforo)، شیمی. عنصر V گروه دوره ای. سیستم های Mendeleeva، AT.N. 15، در متر 30،97376. طبیعی F. توسط یک ایزوتوپ پایدار 31P نشان داده شده است. این 6 هنر شناخته شده است ... ... دانشنامه زمین شناسی
فسفر، فسفر، Mn. بدون شوهر. (یونانی فسفر فسفر) (شیمی). عنصر شیمیایی، به راحتی قابل اشتعال و درخشان در ماده تاریک موجود در برخی از مواد معدنی، در استخوان های حیوانات، در حیوانات و بافت های گیاهی. ... ... فرهنگ لغت ushakova
IIP Lucifer Prophorus، Lucifer)، I.E.، یک حامل نور. نام سیاره زهره به عنوان یک ستاره صبحگاهی. به عنوان ستاره شب، او Gesprer یا Vesper نامیده شد، و پسر Astrey و EOS، پدر Hesperid بود. (
تعریف
فسفر سفید این یکی از تغییرات آلوتروپیک عنصر شیمیایی فسفر است (شکل 1). این شامل مولکول های P 4 است.
متاستاز، در دمای اتاق نرم به عنوان موم (برش توسط یک چاقو)، در سرد - شکننده است. ذوب و جوش بدون تجزیه، پرواز با حرارت ضعیف، با بخار آب تقطیر می شود. به آرامی در هوا اکسید شده (واکنش زنجیره ای با مشارکت رادیکال ها، شیمی درمانی)، با حرارت ضعیف قابل اشتعال در حضور اکسیژن. این به خوبی در کربن سروو، آمونیاک، اکسید گوگرد (IV) محلول است، ضعیف - در تتراکلرید کربن. این در آب حل نمی شود، آن را به خوبی تحت لایه آب حفظ می شود.
شکل. 1. فسفر سفید. ظاهر.
فرمول شیمیایی فسفر سفید
فرمول شیمیایی فسفر سفید - P 4 این نشان می دهد که ترکیب مولکول های این ماده چهار اتم فسفر است (Ar \u003d 31 A.M.). با فرمول شیمیایی، شما می توانید محاسبه کنید وزن مولکولی فسفر سفید:
MR (P 4) \u003d 2 × AR (P) \u003d 4 × 31 \u003d 124
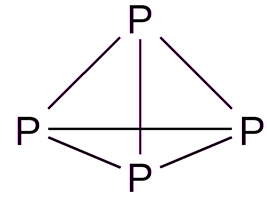
فرمول فسفات سفید ساختاری (گرافیکی)
بصری بیشتر است فرمول فسفات سفید ساختاری (گرافیکی). این نشان می دهد که چگونه اتم ها بین خود در داخل مولکول متصل می شوند. فرمول ساختاری فسفر سفید فرم دارد:
فرمول الکترونیکی
فرمول الکترونیکینشان دادن توزیع الکترونها در یک اتم از زیر انرژی های انرژی زیر نشان داده شده است:
15 P 1S 2 2S 2 2P 6 3S 2 3P 3
همچنین نشان می دهد که فسفر به عناصر خانواده R، و همچنین تعداد الکترون های والنس اشاره دارد - 5 الکترون در سطح انرژی خارجی (3S 2 3P 3) واقع شده اند.
نمونه هایی از حل مشکلات
مثال 1
| وظیفه | فرمول جرم ماده حاوی 55.2٪ از پتاسیم، 6/14٪ فسفر و اکسیژن 30.2٪ را تنظیم کنید. |
| تصمیم |
مقدار عناصر مول را که در ترکیب برای "X" (پتاسیم)، "Y" (فسفر) و "Z" (اکسیژن) وجود دارد، نشان می دهد. سپس، نسبت مولر به شرح زیر خواهد آمد (مقادیر توده های اتمی نسبی گرفته شده از جدول تناوبی D.I. مندلیف، گرد به عدد صحیح): x: y: z \u003d ω (k) / ar (k): ω (p) / ar (p): ω (O) / AR (O)؛ x: Y: Z \u003d 55.2 / 39: 14.6 / 31: 30.2 / 16؛ x: Y: Z \u003d 1.4: 0.5: 1،9 \u003d 3: 1: 4 بنابراین، فرمول ترکیب پتاسیم، فسفر و اکسیژن یک فرم K 3 PO 4 خواهد داشت. این فسفات پتاسیم است. |
| پاسخ | K 3 PO 4 |
مثال 2
| وظیفه | اکسید نیتروژن حاوی 63.2٪ اکسیژن است. فرمول اکسید چیست؟ |
| تصمیم | کسری توده ای از عنصر X در مولکول ترکیب HX با توجه به فرمول زیر محاسبه می شود: Ω (x) \u003d n × AR (x) / m (hx) × 100٪ محاسبه سهم جرم نیتروژن در اکسید: Ω (n) \u003d 100٪ - ω (o) \u003d 100٪ - 63.2٪ \u003d 36.8٪ مقدار مول از عناصر موجود در ترکیب برای "X" (نیتروژن) و "Y" (اکسیژن) را نشان می دهد. سپس، نسبت مولر به شرح زیر خواهد آمد (مقادیر توده های اتمی نسبی گرفته شده از جدول تناوبی D.I. مندلیف، گرد به عدد صحیح): x: y \u003d ω (n) / ar (n): ω (o) / ar (o)؛ x: Y \u003d 36.8 / 14: 63.2 / 16؛ x: y \u003d 2.6: 3،95 \u003d 1: 2 بنابراین، فرمول ترکیب نیتروژن و اکسیژن هیچ 2 مشاهده نخواهد شد. این اکسید نیتروژن (IV) است. |
| پاسخ | شماره 2 |
فسفر در شکل سه اصلی وجود دارد تغییرات آلوتروپیک (کل فسفر حدود 11 است):
1. فسفر سفید -ماده کریستالی سفید با بوی عجیب و غریب.
t pl \u003d 44 ° CС، T KIP \u003d 280 درجه سانتیگراد در قالب مولکول های P 4 وجود دارد.
نامحلول در آب. نرم فرار. به راحتی قابل اشتعال (در حال حاضر در 40 درجه سانتیگراد). اکسیداسیون در هوا همراه با درخشش است. بسیار سمی (حتی از طریق پوست)! این قادر به جمع آوری در بدن است و منجر به نکروز بافت های استخوانی (به خصوص فک) می شود. دوز مرگبار - 0.05 ... 0.15 گرم.
این بسیار شیمیایی بسیار فعال است، بنابراین آن را تحت آب و در تاریکی ذخیره می شود.
آن را با خنک کننده سریع بخار فسفر قرمز تبدیل می شود.
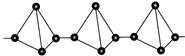 2. فسفر قرمز -ماده کریستالی قرمز بنفش قرمز بنفش نامحلول در آب است. سمی نیست، نه درخشش. کمتر واکنشی این فقط در دمای 210 درجه سانتیگراد قابل اشتعال است. این یک ساختار پلیمری P N دارد.
2. فسفر قرمز -ماده کریستالی قرمز بنفش قرمز بنفش نامحلول در آب است. سمی نیست، نه درخشش. کمتر واکنشی این فقط در دمای 210 درجه سانتیگراد قابل اشتعال است. این یک ساختار پلیمری P N دارد.
 با گرمای طولانی مدت (50 ساعت) گرمای فسفر سفید ("280 درجه سانتیگراد) تبدیل می شود.
با گرمای طولانی مدت (50 ساعت) گرمای فسفر سفید ("280 درجه سانتیگراد) تبدیل می شود.
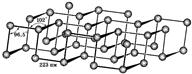
3. فسفر سیاه -پایدار ترین شکل عنصر یک ماده سیاه و سفید با درخشش فلزی، چربی به لمس و بسیار شبیه به گرافیت است، و با حلالیت کاملا غیر وابسته در آب یا حلال های آلی. غلظت فسفر سیاه و سفید تنها می تواند در فضای اکسیژن خالص به 400 درجه سانتیگراد بسیار داغ باشد. فسفر سیاه جریان الکتریکی را انجام می دهد و دارای خواص نیمه هادی است. نقطه ذوب فسفر سیاه - 1000 درجه سانتیگراد تحت فشار 18 × 10 5 PA. قابل اشتعال در دمای 500 درجه سانتیگراد. سمی نیست، کم موثر است.
آن را از فسفر سفید در 220 درجه سانتی گراد و فشار 1.2 GPA (13000 دستگاه خودپرداز)