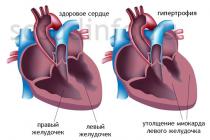
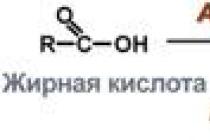
بیماری انسداد مزمن ریوی (COPD) بیماری است که در آن تا حدی محدودیت جریان هوا در مجاری تنفسی وجود دارد. تغییرات غیرقابل برگشت هستند ، COPD تهدیدی برای زندگی انسان است.
امتیاز کلیدی:
در COPD شدید ، ترکیب گاز خون تعیین می شود.
اگر درمان بی اثر باشد ، خلط برای تجزیه و تحلیل باکتری گرفته می شود.
رفتار
بیماری انسدادی مزمن ریوی یک بیماری لاعلاج است. با این حال ، درمان کافی می تواند دفعات تشدید را کاهش داده و عمر بیمار را به طور قابل توجهی طولانی کند. برای درمان COPD از داروهایی استفاده می شود که لومن برونش ها و عوامل موکلیتیکی را که بلغم را نازک می کنند گسترش می دهد و باعث دفع آن از بدن می شود.
برای تسکین التهاب ، گلوکوکورتیکوئید تجویز می شود. اما استفاده طولانی مدت از آنها به دلیل عوارض جانبی جدی توصیه نمی شود.
در طول دوره تشدید بیماری ، اگر ماهیت عفونی آن ثابت شود ، بسته به حساسیت میکروارگانیسم ، آنتی بیوتیک یا عوامل ضد باکتری تجویز می شود.
برای بیماران مبتلا به نارسایی تنفسی ، اکسیژن درمانی تجویز می شود.
بیماری انسدادی مزمن ریوی (COPD) یک بیماری تهدید کننده زندگی است. تعداد مرگ و میرها در سال در سراسر جهان به 6 درصد از کل مرگ ها می رسد.
این بیماری ، که با آسیب طولانی مدت به ریه ها رخ می دهد ، در حال حاضر غیر قابل درمان در نظر گرفته می شود ؛ درمان فقط می تواند فرکانس و شدت تشدید را کاهش دهد و میزان مرگ و میر را کاهش دهد.
COPD (بیماری انسدادی مزمن ریوی) بیماری است که در آن جریان هوا در مجاری تنفسی محدود می شود که تا حدی قابل برگشت است. این انسداد به طور مداوم در حال پیشرفت است ، عملکرد ریه را کاهش می دهد و منجر به نارسایی تنفسی مزمن می شود.
در تماس با
چه کسی مبتلا به COPD است
COPD (بیماری انسدادی مزمن ریوی) عمدتا در افرادی که سالها سابقه سیگار کشیدن دارند ایجاد می شود. این بیماری در بین مردان و زنان در سراسر جهان شیوع یافته است. بیشترین مرگ و میر مربوط به کشورهایی است که سطح زندگی پایین دارند.
منشا بیماری
با تحریک طولانی مدت ریه ها با گازهای مضر و میکروارگانیسم ها ، التهاب مزمن به تدریج ایجاد می شود. نتیجه این امر باریک شدن نایژه ها و تخریب آلوئول های ریه است. در آینده ، کلیه دستگاه تنفسی ، بافت ها و رگ های ریه تحت تأثیر قرار می گیرند و منجر به آسیب شناسی های غیر قابل برگشت می شوند که باعث کمبود اکسیژن در بدن می شوند. COPD (بیماری انسدادی مزمن ریوی) به آرامی ایجاد می شود و طی سالهای متمادی به طور مداوم پیشرفت می کند.
در صورت عدم درمان ، COPD منجر به ناتوانی و سپس مرگ می شود.
دلایل اصلی بیماری

- سیگار کشیدن علت اصلی تا 90٪ موارد است.
- عوامل حرفه ای - کار در صنایع خطرناک ، استنشاق گرد و غبار حاوی سیلیسیم و کادمیوم (استخراج کنندگان ، کارگران ساختمانی ، کارگران راه آهن ، کارگران متالورژی ، کاغذ و کاغذ ، شرکت های پردازش غلات و پنبه) ؛
- عوامل وراثتی - کمبود مادرزادی نادر α1-آنتی تریپسین.
- سرفه اولین و غالباً دست کم گرفته شده است. در ابتدا ، سرفه دوره ای است ، سپس روزانه می شود ، در موارد نادر فقط در شب ظاهر می شود.
- - در مراحل اولیه بیماری به شکل مقدار کمی مخاط ، معمولاً صبح ظاهر می شود. با پیشرفت بیماری ، خلط چرکی و بیشتر و بیشتر می شود.
- تنگی نفس - تنها 10 سال پس از شروع توسعه بیماری یافت می شود. در ابتدا ، فقط با یک تمرین بدنی جدی خود را نشان می دهد. علاوه بر این ، احساس کمبود هوا نیز با حرکات جزئی بدن ایجاد می شود ، بعداً نارسایی تنفسی پیشرونده شدید ظاهر می شود.

این بیماری بر اساس شدت طبقه بندی می شود:
نور - با اختلال خفیف در عملکرد ریه. سرفه جزئی ظاهر می شود. در این مرحله ، بیماری به ندرت تشخیص داده می شود.
شدت متوسط \u200b\u200b- افزایش اختلالات انسدادی در ریه ها. تنگی نفس همراه با جسمی ظاهر می شود. بارها این بیماری با درمان بیماران در ارتباط با تشدید و تنگی نفس تشخیص داده می شود.
شدید - محدودیت شدید هوا رخ می دهد. تشدیدهای مکرر شروع می شود ، تنگی نفس افزایش می یابد.
بسیار شدید - با انسداد شدید برونش. وضعیت سلامتی به شدت خراب می شود ، تشدیدها تهدید می شوند ، ناتوانی ایجاد می شود.
روشهای تشخیصی

مجموعه آنامنیز - با تجزیه و تحلیل عوامل خطر. در افراد سیگاری ، شاخص سیگاری (IC) ارزیابی می شود: تعداد سیگارهای دودی روزانه در تعداد سیگار کشیدن ضرب می شود و در 20 تقسیم می شود. IC بیش از 10 نشان دهنده ابتلا به COPD است.
اسپیرومتری - برای ارزیابی عملکرد ریه. میزان هوا را در هنگام استنشاق و بازدم و سرعت ورود و خروج هوا نشان می دهد.
آزمایش با گشادکننده برونش - احتمال برگشت پذیری روند باریک شدن برونش را نشان می دهد.
معاینه اشعه ایکس - شدت تغییرات ریوی را مشخص می کند. همان کار انجام شده است.
تجزیه و تحلیل خلط - برای تعیین میکروب ها در هنگام تشدید و انتخاب آنتی بیوتیک ها.
تشخیص های افتراقی
از داده های اشعه ایکس برای تمایز از سل و همچنین آنالیز خلط و برونکوسکوپی استفاده می شود.
چگونه یک بیماری را درمان کنیم
قوانین عمومی
- سیگار کشیدن باید برای همیشه قطع شود. در صورت ادامه سیگار کشیدن ، هیچ درمانی برای COPD مDثر نخواهد بود.
- استفاده از تجهیزات حفاظت شخصی برای سیستم تنفسی ، کاهش ، در صورت امکان ، تعداد عوامل مضر در منطقه کار ؛
- منطقی ، تغذیه خوب؛
- کاهش به وزن طبیعی بدن
- ورزش منظم (ورزش تنفس ، شنا ، راه رفتن).
درمان دارویی

هدف آن کاهش دفعات تشدید و شدت علائم ، جلوگیری از ایجاد عوارض است. با پیشرفت بیماری ، دامنه درمان فقط افزایش می یابد. داروهای اساسی برای درمان COPD:
- گشاد كننده برونش عمده ترين داروهاي تحريك كننده انبساط برونش ها هستند (آتروونت ، سالمترول ، سالبوتامول ، فرموترول). ترجیحاً با استنشاق تجویز می شود. از داروهای کوتاه مدت در صورت لزوم استفاده می شود ، از داروهای طولانی مدت به طور مداوم استفاده می شود.
- گلوکوکورتیکوئیدها به شکل استنشاق - در بیماری شدید ، همراه با تشدید (پردنیزولون) استفاده می شود. با نارسایی شدید تنفسی ، حملات با گلوکوکورتیکوئیدها به صورت قرص و تزریق متوقف می شوند.
- واکسن ها - واکسیناسیون آنفلوانزا می تواند مرگ و میر را به نصف کاهش دهد. این یک بار در اکتبر - اوایل نوامبر انجام می شود.
- موکولیتیک - مخاط را نازک کرده و دفع آن را تسهیل می کند (کاربوسیستئین ، آمبروکسول ، تریپسین ، کیموتریپسین). فقط در بیماران با خلط چسبناک استفاده می شود.
- آنتی بیوتیک - فقط برای تشدید بیماری (پنی سیلین ها ، سفالوسپورین ها ، احتمالاً استفاده از فلوروکینولون ها) استفاده می شود. قرص ، تزریق ، استنشاق استفاده می شود.
- آنتی اکسیدان ها - می توانند فرکانس و مدت زمان تشدید را کاهش دهند ، در دوره های حداکثر شش ماهه استفاده می شود (N-استیل سیستئین).
عمل جراحی
- بولکتومی - برداشتن می تواند تنگی نفس را کاهش دهد و عملکرد ریه را بهبود بخشد.
- کاهش حجم ریوی توسط جراحی - تحت مطالعه است. این عمل می تواند وضعیت جسمی بیمار را بهبود بخشد و درصد مرگ و میر را کاهش دهد.
- پیوند ریه - به طور موثر کیفیت زندگی ، عملکرد ریه و عملکرد فیزیکی بیمار را بهبود می بخشد. برنامه با مشکل انتخاب اهداکننده و هزینه بالای عمل با مشکل روبرو می شود.
اکسیژن درمانی

اکسیژن درمانی برای اصلاح نارسایی تنفسی انجام می شود: کوتاه مدت - همراه با تشدید ، طولانی مدت - با درجه چهارم COPD. با یک دوره پایدار ، اکسیژن درمانی مداوم و طولانی مدت تجویز می شود (حداقل 15 ساعت در روز).
اکسیژن درمانی هرگز برای بیمارانی که به سیگار کشیدن ادامه می دهند یا از الکل رنج می برند تجویز نمی شود.
درمان با داروهای قومی

دم کرده های گیاهی... آنها با دم کردن یک قاشق مجموعه با یک لیوان آب جوش آماده می شوند و هر کدام از آنها ظرف 2 ماه مصرف می شود:
√ 1 قسمت مریم گلی ، 2 قسمت بابونه و گل مالو
√ 1 قسمت بذر کتان ، 2 قسمت از هر اکالیپتوس ، گلهای آهک ، بابونه ؛
√ 1 قسمت بابونه ، گل مالو ، شبدر شیرین ، توت انیسون ، ریشه شیرین بیان و گل ختمی ، 3 قسمت بذر كتان.
- تزریق تربچه. تربچه سیاه و چغندرهای متوسط \u200b\u200bرا رنده کنید ، مخلوط کرده و روی آب جوش خنک شده بریزید. بگذارید 3 ساعت بماند. 50 میلی لیتر سه بار در روز به مدت یک ماه بنوشید.
- گزنه ریشه های گزنه را به صورت خراطی خرد کرده و با شکر به نسبت 2: 3 مخلوط کرده و برای 6 ساعت بگذارید. شربت بلغم را از بین می برد ، التهاب را برطرف می کند و سرفه را تسکین می دهد.
- شیر:
√ با یک لیوان شیر ، یک قاشق سدریا (خزه ایسلندی) دم کرده ، در طول روز بنوشید.
√ در یک لیتر شیر ، 6 عدد پیاز خرد شده و یک عدد سیر را به مدت 10 دقیقه بجوشانید. بعد از غذا نیم لیوان بنوشید. هر مادری باید بداند!
طلسم های سرفه شب شما را بیدار نگه می دارد؟ ممکن است به نای مبتلا شوید. می توانید درباره این بیماری بیشتر بدانید
ثانوی
- فعالیت بدنی ، منظم و دوز ، با هدف عضلات تنفسی ؛
- واکسیناسیون سالانه با واکسن آنفلوانزا و پنوموکوک ؛
- مصرف مداوم داروهای تجویز شده و معاینات منظم توسط متخصص ریه.
- استفاده صحیح از استنشاقی ها.
پیش بینی
COPD پیش آگهی شرطی ضعیفی دارد. این بیماری به آرامی اما پایدار پیشرفت می کند و منجر به ناتوانی می شود. درمان ، حتی فعال ترین ، فقط می تواند این روند را کند کند ، اما آسیب شناسی را از بین نمی برد. در بیشتر موارد ، درمان مادام العمر است و دوزهای آن به طور مداوم افزایش می یابد.
با ادامه سیگار کشیدن ، انسداد بسیار سریعتر پیشرفت می کند و به طور قابل توجهی امید به زندگی را کوتاه می کند.
COPD لاعلاج و کشنده مردم را به ترک سیگار برای همیشه ترغیب می کند. و برای افراد در معرض خطر ، فقط یک توصیه وجود دارد - اگر علائمی از بیماری مشاهده کردید ، بلافاصله با یک متخصص ریه تماس بگیرید. به هر حال ، هرچه بیماری زودتر تشخیص داده شود ، احتمال مرگ زودرس کمتر است.
تغییرات پاتوفیزیولوژیک در COPD شامل تغییرات پاتولوژیک زیر است:
- بیش از حد ترشح مخاط ،
- اختلال عملکرد مژک ،
- انسداد برونش ،
- تخریب پارانشیم و آمفیزم ریه ها
- اختلالات تبادل گاز ،
- فشار خون ریوی،
- قلب ریوی ،
- مظاهر سیستمی
بیش از حد ترشح مخاط
ترشح بیش از حد مخاط در اثر تحریک غدد ترشحی و سلولهای جام توسط لکوترین ها ، پروتئینازها و نوروپپتیدها ایجاد می شود.اختلال عملکرد Cilia
اپیتلیوم مژه دار تحت متاپلازی سلول سنگفرشی قرار می گیرد ، که منجر به اختلال در ترخیص کالا از گمرک مخاطی می شود (تخلیه مختل شده خلط از ریه ها). این تظاهرات اولیه COPD می تواند سالها بدون پیشرفت ادامه داشته باشد.انسداد برونش
علل زیر انسداد برونش را مشخص می کند:- برگشت ناپذیر:
- بازسازی و فیبروز راه هوایی ،
- از دست دادن کشش الاستیک ریه در نتیجه تخریب آلوئول ،
- تخریب پشتیبانی آلوئولار برای لومن مجاری تنفسی کوچک ؛
- برگشت پذیر:
- تجمع سلولهای التهابی ، مخاط و ترشحات پلاسما در نایژه ها ،
- انقباض عضلات صاف برونش ،
- تورم بیش از حد دینامیکی در حین ورزش.
بیش از حد تورم ریوی
ابر تورم ریوی (PHI) - افزایش هوایی بافت ریه ، تشکیل و افزایش "بالشتک هوا" در ریه ها. بسته به علت وقوع ، به دو نوع تقسیم می شود:Static PHI: به دلیل تخلیه ناقص آلوئول در هنگام بازدم به دلیل کاهش کشش الاستیک ریه ها
PHI پویا: به دلیل کاهش زمان بازدم در شرایط محدود شده جریان هوای بازدم. از نظر پاتوفیزیولوژی ، PHI مکانیزم سازگار است ، زیرا منجر به کاهش مقاومت راه هوایی ، بهبود توزیع هوا و افزایش دقیقه تهویه در حالت استراحت می شود. با این حال ، LGI منجر به عواقب نامطلوب زیر می شود:
ضعف عضلات تنفسی. دیافراگم کوتاه و صاف شده است ، که باعث انقباضات آن می شود.
محدودیت در افزایش حجم جزر و مد در حین ورزش. در افراد سالم ، هنگام ورزش ، به دلیل افزایش دفعات و عمق تنفس ، حجم تنفس دقیقه افزایش می یابد. در بیماران مبتلا به COPD ، تورم بیش از حد ریوی در حین ورزش افزایش می یابد ، زیرا افزایش NPV در COPD منجر به کوتاه شدن مدت انقضا می شود و حتی هوا بیشتری در آلوئول ها حفظ می شود. افزایش "بالشتک هوا" عمق تنفس را به میزان قابل توجهی افزایش نمی دهد.
هیپرکاپنیا در حین ورزش. به دلیل کاهش نسبت OOL به VC به دلیل کاهش VC به دلیل PHI ، افزایش PaCO2 در خون شریانی رخ می دهد.
افزایش بار الاستیک بر روی ریه ها.
فشار خون ریوی. در نهایت ، PHI منجر به پرفشاری خون ریوی می شود.
آمفیزم ریه ها
تخریب پارانشیم منجر به کاهش کشش الاستیک ریه ها می شود و بنابراین با محدودیت سرعت جریان هوا و افزایش مقاومت هوا در ریه ها ارتباط مستقیم دارد. برونش های کوچک ، از دست دادن تماس با آلوئول ها ، که قبلا در حالت صاف بودند ، فرو می ریزند و قابل عبور نیستند.اختلالات تبادل گاز
انسداد مجاری هوایی ، تخریب پارانشیمال و اختلالات جریان خون ریوی ، ظرفیت ریه را برای تبادل گاز کاهش می دهد ، که ابتدا به هیپوکسمی و سپس به هیپرکاپنیا منجر می شود. همبستگی بین مقادیر عملکرد ریه و سطح گازهای شریانی ضعیف تعیین شده است ، اما با FEV1 بیش از 1 لیتر ، تغییرات قابل توجهی در ترکیب گاز خون به ندرت اتفاق می افتد. در مراحل اولیه ، هیپوکسمی فقط با اعمال جسمی رخ می دهد ، و با پیشرفت بیماری ، حتی در حالت استراحت.فشار خون ریوی
فشار خون ریوی در مرحله IV ایجاد می شود - یک دوره بسیار شدید COPD ، همراه با هیپوکسمی (PaO2 کمتر از 8 کیلو پاسکال یا 60 میلی متر جیوه) و اغلب نیز هایپرکاپنیا. این عارضه مهم قلبی عروقی COPD با پیش آگهی ضعیفی همراه است. معمولاً در بیماران مبتلا به COPD شدید ، فشار در شریان ریوی در حالت استراحت متوسط \u200b\u200bبالا می رود ، اگرچه در اثر فشار می تواند افزایش یابد. عارضه حتی بدون درمان به آرامی پیشرفت می کند. توسعه فشار خون ریوی مربوط به انقباض عروقی ریه ها و ضخیم شدن دیواره عروق به دلیل بازسازی عروق ریوی ، تخریب مویرگ های ریوی در آمفیزم است که فشار مورد نیاز برای عبور خون از ریه ها را بیشتر می کند. انقباض عروق می تواند به دلیل کمبود اکسیژن ایجاد شود ، که باعث انقباض عضلات صاف عروق ریوی ، اختلال در مکانیسم های گشادی عروق وابسته به اندوتلیوم (کاهش تولید NO) و ترشح پاتولوژیک پپتیدهای انقباض کننده عروق می شود. بازسازی عروق یکی از دلایل اصلی ایجاد فشار خون ریوی است که به نوبه خود به دلیل آزاد شدن فاکتورهای رشد یا به دلیل استرس مکانیکی در هنگام انقباض عروق هیپوکسی است.قلب ریوی
پرفشاری خون ریوی به عنوان "هیپرتروفی بطن راست" ناشی از بیماری های م theثر بر عملکرد و / یا ساختار ریه ها تعریف می شود ، به استثنای سایر اختلالات ریوی که ناشی از بیماری هایی هستند که در قلب چپ تأثیر می گذارند ، مانند بیماری های مادرزادی قلب. فشار خون ریوی و کاهش بستر عروقی به دلیل آمفیزم منجر به هیپرتروفی بطن راست و از کار افتادن آن فقط در برخی از بیماران می شود.مظاهر سیستمیک
در COPD ، التهاب سیستمیک و اختلال عملکرد عضلات اسکلتی وجود دارد. التهاب سیستمیک با وجود استرس اکسیداتیو سیستمیک ، افزایش غلظت سیتوکین های در گردش و فعال شدن سلول های التهابی آشکار می شود. اختلال عملکرد عضلات اسکلتی با از بین رفتن توده عضلانی و انواع اختلالات انرژی زیستی آشکار می شود. این تظاهرات منجر به محدودیت توانایی های جسمی بیمار می شود ، سطح سلامتی را کاهش می دهد ، پیش آگهی بیماری را بدتر می کند.مشخصات عمومی و تصویر بالینی بیماری انسدادی مزمن ریوی ، علل و عوامل توسعه آن. علت شناسی و پاتوژنز این بیماری ، اصول تشخیص. تهیه یک رژیم درمانی و پیش آگهی ، جلوگیری از عود.
ارسال کارهای خوب شما در پایگاه دانش ساده است. از فرم زیر استفاده کنید
دانشجویان ، دانشجویان تحصیلات تکمیلی ، دانشمندان جوان که از دانش استفاده می کنند در کار و کار خود بسیار سپاسگزار شما خواهند بود.
ارسال شده در http://www.allbest.ru/
تاریخبیماری
تشخیص بالینی:
بیماری اصلی: COPD ، نوع آمفیزماتیک ، دوره شدید (III مرحله) ، تشدید شدت متوسط.
عوارض: آمفیزم ریه ها. پنوموسکلروز
بیماری های همراه: مرحله فشار خون بالا 3 با فشار خون شریانی 2 درجه ، خطر 4. زخم معده و12 - توزخم اثنی عشر ، بهبودی دورسوپاتی ستون فقرات قفسه سینه. حنجره هایپرتروفیک مزمن.
1. شکایت
در زمان نظارت ، بیمار از سرفه در طول روز شکایت دارد ، که کمتر در شب مشاهده می شود ، با مقدار کمی خلط مخاطی ، بیشتر اوقات صبح. تنگی نفس در هنگام سرفه و بعد از آن اتفاق می افتد.
2. سابقه بیماری فعلی
بیماری مزمن عود آسان
از سال 2006 ، خود را برای چندین سال بیمار می داند ، هنگامی که ، در برابر پس زمینه ARVI ، سرفه در طول روز با ترشح خلط مخاطی ، اغلب در صبح ، تنگی نفس پیشرونده ظاهر می شود. بیمار به پلی کلینیک محل زندگی خود مراجعه کرد و در آنجا پس از معاینه ، آسم برونش متوسط \u200b\u200bرا تشخیص داد و درمان را تجویز کرد. برای این بیماری ، او دائماً سرتید ، Berotek و Ditek را مصرف می کند. او از سپتامبر 2013 ، هنگامی که تنگی نفس و سرفه افزایش می یابد ، تحمل ورزش کاهش می یابد ، همراه با افزایش تعداد حملات به روزانه ، وضعیت خود را بدتر می کند. وی در محل زندگی خود تحت معالجه بستری قرار گرفت. با وجود درمان ، وضعیت سلامتی بیمار بهبود نیافت ، سرفه همراه با ترشح خلط مخاطی ، افزایش تنگی نفس ، با توجه به عدم تأثیر درمان ، بیمار برای درمان و بررسی بیشتر در بخش درمانی بستری شد. هنگام پذیرش ، بیمار از تنگی نفس با اعمال جسمی ناچیز ، سرفه متناوب با خلط سبز زرد شکایت کرد. حملات تنگی نفس بیشتر در شب رخ می دهد ، بلکه در صبح نیز رخ می دهد. حمله با سالبوتامول متوقف می شود. بیمار همچنین از سردرد ، سرگیجه ، تعریق ، تب تا 37.5 درجه شکایت داشت.
3. تاریخ زندگی
با توجه به سن و جنسیت رشد کرده و رشد کرده است. 12.09.1954 سال تولد (59 ساله). به عنوان تنها فرزند خانواده به دنیا آمد. در زمان تولد ، مادر و پدر سالم هستند. تحصیلات تخصصی متوسطه دارد. وی 2 سال در ارتش خدمت کرد.
وی متاهل است و فرزندی ندارد. وی از سن 18 سالگی به عنوان جوشکار ، نجار ، چوب بری شروع به کار کرد. او شیفت شب کار کرد ، در یک پیش نویس وارد شد. یک معلولیت گروه 2 وجود دارد.
شرایط زندگی خوب است. تغذیه در طول زندگی: کامل ، منظم ، تمام قوانین بهداشت را رعایت می کند ، یک سبک زندگی منفعل را دنبال می کند. بیماری های منتقل شده در دوران کودکی: سرخک ، سرماخوردگی مکرر. وی در مورد واکسیناسیون پیشگیرانه به یاد نمی آورد.
عادت های بد - از 10 سالگی سیگار می کشد ، حدود 10 سیگار در روز. الکل می نوشد. سایر عادت ها را انکار می کند.
سابقه وراثت - مادر از فشار خون بالا رنج می برد ، پدر در سن 56 سالگی بر اثر سرطان معده درگذشت.
بیماری Botkin ، سل ، زردی ، بیماری های وریدی منکر می شوند. وجود واکنش های آلرژیک به داروها - جنتامایسین ، آمپی سیلین ، خود را به صورت برونکوسپاسم نشان می دهد. تنگی نفس هنگام بیرون رفتن در هوای سرد ، در سرما ، روی لاک و رنگ رخ می دهد. از سال 2006 او دییتک ، بروتک ، سالبوتامول مصرف کرده است.
4. حالت فعلی (وضعیت praesens)
بازرسی عمومی
یکی) شرایط راضی کننده است. دمای بدن 36.8 درجه سانتی گراد
2) موقعیت بیمار در رختخواب فعال است.
3) هوشیاری روشن است.
4) حالت صورت آرام است.
5) قد - 175 سانتی متر وزن بدن - 115 کیلوگرم هیکل فوق هیستن است. حالت صاف ، راه رفتن سریع است. شاخص توده بدن - 37.5 کیلوگرم در متر مربع.
6) پوست آکروسیانوز خفیف و ملایم است (نقض اکسیژن رسانی خون در ریه ها منجر به افزایش محتوای هموگلوبین کاهش یافته در بافت ها می شود). در لمس ، پوست مرطوب است. پوست الاستیک است. بثورات پوستی وجود ندارد. تورگور کاهش می یابد. ناخن های صورتی ، بدون تغییر قابل مشاهده است. رنگ غشاهای مخاطی قابل مشاهده صورتی کم رنگ است ، هیچ جوش وجود ندارد. لمس ، درد ، حساسیت به درجه حرارت حفظ می شود ، هیچ هیپرستزی وجود ندارد.
7) درجه تکامل چربی زیر پوستی بیش از حد است. بافت چربی زیر جلدی هنگام لمس بدون درد است. ادم محیطی در یک سوم تحتانی ساق پا در هر دو طرف.
8) گره های لنفاوی: زیر فکی ، پس سری ، دهانه رحم ، زیر بغل ، فوق- ، زیر کلاوین ، قابل لمس نیستند.
نه). سیستم اسکلتی عضلانی:
عضلات: رشد عضلات رضایت بخش است. در هنگام احساس درد وجود ندارد. آنها به طور متقارن در حرکت شرکت می کنند.
استخوان: هنگام احساس و ضربه استخوانها بدون درد هستند. در معاینه ، هیچ تغییر شکل وجود ندارد.
اتصالات: پیکربندی طبیعی. تورم ، نوسان (وجود افیوژن در مفاصل) وجود ندارد. دمای پوست روی مفاصل طبیعی است. لمس و حرکت مفاصل بدون درد است.
عملکرد مفاصل حفظ می شود ، هنگام حرکت هیچ تردی وجود ندارد. حجم حرکات فعال و غیرفعال در تمام مفاصل و قسمتهای ستون فقرات طبیعی است.
دستگاه تنفسی
بازرسی. بینی: شکل بینی تغییر نمی کند. تنفس آزاد از طریق بینی. تغییر شکل بافت های نرم ، قرمزی و زخم در لبه خارجی سوراخ های بینی ، عدم وجود بثورات هرپیت. وضعیت مخاط بینی مطلوب است.
حنجره: عدم تغییر شکل و تورم در ناحیه حنجره. صدا بلند ، واضح است.
قفسه سینه: شکل قفسه سینه آمفیزماتیک است. افزایش اندازه عرض و خلفی خلفی قفسه سینه ، زاویه اپی گاستریک مستقر (بیش از 90 درجه) ، جهت افقی دنده ها و افزایش فضاهای بین دنده ای ، در نواحی فوق کلاک تورم مشخص وجود دارد ، افزایش قابل توجهی در فضاهای بین دنده ای ، کاهش کشش سینه ، انعطاف پذیری تیغه های شانه به سینه ... قفسه سینه متقارن است.
تنفس: نوع تنفس مخلوط است. حرکات تنفسی متقارن هستند. میزان تنفس 23 در دقیقه. تنفس کم ریتمیک ، طولانی شدن مرحله استنشاق و بازدم.
لمس کردن با لمس ، مناطق دردناک مشخص نشد. کاهش کشش قفسه سینه. لرزش صدا متقارن ، میرایی دو طرفه.
کوبه ای ریه
کوبه ای مقایسه ای: در نواحی متقارن قفسه سینه ، صدای جعبه کوبه ای مشخص می شود.
کوبه توپوگرافی:
مرز بالایی ریه ها: راست چپ
ارتفاع ایستاده تاپس در جلو 6 سانتی متر 6 سانتی متر
ارتفاع ایستاده تاپس پشت 8 سانتی متر 8 سانتی متر
عرض لبه Krenig 9 سانتی متر 9 سانتی متر
مرز پایین ریه:
در امتداد خط پیر استخوان 7 ، فضای بین دنده ای تعیین نشده است
در امتداد خط میانی ترقوه 7 ، دنده تعریف نشده است
در امتداد خط زیر بغل 8 دنده 8 دنده
خط زیر بغل 9 دنده 9 دنده
روی خط زیر بغل 10 دنده 10 دنده
در امتداد خط کتف 11 دنده 11 دنده
در امتداد خط مهره ای فرآیند چرخشی فرآیند چرخشی
11 مهره قفسه سینه 11 مهره قفسه سینه
گردش تنفسی در لبه پایین ریه
در امتداد خط میانی ترقوه در امتداد خط زیر بغل خلفی
در امتداد خط کتف
سکوت تنفس وزیکولار ضعیف در نواحی متقارن قفسه سینه شنیده می شود. در ریه ها ، رال های خشک با رنگ های مختلف در تمام زمینه های ریوی شنیده می شوند. برونکوفونی بیش از نواحی متقارن سینه در هر دو طرف ضعیف شده است.
سیستم قلبی عروقی
معاینه و لمس ناحیه قلب. تغییر شکل قفسه سینه و ضربان قلب در ناحیه قلب مشاهده نشد. در معاینه ، تکانه و ضربان قلب در ناحیه اپی گاستریک تشخیص داده نمی شود. ضربه آپیکال در فضای بین دنده ای 5 در سمت چپ 2 سانتی متر از لاین لمس می شود. medioclavicularis ، موضعی ، ریخته نشده ، تقویت نشده است. ضربه بطن راست و تپش قلب در قلب با لمس تشخیص داده نمی شود.
کوبه ای قلب. مرزهای تیرگی نسبی قلب:
راست - در فضای بین دنده ای 4 و 1.5 سانتی متر از لبه سمت راست جناغ به سمت خارج.
بالا - در سطح دنده 3 در امتداد l. parasternalis sinistrae؛
چپ - در فضای بین دنده ای 5 و به فاصله 1.5 سانتی متر از خط میانی کراسکولار.
مرزهای تیرگی مطلق قلب:
راست - در لبه سمت چپ جناغ در فضای بین دنده ای 4 ؛
بالا - در سطح دنده 4 در امتداد l. parasternalis sinistrae؛
سمت چپ - 2 سانتی متر از l به داخل. medioclavicularis در فضای بین دنده ای 5.
قطر قلب: 12 سانتی متر (با سرعت 12 - 12.5 سانتی متر).
عرض بسته نرم افزاری عروقی: حدود 5 سانتی متر (در فضای بین دنده ای 1 و 2 فراتر از جناغ نمی رود).
2 صدای اساسی قلب وجود دارد. بدون شکاف و انشعاب صدای II. انشعاب صدای I وجود ندارد. هیچ کلیک برای باز کردن دریچه کانتر و دریچه میترال وجود ندارد. ضربان قلب در دقیقه / 70 ، ریتمیک ، ایمن ، در مکان های اصلی گوش دادن ضعیف می شوند. هیچ سوفل پاتولوژیک یافت نشد.
تحقیق در مورد رگهای خونی. تپش در ناحیه دسته جناغ ، "رقص کاروتید" ، عدم ایجاد شکنجه در عروق. واریس اندام تحتانی وجود ندارد. رنگ آمیزی پوست اندام طبیعی است. واریس وجود ندارد. هیچ زخم تروفیک وجود ندارد. قوس و آئورت شکم قابل لمس نیست. نبض شریانی در شریان های شعاعی: در عروق شعاعی هر دو بازو ، ریتمیک ، فرکانس طبیعی - 70 ضربان در دقیقه ، پرشدن خوب ، کشش طبیعی ، اندازه ، سرعت و شکل. نقص نبض وجود ندارد. معاینه و لمس عروق در مناطق دیگر بدون آسیب شناسی. وضعیت دیواره عروق رضایت بخش است.
دمای پوست اندام طبیعی است ، همان. فشار خون در شریان بازویی راست مطابق با فشار خون در شریان بازویی چپ است و برابر با 110/80 است.
دستگاه گوارش
معاینه حفره دهان. مرز قرمز لب ها به رنگ معمول است ، هیچ راش وجود ندارد. لقمه درست است. لثه خونریزی نمی کند. شل شدن ، زخم ، بثورات وجود ندارد. زبانی با شکل منظم ، اندازه طبیعی ، رنگ طبیعی ، بدون پلاک ، زخم و تومور ، در مرکز قرار دارد. مخاط آن صورتی کمرنگ ، براق و بدون زخم است. لوزه ها بزرگ نشده اند. قوس پالاتین بدون تغییر. خونریزی و زخم در مخاط دهان وجود ندارد.
معاینه شکم. شکل درست است ، یک افزایش کلی وجود دارد. هر دو نیمه شکم متقارن هستند. هیچ منطقه ای از رنگدانه ، بثورات پوستی ، خراشیدن ، خونریزی وجود ندارد. هیچ وثیقه وریدی وجود ندارد. در عضلات راست روده شکم فتق و اختلاف وجود ندارد. ناف جمع شده است.
لمس سطحی شکم. دیواره شکم نرم ، بدون تنش ، بدون درد است. برجستگی های فتق مشخص نشده است.
لمس عمیق کور روده واقع در یک سوم میانی فاصله از ناف تا تاج استخوان ایلیاک ؛ قطر حدود 3 سانتی متر ؛ کشسان؛ دیوار صاف ، یکنواخت ، تحرک کافی (2 سانتی متر) است. بدون درد سر و صدا تشخیص داده نمی شود
روده بزرگ سیگموئید به درستی واقع شده است قطر حدود 2 سانتی متر ؛ کشسان؛ دیوار صاف ، یکنواخت ، تحرک کافی (3 سانتی متر) است. بدون درد سر و صدا تشخیص داده نمی شود
روده بزرگ ، عرض های صعودی و نزولی آن به درستی واقع شده است قطر حدود 2 سانتی متر ؛ کشسان؛ دیوار صاف ، یکنواخت ، تحرک کافی (2 سانتی متر) است. بدون درد سر و صدا تشخیص داده نمی شود
تومورهای سطحی وجود ندارد.
کوبه ای صداهای کوبه ای در بخشهای مختلف طبیعی است. تومور وجود ندارد. هیچ مایع آزاد و محصور شده ای وجود ندارد.
سکوت پرستالیست روده ، صدای اصطکاک صفاقی شنیده نمی شود.
معاینه کبد. از نظر بصری ، کبد و کیسه صفرا بزرگ نشده اند ، تپش کبد تشخیص داده نمی شود. لمس: لبه کبد کشسان ، صاف ، تیز ، سطح صاف ، بدون درد است. با نفس عمیق ، 1 سانتی متر از زیر لبه قوس ساحلی در امتداد خط میانی ترقوه خارج می شود. کوفتگی مرز فوقانی تیرگی نسبی در امتداد خط راست استخوان راست - 6 دنده ، در امتداد خط midclavicular راست - 6 دنده ؛ در امتداد خط زیر بغل قدامی - 6 فضای بین دنده ای. مرز پایین در مرز یک سوم بالایی و میانی فاصله از فرایند xiphoid تا ناف است. مرز چپ در امتداد لبه قوس تابستانی سمت چپ فراتر از خط پاراسترنال چپ نیست. ابعاد مطابق Kurlov: 10 * 8 * 9 سانتی متر.
معاینه کیسه صفرا. قابل لمس نیست
معاینه طحال. بزرگ شدن قابل مشاهده طحال وجود ندارد. قابل لمس نیست ضربات تعیین شده:
مرز بالایی در سطح 9 دنده در امتداد خط میانی بغل چپ است.
مرز پایین در سطح 11 دنده است.
قطب خلفی - برتر - در امتداد خط از ستون فقرات تا مرز فوقانی ؛
قطب پیشین پایین - در امتداد خط از ناف تا وسط فاصله بین مرزهای بالا و پایین.
طول طحال 11.5 سانتی متر ؛ قطر 7 سانتی متر
بررسی ناحیه روده هیچ گونه تغییر پاتولوژیک نشان نداد.
سیستم ادراری
معاینه مثانه. مثانه هنگام مشاهده بدون آسیب شناسی.
لمس کردنقابل لمس بدون درد. هیچ دردی در امتداد حالب وجود ندارد. هیچ نشانه ای برای معاینه ویژه دستگاه تناسلی و راست روده وجود ندارد.
معاینه کلیه ها. معاینه ناحیه کمر هیچ ادم یا تورم را نشان نداد.
لمس کردن با لمس عمیق ایستاده و دراز کشیده ، کلیه ها قابل لمس نیستند. هیچ کشش و درد عضلانی وجود ندارد. علائم پاسترناتسکی منفی است.
سیستم خونسازى
رنگ پوست صورتی کم رنگ ، غشاهای مخاطی صورتی است. بدون خونریزی هنگام ضربه زدن روی استخوان جناغ و لوله ، هیچ گونه درد وجود ندارد. وضعیت دستگاه لنفاوی و طحال طبیعی است. هیچ گونه سوفل خونساز و کم خون در قلب و رگهای خونی وجود ندارد.
سیستم غدد درون ریز
شکل ظاهری بیمار با توجه به سن. رشد و اندازه قسمتهای جداگانه بدن طبیعی است. رنگدانه سازی پوست و غشاهای مخاطی بدون آسیب شناسی. رشد مو با الگوی مردانه. صورت بیضی شکل ، رنگ صورتی کم رنگ است. بافت زیرپوستی متوسط \u200b\u200bبیان می شود. هیچ استریایی یافت نشد. بدون ادم معاینه هیچ گونه آسیب شناسی غده تیروئید را نشان نداد. لرزش دست ، پلک و زبان وجود ندارد. علائم Moebius ، Graefe ، Shtelvag منفی است. با لمس ، غده تیروئید بزرگ نشده ، بدون درد است. معاینه ، لمس لوزالمعده بدون آسیب شناسی. افزایش تشنگی ، اشتها ، درد کمربند. غدد فوق کلیوی بدون آسیب شناسی. علائم بیماری آدیسون ، کاهش وزن ، رنگ آمیزی "برنز" پوست ، لکه دار شدن لکه های عمومی ، کاهش فشار خون. هیچ علامت و نشانه ای از بیماری ایتسنکو-کوشینگ وجود ندارد.
سیستم عصبی
هوشیاری بدون تغییر است. هوش ، توجه ، گفتار اختلال ندارد. هنگام لمس درد در تنه های عصبی وجود ندارد. حساسیت حفظ شده است. هماهنگی شکسته نشده است. هیچ فلج و پارسی وجود ندارد. رفلکس ها بدون تغییر هستند. واکنش مردمک ها در برابر نور دوستانه است. علائم مننژال وجود ندارد. اختلالات وازوموتور ، درموگرافی وجود ندارد. تعریق ، ترشح بزاق طبیعی است. اختلالات تروفیک مشاهده نمی شود.
وضعیت روانی
روان بیمار آشفته نیست. روحیه خوب است ، رفتار کافی است ، هیچ افسردگی وجود ندارد. وضعیت حافظه راضی کننده است. شخصیت بیمار آرام است ، انرژی کمی کاهش می یابد ، ذهن حفظ می شود ، دارای طیف وسیعی از علایق است ، نگرش نسبت به خانواده و افراد دیگر خوب است. هیچ ضربه و تعارضی از نظم روانی-عاطفی وجود ندارد. ضربه مغزی ، ضربه مغزی وجود ندارد. خواب طبیعی است. به دلیل بیماری تغییری در شخصیت ، رفاه و روحیه بیمار ایجاد نمی شود.
5. جداسازی سندرم های بیماری با توجه به داده های معاینه بالینی
با توجه به تاریخچه و تحقیقات عینی ، سندرم های زیر را می توان تشخیص داد:
سندرم انسداد انسدادی
سندرم برونشیت
سندرم انسداد انسدادی:
از نظر ذهنی: با اعمال جسمی جزئی ، تنگی نفس دائمی از طبیعت مختلط (جز exp بازدمی) رخ می دهد که در هنگام راه رفتن و شب افزایش می یابد. علاوه بر این ، یک سرفه مولد متناوب که با مقدار کمی خلط خاکستری بدون بو ، سخت قابل جدا شدن است ، تسکین می بخشد.
عینی: بالای قسمتهای جلوی ریه ها - تنفس وزیکولار سفت و سخت. بالای سطح قدامی ریه ها (به خصوص در سمت راست) ، بالا خشک و خس خس سینه کم (بهتر - با بازدم اجباری).
عامل اصلی بیماری زایی در ایجاد انسداد برونش ، عفونت تنفسی است. با شیوع عفونت برونش ، تعداد زیادی سلول چند هسته ای نوتروفیل در لومن نایژه ها جمع می شوند. لکوسیت الاستاز در لومن و بافت اطراف برونش آزاد می شود ، در نتیجه عناصر الاستیک دیواره برونش و بافت ریه اطراف برونش تخریب می شوند. در روند فرآیند های احیا بیشتر ، تغییرات فیبروتیک آنها مشاهده می شود. عوامل موثر در اینجا عفونت های تنفسی مکرر در 2-3 سال گذشته و همچنین سابقه طولانی سیگار کشیدن است. بنابراین ، هوای "درمان نشده" وارد دستگاه تنفسی می شود ، که به هیپوترمی و خشک شدن مخاط برونش کمک می کند. این امر منجر به افزایش بیش از حد ترشح مخاط جبرانی و اختلال در ترشحات مخاط سلولی می شود. با گذشت زمان ، هایپرپلازی غدد مخاطی برونش ایجاد می شود. در نتیجه ایجاد واکنش التهابی در دیواره نایژه ها و آزاد شدن واسطه های التهابی ، نفوذ پذیری رگ های خونی افزایش می یابد و ادم مخاط برونش ایجاد می شود.
کاهش لومن نایژه ها در نهایت منجر به افزایش قابل توجه بار در سیستم تنفسی می شود تا تهویه لازم آلوئول ها را در سطح مناسب حفظ کند. با کاهش فشار جزئی اکسیژن در خون ، تحریک رفلکس مرکز تنفسی رخ می دهد ، که منجر به افزایش سرعت تنفس می شود. و در صورت وجود تغییرات انسدادی در نایژه ها ، بیمار دچار تنگی نفس در بازدم است. باریک شدن لومن نایژه ها و تغییر در تسکین غشای مخاطی آنها ، تنفس صحیح وزیکولار صحیح را توضیح می دهد. در صورت وجود ترشح بسیار چسبناک در لومن نایژه ها ، که محکم در برابر دیواره ها نگه داشته شده است ، صدای خس خس سینه شنیده می شود.
وقوع سرفه در بیمار با تحریک مناطق رفلکسوژنیک مرکز سرفه در حنجره ، نای و برونش ها با ذرات استنشاق توضیح داده می شود. تکانه های حاصل از این گیرنده ها در امتداد n الیاف منتقل می شوند. واگ به نورونهای بازدمی مرکز تنفسی ، جایی که توالی خاصی از مراحل سرفه تشکیل می شود.
وقوع حملات آسم را می توان با برونکوسپاسم در نتیجه افزایش رفلکس در عضلات برونش تحت تأثیر عوامل مختلف (سرفه ، ذرات خارجی ، گازهای تحریک کننده) توضیح داد ، که مستقیماً یا از طریق n عمل می کنند. واگوس (در التهاب مزمن ، در آستانه حساسیت این گیرنده ها کاهش می یابد ، که بیش فعالی برونش ها را در پاسخ به تحریکات جزئی تعیین می کند).
در این بیمار تنگی نفس با اعمال جسمی جزئی ، در حین و بعد از سرفه ظاهر می شود.
سندرم برونشیت: سندرم پیچیده ذهنی - عینی - پاراکلینیکی.
از نظر ذهنی: سرفه تولیدی دوره ای با مقدار کمی خلط خاکستری بدون بو که سخت قابل جدا شدن است. سرفه باعث تسکین می شود.
عینی: بیش از قسمتهای جلوی ریه ها - تنفس مثانه سفت و سخت. بالای سطح قدامی ریه ها (به خصوص در سمت راست) ، خشک زیاد و کم خس خس سینه (بهتر - با بازدم اجباری).
التهاب نایژه ها در این مورد بالینی ، با توجه به علت آن ، می تواند باکتریایی یا ویروسی باشد. در هر صورت افزایش حساسیت هومورال یا سلولی در بدن امکان پذیر است.
در صورت افزایش حساسیت هومورال ، خون حاوی آنتی بادی (AT) به آنتی ژن های باکتریایی (یا ویروسی) مربوطه (AH) است و مجتمع های ایمنی ناشی از آن باعث ایجاد واکنش های زیادی می شوند که باعث ایجاد ورم مخاط برونش و ترشح بیش از حد غدد برونش می شوند. در صورت افزایش حساسیت سلولی ، بافت همبند ریه ها و برونش ها حاوی سلول های حساس به AH خاص است که تماس آنها با AH نیز منجر به آزاد شدن واسطه ها و ایجاد التهاب ایمنی می شود. اگر بدن قادر به کنار آمدن با عفونت نباشد ، فشار خون مداوم باعث یک واکنش موضعی HNT مزمن می شود.
مکانیسم های توسعه تنفس وزیکولار سخت و خس خس سینه خشک در توصیف سندرم انسداد برونش آورده شده است.
این بیمار سرفه مکرر دارد ، کمتر در شب ، با مقدار کمی خلط مخاطی ، بیشتر در صبح. تنگی نفس در هنگام سرفه و بعد از آن اتفاق می افتد.
6. تشخیص اولیه و منطق آن
بیماری اصلی: COPD ، نوع آمفیزماتیک ، سیر شدید (مرحله III) ، تشدید شدت متوسط .
عوارض: آمفیزم ریه ها. پنوموسکلروز
بیماری های همزمان: بیماری فشار خون مرحله 3 با فشار خون شریانی مرحله 2 ، خطر 4. زخم معده و 12 زخم اثنی عشر ، بهبودی. دورسوپاتی ستون فقرات قفسه سینه. حنجره هایپرتروفیک مزمن.
مستقر:
شکایت از سرفه در طول روز ، کمتر در شب ، با مقدار کمی خلط مخاطی ، بیشتر در صبح. تنگی نفس در هنگام سرفه و بعد از آن اتفاق می افتد.
Anamnesis morbi - از سال 2006 ، خود را چندین سال بیمار می داند ، هنگامی که در برابر عفونت های حاد ویروسی تنفسی ، سرفه در طول روز با ترشح خلط مخاطی ، بیشتر در صبح ، تنگی نفس پیشرونده ظاهر می شود. بیمار به پلی کلینیک محل اقامت مراجعه کرد و در آنجا پس از معاینه ، آسم برونش متوسط \u200b\u200bرا تشخیص داد و درمان را تجویز کرد. او از سپتامبر 2013 ، هنگامی که تنگی نفس و سرفه افزایش می یابد ، تحمل ورزش کاهش می یابد ، همراه با افزایش تعداد حملات به روزانه ، وضعیت خود را بدتر می کند. وی تحت معالجه بستری در محل زندگی خود قرار گرفت. با وجود درمان ، وضعیت سلامتی بیمار بهبود نیافت ، سرفه همراه با ترشح خلط مخاطی ، افزایش تنگی نفس ، با توجه به عدم تأثیر درمان ، بیمار برای درمان و بررسی بیشتر در بخش درمانی بستری شد. بنابراین ، برای چندین سال بیمار به دنبال کمک پزشکی نبود ، بیماری به آرامی پیشرفت کرد.
داده های معاینه فیزیکی - کاهش کشش قفسه سینه. لرزش صدا متقارن ، میرایی دو طرفه. با ضرب در نواحی متقارن قفسه سینه ، صدای جعبه ای مشخص می شود. در سمع ، تنفس وزیکولار ضعیف در نواحی متقارن قفسه سینه شنیده می شود. در ریه ها ، رال های خشک با رنگ های مختلف در تمام زمینه های ریوی شنیده می شوند. برونکوفونی بیش از نواحی متقارن قفسه سینه در هر دو طرف ضعیف شده است.
یک دوره متوسط \u200b\u200bبر اساس تشدید مکرر بیماری و بر اساس شکایات تعیین می شود.
تشدید درجه متوسط \u200b\u200bبر اساس شدت تنگی نفس با کمی اعمال جسمی ، خلط زرد-سبز است. افزایش DN - مشارکت در تنفس عضلات کمکی ، حرکت متناقض قفسه سینه ، ظاهر و تشدید سیانوز مرکزی ، تغییر در ترکیب گاز خون.
7. برنامه معاینه اضافی بیمار
I. روشهای تحقیق آزمایشگاهی
1) شمارش کامل خون
2) آزمایش خون بیوشیمیایی (اوره ، بیلی روبین ، کلسترول ، ALT ، AST ، کراتینین ، گلوکز)
3) آنالیز عمومی ادرار
4) خون بر روی RW ، HIV
دوم روشهای تحقیق ابزاری
1 ) اشعه ایکس قفسه سینه.
2 ) نوار قلب
8. نتایج تحقیق اضافی
اشعه ایکس. الگوی ریوی در قسمت پایین سمت راست افزایش و تغییر شکل داده است که نفوذ را از بین نمی برد.
نتیجه گیری: ذات الریه در قسمت تحتانی ریه راست مستثنی نیست.
نوار قلب ریتم سینوسی. ضربان قلب 60 ضربان در دقیقه. محاصره ناقص بلوک شاخه بسته نرم افزاری راست.
آنالیز عمومی خون.
هموگلوبین 139 گرم در لیتر
گلبول قرمز 4.39x10№І / l
شاخص رنگ 0.95
ESR 9 میلی متر در ساعت
پلاکت 195x10 / l
لکوسیت ها 8.1x10 / l
رتیکولوسیتها 5.5٪
نتیجه گیری: در تجزیه و تحلیل کلی خون ، تغییرات پاتولوژیک مشاهده نمی شود.
آزمایش خون بیوشیمیایی.
اوره 9.21 mmol / l
بیلی روبین 7.1 میلی مول در لیتر
کلسترول 4.72 میلی مول در لیتر
ALT 0.18 میکرومول در لیتر
AST 0.24 میکرومول در لیتر
کراتینین 98 میلی مول در لیتر
گلوکز 4.0 میلی مول در لیتر
نتیجه گیری: تجزیه و تحلیل بیوشیمیایی طبیعی است.
آنالیز عمومی ادرار.
مقدار: 10 میلی لیتر
رنگ: زرد نی
شفافیت: کامل
واکنش: اسیدی
پروتئین: منفی
لکوسیت ها: 2-3 سلول. بینش، بصیرت، درون بینی
گلبول های قرمز: تازه است. 0-1 ، اصلاح شده 10-12
سلولهای اپیتلیال: 0-1 سلول بینش، بصیرت، درون بینی
9. توجیه نهایی گناهپتومتحرک
با در نظر گرفتن آزمایشات آزمایشگاهی انجام شده ، وجود سندرم می تواند تأیید شود. یک سندرم نفوذی نیز مشخص شد که منجر به سندرم برونشیت می شود ، که به نوبه خود منجر به انسداد برونش می شود.
10. تشخیص های افتراقی
در مراحل اولیه COPD ، باید بین COP و AD تمایز قائل شد ، زیرا در این زمان ، رویکردهای کاملاً متفاوتی برای درمان هر یک از این بیماری ها مورد نیاز است. تشخیص افتراقی BA و COB دشوارترین است. معاینه بالینی علائم پاروکسیسم را در BA نشان می دهد ، اغلب در ترکیب با علائم خارج ریوی آلرژی (رینیت ، ملتحمه ، تظاهرات پوستی ، آلرژی غذایی). بیماران مبتلا به COB با علائم ثابت و کم تغییر مشخص می شوند. یکی از عناصر مهم تشخیص افتراقی کاهش FEV 1 به میزان 50 میلی لیتر یا بیشتر در سال در بیماران مبتلا به COB است که در BA مشاهده نمی شود. COB با تغییر روزانه کم پارامترهای حداکثر جریان سنجی مشخص می شود (< 15%). При БА разность между утренними и вечерними показателями пикфлоуметрии увеличивается и превышает 20%. При БА чаще наблюдается бронхиальная гиперреактивность. Из лабораторных признаков при БА чаще встречается увеличение содержания IgE.
هنگامی که یک م componentلفه برگشت ناپذیر انسداد برونش در بیماران BA ظاهر می شود ، تشخیص افتراقی بین این بیماری ها معنی خود را از دست می دهد ، زیرا ما می توانیم افزودن بیماری دوم - COP و نزدیک شدن به مرحله نهایی بیماری - COPD را بیان کنیم.
معیارهای اصلی تشخیص افتراقی برای COPD و BA.
|
علائم |
||||
|
1. آلرژی |
معمولی نیست |
مشخصه |
||
|
ثابت ، با شدت متفاوت |
پاروکسیسم |
|||
|
ثابت ، بدون نوسانات شدید شدت |
حملات تنگی نفس بازدم |
|||
|
4. تغییرات روزانه در FEV1 |
کمتر از 10٪ از بدهی |
بیش از 15٪ از بدهی |
||
|
5. انسداد برونش |
برگشت پذیری غیر معمول ، وخیم تدریجی در عملکرد ریه است |
برگشت پذیری مشخصه ، هیچ وخیم ترقی در عملکرد ریه وجود ندارد |
||
|
6. ائوزینوفیلی خون و خلط |
شاید ، اما مربوط به آسیب شناسی اساسی نیست |
مشخصه |
بیایید به فرمولاسیون هایی که ماهیت این بیماری ها را تعریف می کنند ، بپردازیم.
BA یک التهاب مزمن در مجاری تنفسی با مشارکت غالب ماست سل ها ، ائوزینوفیل ها و لنفوسیت های T است که با حملات مکرر خس خس سینه ، تنگی نفس ، فشردن قفسه سینه و سرفه ظاهر می شود ، که عمدتا در شب یا صبح زود اتفاق می افتد. این علائم معمولاً با انسداد گسترده و متغیر برونش همراه است که به صورت خود به خودی یا در نتیجه درمان برگشت پذیر است (حداقل تا حدی).
COPD یک بیماری التهابی مزمن سیستم تنفسی با واسطه زیست محیطی با ضایعه غالب دستگاه تنفسی محیطی و پارانشیم ریوی با توسعه آمفیزم است که با انسداد برونش تا حدودی برگشت پذیر ظاهر می شود و با پیشرفت و افزایش پدیده های نارسایی مزمن تنفسی ناشی از استنشاق ذرات یا گازها مشخص می شود.
در این بیماری ها متداول روند التهابی مزمن است که تصویر بالینی بیماری و همچنین روش های تشخیص و درمان را تعیین می کند. و اگر در BA روند التهابی آلرژیک باشد و عمدتاً در مجاری هوایی موضعی باشد ، در COPD یک تصویر کاملاً متفاوت مشاهده می شود.
اول از همه ، ماهیت التهاب مزمن در COPD هنوز به طور کامل شناخته نشده است. واضح است که این التهاب آلرژیک نیست. در عین حال ، به دلیل پیشرفت مداوم و واسطه گری محیطی ، ارجاع آن به دسته فرآیندهای التهابی مزمن معمولی غیرممکن است.
بین COPD و محل التهاب تمایز قائل می شود. همانطور که در AD وجود دارد ، التهاب در COPD عمدتا در مجاری هوایی محیطی موضعی است ، اما بر خلاف AD ، به این محدود نمی شود ، بلکه به بافت بینابینی و پارانشیم ریه گسترش می یابد و منجر به تخریب دیواره آلوئول و توسعه آمفیزم ریوی می شود. این سازوکار است که در تشکیل یک جز component برگشت ناپذیر انسداد برونش اساسی است. بنابراین ، این بیماری "بیماری انسدادی مزمن ریوی" نامیده می شود ، که شامل شکست تمام اجزای ریه ها ، و نه فقط مجاری تنفسی است.
یکی دیگر از ویژگی های متمایز COPD ماهیت پیشرونده بیماری است که برای AD کلاسیک معمول نیست.
سرانجام ، تظاهرات بالینی. BA با تورم و برگشت پذیری علائم تنفسی مشخص می شود. در COPD ، تنگی نفس آهسته اما مداوم ایجاد می شود ، که توسط ضعف برونش معمولی کنترل ضعیفی دارد.
تشخیص افتراقی BA و COPD براساس ادغام داده های کلینیک اساسی ، نتایج آزمایشات عملکردی و آزمایشگاهی است. در حال حاضر هیچ نشانگر آزمایشگاهی وجود ندارد که بتواند به طور قابل اعتماد این دو بیماری را از یکدیگر متمایز کند. تأکید اصلی در تشخیص افتراقی بر ایجاد علائم اصلی است که ماهیت بیماری را تعیین می کند: در AD ، این تورم و برگشت پذیری علائم است و در COPD ، پیشرفت مداوم و عدم برگشت پذیری است.
بیماران BA با یک لیست کلاسیک از عوامل خطر مشخص می شوند - آلرژن ها که باعث پیشرفت بیماری می شوند. اینها آلرژن های خانگی ، گرده گیاهان ، برخی از عوامل تولید و غیره هستند. لیست عوامل علی احتمالی طولانی است و در رهنمودهای ویژه BA شرح داده شده است. در مورد COPD ، سیگار عامل اصلی خطر است (تا 90٪). در سالهای اخیر ، اطلاعات در مورد تأثیر محصولات احتراق انواع خاصی از سوخت خانگی ، آلودگی صنعتی و برخی از عوامل تولید (سیلیکون ، کادمیوم) ظاهر شده است.
اکثر بیماران BA استعدادی ارثی دارند که در بیماران COPD مشاهده نمی شود. AD می تواند در هر دوره از زندگی آغاز شود و COPD بیماری نیمه دوم زندگی است و برای تشخیص COPD در سنین جوانی بحث های بسیار جدی لازم است. این امر تا حدی به دلیل اثر تجمعی عامل خطر در طی سالهای متمادی است.
مهمترین م componentلفه تشخیص ، تجزیه و تحلیل تظاهرات بالینی است. در اینجا تفاوتهای کاملاً مشخص و اساسی نمایان می شود.
AD با یک علامت شناسی موج مانند ، روشنایی تظاهرات بالینی و برگشت پذیری آنها (خود به خودی یا تحت تأثیر درمان) مشخص می شود. شدت وضعیت یک بیمار BA با توجه به طول مدت بیماری تعیین نمی شود و ممکن است در ابتدای بیماری حداکثر باشد و سپس با درمان کافی ، علائم اصلی بیماری به طور کامل از بین می روند. با ابتلا به COPD ، بیماری به تدریج خزش می کند ، به شرط آنکه عامل خطر طولانی مدت باشد. اولین علائم توسط بیمار معمولاً در مرحله دوم بیماری مشاهده می شود.
برخي تفاوتها در وضعيت اجتماعي بيماران متوسط \u200b\u200bBA و COPD بايد تاكيد شود. اگر یک بیمار BA می تواند به هر طبقه از جمعیت تعلق داشته باشد ، COPD اغلب در بیمارانی با سطح اقتصادی-اجتماعی پایین ایجاد می شود. این امر تا حد زیادی واکنش بیماران را نسبت به علائم اولیه بیماری تعیین می کند. بیماران مبتلا به آسم افراد قابل تأملی هستند و هر علامت ناچیزی از بیماری ، چه "قلقلک" پشت استخوان سینه ، تنفس سرفه در شب یا حمله خفگی طولانی مدت ، بیمار قطعاً چشم پوشی نمی کند و به دنبال کمک پزشکی است. یک بیمار مبتلا به COPD ، نشانه اولیه بیماری - سرفه صبح - معمولاً به حالت طبیعی فرد سیگاری اشاره دارد و هیچ اقدامی انجام نمی دهد ، اما فقط در صورت ایجاد تنگی نفس در مورد وضعیت سلامتی وی فکر می کند (این اتفاق معمولاً 8-10 سال پس از اولین نشانه بیماری - سرفه) می افتد ... بنابراین ، پیش نیازهایی برای تشخیص دیررس COPD وجود دارد.
در طبقه بندی AD و COPD نیز از اصول مختلفی استفاده شده است. در BA ، طبقه بندی شدت بر اساس شدت علائم بالینی است و در COPD ، پارامتر عملکردی اساس است - درجه کاهش و ارتباط آن با FVC. بنابراین ، در BA ، علائم عملکردی نقص حفره برونش عواملی هستند که تشخیص را تکمیل می کنند و در COPD ، آنها برای تعیین شدت (مرحله) بیماری اساسی هستند ، که این امر ماهیت ثانویه تظاهرات بالینی را با نقش اصلی شاخص های FVD نشان می دهد.
علیرغم شباهت ظاهری تظاهرات بالینی BA و COPD ، تقریباً در همه علائم اصلی تفاوت وجود دارد که تشخیص در این دو فرم بیمارشناسی را حتی در مرحله یک معاینه بدنی ساده امکان پذیر می کند.
تغییرات در FVD همچنین تفاوت اصلی بین این بیماری ها را برجسته می کند - شکل موج علائم ، که مشخصه AD است و در COPD وجود ندارد. علاوه بر این ، تغییرات عملکردی در COPD پیشرونده و ناتوان کننده است.
کمترین تفاوت بارز در تجزیه و تحلیل پارامترهای آزمایشگاهی بیماران مبتلا به BA و COPD مشاهده می شود. ائوزینوفیلی و افزایش سطح IgE سرم که قبلاً از علائم قابل اعتماد AD قلمداد می شدند ، در COPD نیز مشاهده می شود که می تواند منجر به خطاهای تشخیصی شود.
بنابراین ، تشخیص افتراقی بین BA و COPD باید با جمع بندی داده های مطالعات بالینی ، عملکردی و آزمایشگاهی انجام شود. جمعیت ویژه ای (و بسیار قابل توجه) را بیمارانی تشکیل می دهند که BA و COPD دارند. در چنین مواردی ، معنای تشخیص افتراقی از بین می رود و هر دو بیماری تشخیص داده می شوند. در این بیماران ، در واقع ، جمع بندی علائم هر دو بیماری وجود دارد. بنابراین ، در حال حاضر ، معیارهای کاملاً ساده و قابل اعتمادی برای تشخیص افتراقی BA و COPD ایجاد شده است ، که اجازه می دهد از تعداد زیادی از خطاهای استاندارد جلوگیری شود.
COPD و سایر بیماری ها
در مراحل خاصی از توسعه COPD ، به ویژه با یک جلسه ملاقات (اول) با یک بیمار ، ممکن است لازم باشد COPD از تعدادی از بیماری ها با علائم مشابه (خارجی) متمایز شود.
COPD و سل ریوی
با تشخیص افتراقی سل ریوی و COPD مکان ویژه ای اشغال شده است. بیماری سل
پیوستن به سل ریه ها در شکست درخت برونش و انسداد برونش به طور قابل توجهی روند بیماری را تشدید می کند. سندرم انسداد انسدادی برونکو (BOS) در انواع اشکال سل ریوی رخ می دهد ، فراوانی تشخیص آن به مدت زمان یک فرایند خاص و شدت تغییرات پسماند در ریه ها بستگی دارد. با سل کانونی ، انسداد برونش در 52.7٪ ، با سل نفوذی - در 56.6، ، با رشته- غار- در 76.9، ، با انتشار - در 88.2 occurs رخ می دهد. شیوع بازخورد زیستی در بین افراد مبتلا به تغییرات پس از سل در ریه ها از 59.5 تا 83.9 ranges - 2-3 برابر بیشتر از بقیه افراد است. BFB یکی از دلایل اصلی ناتوانی موقتی ، ناتوانی و مرگ زودرس این بیماران است.
3 شکل از ترکیب بیوفیدبک با سل ریوی وجود دارد:
1. Paratuberculous (قبل از سل ریوی) به دلیل برونشیت انسدادی مزمن (COP) یا بیماری انسدادی مزمن ریوی (COPD).
2. بازخورد زیستی متاتوبرکلوز ، که در طی سل ریوی طولانی مدت اتفاق می افتد.
3. بیوفیدبک پس از سل ، که پس از درمان سل فعال در برابر پس زمینه تغییرات پس از سل در ریه ها ایجاد می شود.
بنابراین ، در بیماران مبتلا به سل ریوی ، حداقل دلایل زیر انسداد برونش امکان پذیر است: تظاهرات COPD ، تظاهرات COB ، تظاهرات برونشیت سل ، انسداد برونش ثانویه بدون تغییرات مورفولوژیکی قابل توجهی در برونش ها. به دلیل عدم اطمینان اصطلاحی که در سالهای اخیر وجود داشته است ، هیچ اطلاعات دقیق اپیدمیولوژیکی در مورد ترکیب COPD با سل ریوی وجود ندارد. با این وجود ، وجود علائم واضح سل ریوی (مسمومیت ، داده های اشعه ایکس ، آزمایش سل مثبت ، جداسازی مایکوباکتری ها) در حضور بازخورد زیستی ، قبل از هر چیز مستلزم آسیب خاص (سل) مجاری تنفسی است. انجام این کار در هنگام انجام معاینه برونشولوژی آسان است.
برای ایجاد تعلق بیوفیدبک به COPD در بیماران مبتلا به سل ریوی ، لازم است وجود معیارهای اصلی COPD در بیمار مشخص شود:
التهاب مزمن ناشی از عوامل محیطی (سیگار کشیدن ، ذرات تحریک کننده و گازها) ؛
آسیب به مجاری هوایی و پارانشیم ریه با تشکیل آمفیزم ؛
انسداد پیشرونده برونش.
اگر بتواند دو وضعیت اول در معاینه اولیه بیمار ایجاد شود ، با مشاهده طولانی مدت (طی یک سال) می توان پیشرفت را به وضوح تأیید کرد.
11. تشخیص نهایی
بر اساس روشهای تحقیقاتی آزمایشگاهی و ابزاری اضافی ، تشخیص اولیه تأیید می شود.
تشخیص اصلی: COPD ، نوع آمفیزماتیک ، سیر شدید (مرحله III) ، تشدید شدت متوسط.
عوارض: آمفیزم ریه ها. پنوموسکلروز
بیماری های همزمان: بیماری فشار خون ، مرحله 3 همراه با فشار خون شریانی ، درجه 2 ، خطر 4. زخم معده و زخم اثنی عشر ، بهبودی. دورسوپاتی ستون فقرات قفسه سینه. حنجره هایپرتروفیک مزمن.
12. علت شناسی و پاتوژنز
عوامل خطر:
1. قرار گرفتن طولانی مدت در معرض مواد موجود در هوا: (گرد و غبار ؛ آلاینده های شیمیایی - بخار اسیدها ، مواد قلیایی ؛ آلاینده های صنعتی - SO2 ، NO2 ، دود سیاه.)
2. عوامل محیطی - آلودگی هوا در جو و محل (دود سیاه - SO2 ، دود حاصل از پخت و پز و سوخت های فسیلی و غیره). تماس با خطرات شغلی - کادمیوم ، سیلیکون ، که به ویژه مضر هستند. افزایش آسیب در افراد از مشاغل زیر: معدن کاران ، کارگران ساختمانی در تماس با سیمان ، کارگران در تماس با فلز گرم کار ، پنبه کاران ، کارگران راه آهن و غیره. تقریباً همیشه ادغام عوامل خارجی با عوامل داخلی وجود دارد - یک زمینه مستعد ژنتیکی.
3. استعداد ارثی (کمبود مهارکننده های نوتروفیل الاستاز - آلفا -1-آنتی تریپسین ، آلفا -1-آنتی سایمو تریپسین ، آلفا-2-ماکروگلوبولین.). سهم این علت در بروز COPD بسیار کمتر از مصرف سیگار است. کمبود آلفا-1-آنتی تریپسین منجر به آمفیزم ، COPD و برونشکتازی می شود.
4. بیماری های التهابی مکرر سیستم تنفسی در اوایل کودکی ، وزن کم هنگام تولد. نقطه نظرات مختلفی در مورد اهمیت اتیولوژیکی میکروارگانیسم ها در COPD وجود دارد ، اما درگیری عفونت در مکانیسم توسعه COPD و بروز تشدیدات غیرقابل انکار است. عوامل اصلی استعمار باکتریها (ته نشین شدن) چسبندگی باکتریها ، تضعیف دفاع مخاط-سیلیاری ، آسیب به یکپارچگی اپیتلیوم و نقض ایمنی موضعی و سیستمیک است. عوامل عفونی نه از طریق فعال شدن سلولهای اصلی مهاجم: از نوتروفیل ها ، ماکروفاژها ، لنفوسیت ها و غیره ، از التهاب در COPD پشتیبانی می کنند.
بیماری زایی
نتیجه اصلی تأثیر عوامل اتیولوژیکی ، ایجاد التهاب مزمن است. محلی سازی التهاب و ویژگی های عوامل محرک ، ویژگی فرآیند آسیب شناختی در COPD را تعیین می کند. اثربخشی حمل و نقل مخاطی - مهمترین م componentلفه عملکرد طبیعی راههای هوایی - به هماهنگی عملکرد دستگاه مژه ای اپیتلیوم مژه دار و همچنین ویژگیهای کمی و کیفی ترشحات برونش بستگی دارد. تحت تأثیر عوامل خطر ، حرکت مژک ها مختل می شود تا زمانی که کاملاً متوقف شود ، متاپلازی اپیتلیوم با از بین رفتن سلولهای اپیتلیال مژگانی و افزایش تعداد سلولهای جام ایجاد می شود. ترکیب ترشح برونش تغییر می کند ، که باعث مختل شدن حرکت مژک های نازک قابل توجه می شود. این به وقوع مخاط کمک می کند ، که باعث انسداد مجاری تنفسی کوچک می شود. عوامل اتیولوژیکی محیط خارجی نه تنها منجر به اختلال در حمل و نقل مخاطی در برونش ها می شود ، بلکه به موازات این شکل استرس اکسیداتیو وجود دارد که با تشکیل تعداد زیادی رادیکال آزاد در مجاری هوایی آشکار می شود. منبع اصلی رادیکال های آزاد نوتروفیل های خون در گردش هستند که تحت تأثیر عوامل محرک به تعداد زیادی در ریه ها متمرکز شده اند. در شرایط غلظت بالای نوتروفیل ها ، تعادل سیستم پروتئاز - آنتی پروتئاز بهم می خورد. همراه با نوتروفیل ها ، ماکروفاژها و لنفوسیت های T در تشکیل و اجرای التهاب شرکت می کنند. نشانگر زیستی یک فرآیند التهابی مزمن ، مشارکت نوتروفیل ها با افزایش فعالیت میلوپراکسیداز ، نوتروفیل الاستاز ، ظهور متالوپروتئازها ، عدم تعادل در سیستم های پروتئولیز - آنتی اکسیدان و آنتی اکسیدان است. مجموعه بزرگی از واسطه های پیش التهابی که از سلولهای نفوذی در غشای مخاطی رها می شوند ، در مویرگ های ریوی و بافت اطراف برونش جمع می شوند و تا حدود زیادی کل تغییرات پاتولوژیک را تعیین می کنند. واسطه های اصلی التهاب در COPD اینترلوکین ها ، فاکتور نکروز تومور ، میلوپراکسیدازها ، الاستازهای نوتروفیل ، متالوپروتئازها هستند و اخیراً نقش دفنسین ها توصیف شده است. تغییر در خصوصیات ویسکوالاستیک ترشح برونش با تغییرات کیفی قابل توجهی در ترکیب آن همراه است: محتوای اجزای غیر اختصاصی ایمنی محلی ، که دارای فعالیت ضد ویروسی و ضد میکروبی هستند ، کاهش می یابد: اینترفرون ، لاکتوفرین و لیزوزیم. همراه با این ، محتوای IgA ترشحی کاهش می یابد. بی نظمی در ترخیص کالا از گمرک مخاطی و پدیده نقص ایمنی موضعی شرایط بهینه را برای استعمار میکروارگانیسم ها ایجاد می کند. مخاط برونش ضخیم و چسبناک با کاهش پتانسیل ضد باکتری زمینه مناسبی برای تولید میکروارگانیسم های مختلف (ویروس ها ، باکتری ها ، قارچ ها) است. تحت شرایط خاص ، این بیماران با عفونت تنفسی فعال می شوند. این ممکن است به دلیل فعال شدن مجدد اتوفلورا یا فوق عفونت با میکروارگانیسم های پنوموتروپیک باشد ، که بیماران COPD بسیار حساس به آن هستند. این مجموعه کامل از مکانیسم های التهاب منجر به تشکیل دو فرآیند اصلی مشخصه COPD می شود - اختلال در حفره برونش و ایجاد آمفیزم مرکز لوب. یک پیوند اساسی در پاتوژنز اختلال حفره برونش ، فعال سازی مکانیسم های کولینرژیک سیستم عصبی خودمختار است که منجر به افزایش واکنش های برونکوسپاستیک می شود. صدای عصب واگ در بیماران مبتلا به COPD در مراحل اولیه بیماری به دلیل تحریک گیرنده های تحریک کننده اپیتلیوم برونش افزایش می یابد. اثر تحریک کننده بر روی گیرنده ها با اثرات دود تنباکو ، گازهای سمی (ازن ، دی اکسید نیتروژن ، گوگرد و غیره) اعمال می شود. شکست اپیتلیوم پیوند اولیه التهاب است.
نقض قابلیت بازرسی برونش در بیماران مبتلا به COPD به دلیل اجزای برگشت پذیر و غیر قابل برگشت ایجاد می شود. وجود و شدت یک م componentلفه برگشت پذیر ، بیماری را که COPD را تشکیل می دهند ، فردیت می بخشد و به آنها اجازه می دهد تا به شکل های جداگانه بینی تشخیص دهند. جز component برگشت پذیر از اسپاسم عضلات صاف ، ادم مخاط برونش و ترشح بیش از حد مخاط ایجاد می شود ، که تحت تأثیر افزایش صدای عصب واگ و آزاد شدن طیف وسیعی از واسطه های پیش التهابی (اینترلوکین -8 ، فاکتور نکروز تومور ، پروتئازهای نوتروفیل و رادیکال های آزاد) ایجاد می شود. در روند پیشرفت بیماری ، جز component برگشت پذیر به تدریج از بین می رود. با از دست دادن کامل ، بیماری کیفیت خود را تغییر می دهد ، و مرزهای فرم های بینی که COPD را تشکیل می دهند پاک می شود. یک جز component برگشت ناپذیر انسداد برونش با ایجاد آمفیزم و فیبروز دور برونش تعیین می شود. آمفیزم عمدتا در نتیجه کاهش (به دلیل استرس اکسیداتیو) از مهارکننده های پروتئاز محلی و تحت تأثیر پروتئازهای نوتروفیل ایجاد می شود ، که استرومای الاستیک آلوئول ها را از بین می برد. به دلیل نقض خواص الاستیک ریه ها ، مکانیک تنفس تغییر می کند و فروپاشی بازدم ایجاد می شود ، که مهمترین علت انسداد برونش برگشت ناپذیر است. فیبروز پری برونش - نتیجه التهاب مزمن ، بر تشکیل یک جز ir غیرقابل برگشت کمتر از آمفیزم تأثیر می گذارد. توسعه آمفیزم منجر به کاهش عروق در مناطقی از بافت ریه می شود که توانایی تبادل گاز ندارند. در نتیجه ، جریان خون در نواحی باقیمانده بافت ریه توزیع می شود و اختلالات برجسته تهویه-پرفیوژن رخ می دهد. ناهمواری روابط تهویه و پرفیوژن یکی از عناصر مهم پاتوژنز COPD است. پرفیوژن در مناطق با تهویه ضعیف منجر به کاهش اکسیژناسیون شریانی می شود ، تهویه بیش از حد در مناطق کم تزریق منجر به افزایش تهویه فضای مرده و تأخیر در آزاد شدن CO2 می شود. همه اینها شرایط را برای افزایش فشار در حوضچه شریان ریوی ایجاد می کند. در این مرحله ، فشار خون ریوی با تکامل بیشتر Cor pulmonale شکل می گیرد. هیپوکسی مزمن منجر به اریتروسیتوز جبرانی - پلی سیتمی ثانویه با افزایش مربوطه در ویسکوزیته خون و اختلالات میکروسیرکولاسیون می شود ، که عدم تعادل تهویه-پرفیوژن را تشدید می کند.
انسداد برونش را تشدید می کند و منجر به افزایش تمام علائم بیماری ، تشدید روند عفونی در سیستم تنفسی می شود. تحت شرایط مخاط ، نقص ایمنی موضعی و بعضاً سیستمیک ، استعمار میکروارگانیسم ها می تواند ماهیتی غیرقابل کنترل داشته باشد و به یک شکل متفاوت از نظر کیفی با یک کلان ارگانیسم - یک روند عفونی - تغییر کند. راه دیگری نیز ممکن است - عفونت معمول توسط قطرات موجود در هوا با فلور بسیار بدخیم ، که در شرایط مکانیسم های محافظتی آشفته به راحتی قابل درک است.
13. ویژگی های بالینی سیر بیماری
ویژگی های بالینی: جنسیت (مرد) ، سن (60 سال) ، سیگار کشیدن.
14. رفتار
برای جلوگیری از تشدید توسعه ، از گشاد کننده های برونش (آگونیست های B2 ، آنتی کولینرژیک ها ، متیل گزانتین ها) ، گلوکوکورتیکوئیدها ، آنتی بیوتیک ها ، اکسیژن درمانی کنترل شده ، تهویه غیرتهاجمی ریه ها و ... استفاده می شود.
گشادکننده برونش
یکی از اصول اصلی درمان تشدید COPD ، تشدید درمان با گشادکننده برونش است. تقویت درمان گشادکننده برونش با افزایش دوزها و اصلاح روشهای تحویل دارو حاصل می شود. در حال حاضر ، اثر β آگونیست های کوتاه اثر (سالبوتامول ، فنوترول) و IB در بیماران مبتلا به تشدید COPD اثبات شده است. گشادکننده برونش برای ترشحات حاد COPD آگونیست های β2 اثر کوتاه مدت هستند.
به عنوان یک درمان برش دهنده برونش برای تشدید COPD شدید ، توصیه می شود که محلولهای نبولایزاسیون β2-آگونیستهای کوتاه اثر را تجویز کنید ، به عنوان مثال ، ونتولین 2.5-5 میلی گرم در هر استنشاق. هنگام درمان بیماران شدید بیمار با آسیب شناسی اندام های متعدد ، تاکی کاردی ، هیپوکسمی ، نقش داروهای ACP افزایش می یابد. IB هم بصورت مونوتراپی و هم در ترکیب با آگونیست β2 (محلول زودرس) تجویز می شود.
داروهای گلوکوکورتیکواستروئید
به طور کلی پذیرفته شده است که با تشدید COPD ، همراه با کاهش FEV1 کمتر از 50 of از مقادیر مناسب ، گلوکوکورتیکواستروئیدها به موازات درمان گشادکننده برونش تجویز می شوند. درمان با گلوکوکورتیکواستروئیدهای سیستمیک (خوراکی یا تزریقی) باعث افزایش سریعتر FEV1 ، کاهش تنگی نفس ، بهبود اکسیژناسیون خون شریانی و بستری کوتاه تر در بیمارستان می شود. , و همچنین کاهش تعداد عوارض از جمله مرگ به هر علتی ، نیاز به لوله گذاری ، مراقبت های ویژه مکرر و ... کورتیکواستروئیدها باید در اسرع وقت ، حتی با پذیرش در بخش اورژانس تجویز شوند. تجویز گلوکوکورتیکوئیدها به صورت خوراکی یا داخل وریدی برای تشدید COPD در مرحله بیمارستان به موازات درمان با گشادکننده برونش انجام می شود (در صورت وجود در ترکیب با آنتی بیوتیک و اکسیژن درمانی). با توجه به خطر جدی ایجاد عوارض جانبی با استروئید درمانی با دوز بالا ، 30-40 میلی گرم پردنیزون باید برای 10-14 روز تجویز شود . ادامه درمان به افزایش کارایی منجر نمی شود و همزمان خطر ابتلا به عوارض جانبی را افزایش می دهد.
عوامل ضد باکتری
نشانه های آنتی بیوتیک درمانی در بیماران مبتلا به تشدید COPD افزایش تنگی نفس ، افزایش حجم خلط و شخصیت چرکی است. . با در نظر گرفتن ناهمگنی بیمارانی که تحت تشدید COPD قرار دارند ، توصیه می شود گروههای جداگانه ای از بیماران را از هم جدا کنید ، برای هر یک از آنها می توان لیستی از پاتوژنهای احتمالی و شیوع سویههای مقاوم به آنتی بیوتیک را پیش بینی کرد.
آنتی بیوتیک درمانی برای تشدید COPD
|
تعریف |
عوامل بیماری زای اصلی |
ضد باکتری درمانی |
||
|
داروهای انتخابی |
داروهای جایگزین |
|||
|
تشدید ساده (بدون عارضه) COPD |
||||
|
افزایش تنگی نفس ، افزایش حجم و خلط چرکی |
H.influenzae H.parainfluenzae S.pneumoniae M.catarrhalis مقاومت احتمالی در برابر β-lactams |
آموکسی سیلین |
فلوئوروکینولونهای تنفسی (لووفلوکساسین) یا ماکرولیدهای "جدید" (آزیترومایسین ، کلاریترومایسین) ، سفوروکسیم آکستیل (zinnat). |
|
|
تشدید پیچیده COPD |
||||
|
افزایش تنگی نفس ، افزایش حجم و چرک خلط. تشدیدهای مکرر\u003e 4 در سال سن\u003e 65 سال |
H.influenzae H.parainfluenzae S.pneumoniae M.catarrhalis مقاومت احتمالی در برابر β-lactams |
آموکسی سیلین + کلاولانات (اوگمنتین ، آموکسی کلاو) ، فلوئوروکینولونهای تنفسی (لووفلوکساسین) یا سفالوسپیرینهای 2-3 نسل (سفوروکسیم axetil یا zinnat ، claforan و غیره) |
گروه اول (تشدید بدون عارضه COPD) شامل بیماران زیر 65 سال با تشدید نادر بیماری (کمتر از 4 سال در سال) ، عدم وجود بیماری های جدی همزمان و اختلالات جزئی یا متوسط \u200b\u200bباز بودن برونش (50٪ FEV1) است. برای این دسته از بیماران ، عوامل احتمالی تشدید H. influenzae ، H. parainfluenzae ، S. pneumoniae و M. catarrhalis با سطح طبیعی حساسیت به آنتی بیوتیک ها هستند.
...اسناد مشابه
شکایات اصلی بیمار هنگام پذیرش. تاریخچه توسعه بیماری انسدادی مزمن ریوی (COPD). تجزیه و تحلیل زندگی بیمار ، وضعیت فعلی او. منطق تشخیص: نوع آمفیزماتیک COPD ، مرحله تشدید. تجویز درمان برای بیمار.
تاریخچه پرونده ، اضافه شده در 19/12/2014
مفهوم و مشخصات عمومی نارسایی قلبی ، دلایل اصلی و پیش نیازهای ابتلا به این بیماری است. تصویر و علائم بالینی ، علل و پاتوژنز ، اصول تشخیص. رویکردهای رژیم درمانی ، پیشگیری.
تاریخچه مورد ، اضافه شده در 12/23/2014
مفهوم و علل اصلی بیماری انسدادی مزمن ریوی ، علائم بالینی و مراحل رشد ، علائم. روش های تشخیص این بیماری ، اصول و تهیه یک طرح برای درمان ، پیشگیری و پیش آگهی آن.
تاریخچه مورد ، اضافه شده در 11/26/2013
خصوصیات عمومی و علل ایجاد بیماری سنگ صفرا ، تصویر بالینی و علائم آن ، علت شناسی و پاتوژنز. یک طرح معاینه برای تشخیص افتراقی ، انجام مراحل و آزمایشات لازم. تهیه یک رژیم درمانی.
تاریخچه مورد ، اضافه شده در 2014/05/23
برونشیت انسدادی مزمن ، آمفیزم ریوی ، اشکال شدید آسم برونش. عوامل خطر عمده طبقه بندی بیماری انسدادی مزمن ریوی (COPD) بر اساس شدت آن. اصلی ترین مشخصات بالینی و مراحل دوره انواع COPD.
ارائه در تاریخ 10/04/2015 اضافه شده است
ابتکار جهانی بیماری انسداد مزمن ریوی (COPD) موسسه ملی قلب ، ریه و خون ایالات متحده. تدوین و تصویب استراتژی جهانی کنترل COPD. تصویر بالینی بیماری ، فنوتیپ ها و عوامل خطر آن.
ارائه اضافه شد 2015/02/22
آزمایشات عملکرد ریوی ، تشخیص افتراقی بیماری انسداد مزمن: علائم ، تصویر بالینی ، نتایج. پاتوژنز COPD ، در مقابل آسم برونش: طبیعت تنفس خارجی و تنگی نفس. عوامل توسعه ، اقدامات پیشگیرانه.
ارائه در 11/12/2013 اضافه شد
ویژگی های عمومی ، علل اصلی ظاهر و عوامل توسعه سرطان پستان. تصویر بالینی و علائم این بیماری ، مراحل و بازه های زمانی پیشرفت آن. اصول تشخیص ، رژیم درمانی ، پیش آگهی زندگی.
تاریخچه پرونده ، اضافه شده 06/03/2014
عوامل و عوامل خطر برای انسداد مزمن ریوی (COPD). پاتوژنز و اشکال دوره COPD ، مشخصات بالینی ، مراحل دوره ، تشخیص و درمان. داروهای ضد باکتری برای تشدیدها و گشاد کننده های برونش تنفسی.
ارائه در تاریخ 10/04/2015 اضافه شده است
تشخیص بیماری: بیماری انسدادی مزمن ریوی ، نوع آمفیزماتیک ، تشدید شدت متوسط. معاینه بیمار: انجام آنالیزهای بالینی ، نتیجه گیری ، شناسایی تشخیص. درمان و مشاهده بیمار
تعریف.
بیماری مزمن انسدادی ریه (COPD) بیماری است که با محدودیت جبران ناپذیر ، مداوم پیش رونده جریان هوا ناشی از پاسخ التهابی غیر طبیعی بافت ریه به عوامل آسیب رساننده محیطی مانند سیگار کشیدن ، استنشاق ذرات یا گازها مشخص می شود. اصطلاح "COPD" به ترکیبی از برونشیت مزمن و آمفیزم ریوی اشاره دارد.
مفاد مهم در مورد COPD در یک سند بین المللی که توسط متخصصان 48 کشور تهیه شده است - "ابتکار جهانی برای درمان بیماری انسدادی مزمن ریوی - GOLD ، 2003" بیان شده است. نکات کلیدی در مورد COPD باید ذکر شود.
COPD یک مفهوم جمعی متوقف شده است (برونشیت انسدادی مزمن ، اشکال شدید آسم برونش ، برونشیت از بین برنده ، فیبروز کیستیک و غیره).
COPD فقط به بیماران مبتلا به نارسایی تنفسی انتهایی اشاره نمی کند.
مفهوم "برونشیت انسدادی مزمن" توسط مفهوم "بیماری انسدادی مزمن ریوی" جذب می شود.
ارتباط.
COPD در حال حاضر چهارمین علت اصلی مرگ و میر در جهان است که با افزایش شیوع و مرگ و میر در دهه های آینده پیش بینی شده است. طبق مطالعه جهانی بار بیماری ، شیوع COPD در سال 1990 ، 34/9 در هر 1000 مرد و 33/7 در هر 1000 زن بود (GOLD ، 2003). داده های مربوط به شیوع ، بیماری و مرگ و میر ناشی از COPD به طور قابل توجهی هزینه کل بیماری را دست کم می گیرد. COPD معمولاً شناخته نشده یا تشخیص داده نمی شود تا زمانی که از نظر بالینی قابل توجه باشد. افزایش قابل توجه در آسیب گسترده ناشی از COPD طی 20 سال گذشته نشان دهنده افزایش استعمال دخانیات ، و همچنین تغییر ساختار سنی جمعیت است.
عوامل خطر برای hobl. عوامل داخلی:
عوامل ژنتیکی (کمبود آلفا 1-آنتی تریپسین) ؛
حساسیت بیش از حد راه هوایی ؛
رشد ریه
عوامل خارجی:
سیگار کشیدن
گرد و غبار و مواد شیمیایی حرفه ای ؛
آلاینده های داخلی و خارجی هوا؛
عفونت ها
وضعیت اقتصادی - اجتماعی.
اتيولوژي و پاتوژنز
توسعه COPD را می توان با کمبود مادرزادی آلفا-1-آنتی تریپسین تعیین کرد ، اما بیشتر اوقات ناشی از سیگار کشیدن فعال یا غیرفعال ، آلودگی هوا ، قرار گرفتن طولانی مدت در معرض عوامل شغلی (گرد و غبار ، بخارات ، مواد محرک شیمیایی) ، جو نامطلوب خانه (بخارات آشپزخانه ، مواد شیمیایی خانگی) است. ) اساس بیماری زایی COPD یک فرآیند التهابی مزمن از درخت نای ، پارانشیم ریوی و عروق خونی است ، که در آن تعداد بیشتری از ماکروفاژها ، لنفوسیت های T و نوتروفیل ها تشخیص داده می شود. سلولهای التهابی تعداد زیادی واسطه ترشح می کنند: لکوترین B4 ، اینترلوکین 8 ، فاکتور نکروز تومور و سایر موارد که می توانند به ساختار ریه آسیب برسانند و التهاب نوتروفیل را حفظ کنند. علاوه بر این ، عدم تعادل آنزیم های پروتئولیتیک ، آنتی پروتئینازها و استرس اکسیداتیو در پاتوژنز COPD مهم است.
از نظر ریخت شناسی در درخت نای ، سلولهای التهابی به اپیتلیوم سطحی نفوذ می کنند. غدد مخاطی منبسط شده و تعداد سلولهای جام افزایش می یابد و منجر به ترشح بیش از حد مخاط می شود. در برونش ها و برونشیول های کوچک ، روند التهابی به صورت چرخشی با بازسازی ساختاری دیواره برونش رخ می دهد ، که با افزایش محتوای کلاژن و تشکیل بافت اسکار مشخص می شود ، و منجر به انسداد مداوم مجاری تنفسی می شود.
در توسعه COPD ، یک مرحله بندی متوالی وجود دارد: بیماری با ترشح مخاط شروع می شود و بدنبال آن اختلال در اپیتلیوم مژه دار ایجاد می شود ، انسداد برونش ایجاد می شود ، که منجر به تشکیل آمفیزم ریوی ، تبادل گاز مختل ، نارسایی تنفسی ، فشار خون ریوی و ایجاد Cor pulmonale می شود. داده های داده شده به دلایل ، پاتوژنز ، مورفولوژی نشان می دهد که COPD نتیجه برونشیت مزمن ، سندرم برونکوسپاستیک طولانی مدت و / یا آمفیزم ریوی و سایر تخریب های پارانشیم (از جمله مادرزادی) همراه با کاهش خواص الاستیک ریه ها است.
هیپوکسی مزمن منجر به گلبول قرمز جبرانی - پلی سیتمی ثانویه با افزایش مربوط به ویسکوزیته خون و اختلالات میکروسیرکولاسیون می شود ، که عدم تعادل تهویه و پرفیوژن را تشدید می کند.
تشدید روند عفونی در سیستم تنفسی منجر به افزایش علائم بیماری می شود. تحت شرایط مخاط ، نقص ایمنی موضعی و بعضاً سیستمیک ، استعمار میکروارگانیسم ها می تواند ماهیتی غیرقابل کنترل داشته باشد و به یک شکل متفاوت از نظر کیفی با یک کلان ارگانیسم - یک روند عفونی - تغییر کند. راه دیگری نیز ممکن است - عفونت معمول توسط قطرات هوا با فلور بسیار بدخیم ، که در شرایط مکانیسم های محافظتی آشفته به راحتی قابل درک است. باید تأکید کرد که عفونت برونش ریوی ، اگرچه مکرر است ، اما تنها دلیل ایجاد یک تشدید نیست. همراه با این ، تشدید بیماری ممکن است همراه با افزایش تأثیر عوامل آسیب رسان برونزا ، یا در ارتباط با فعالیت بدنی ناکافی باشد. در این موارد ، علائم ضایعه عفونی دستگاه تنفسی کم است. با پیشرفت COPD ، فواصل بین تشدیدها کوتاهتر می شود.
طبقه بندی COPD(GOLD ، 2003)
0 - خطر ابتلا به بیماری:
اسپیرومتری طبیعی
علائم مزمن (سرفه ، تولید خلط) ؛
من - البته خفیف:
FEV 1 / FVC<70% от должного;
وجود یا عدم وجود علائم مزمن (سرفه ، بلغم) ؛
II - دوره متوسط:
FEV 1 / FVC<70% от должного;
50٪ ≤ OFV 1<80% от должных значений;
III - دوره شدید:
FEV 1 / FVC<70% от должного;
30٪ ≤ OFV 1<50% от должных значений;
وجود یا عدم وجود علائم مزمن ؛
IV - دوره بسیار شدید:
FEV 1 / FVC<70% от должного;
FEV 1 ≤ 30٪ از سررسید یا FEV 1<50% от должного в сочетании с хронической дыхательной недостаточностью (PaO2≤60% мм рт. ст. и/или PaCO 2 ≥ 50 мм рт. ст.);
وجود سرفه ، خلط ، تنگی نفس ، علائم بالینی نارسایی بطن راست.
درمانگاه.
تصویر بالینی COPD با همان نوع تظاهرات بالینی مشخص می شود - سرفه و تنگی نفس ، با وجود ناهمگنی بیماری های سازنده آن. میزان شدت آنها به مرحله بیماری ، میزان پیشرفت بیماری و میزان غالب آسیب به درخت برونش بستگی دارد.
میزان پیشرفت و شدت علائم COPD به شدت قرار گرفتن در معرض عوامل اتیولوژیک و جمع آنها بستگی دارد. بنابراین ، استانداردهای انجمن قفسه سینه آمریکا تأکید می کنند که ظهور اولین علائم بالینی در بیماران مبتلا به COPD معمولاً با کشیدن حداقل 20 نخ سیگار در روز به مدت 20 سال یا بیشتر است.
اولین علائمی که بیماران معمولاً با آن به پزشک مراجعه می کنند سرفه و تنگی نفس است که گاهی اوقات همراه با خس خس همراه با تولید خلط است. این علائم در صبح بیشتر نمایان می شوند.
اولین علامتی که در سن 40-50 سالگی ظاهر می شود ، سرفه است. در همان زمان ، در فصول سرد ، قسمت هایی از عفونت تنفسی شروع می شود که در ابتدا با یک بیماری همراه نیست. تنگی نفس در حین ورزش به طور متوسط \u200b\u200b10 سال پس از شروع سرفه رخ می دهد. با این حال ، در برخی موارد ، شروع بیماری از تنگی نفس امکان پذیر است.
خلط در صبح مقدار کمی ترشح می شود (به ندرت\u003e 60 میلی لیتر در روز) و دارای خصوصیاتی لزج است. تشدید طبیعت عفونی با تشدید همه علائم بیماری ، ظاهر خلط چرکی و افزایش مقدار آن آشکار می شود.
تنگی نفس می تواند بسیار متفاوت باشد ، از احساس تنگی نفس در طی فعالیت بدنی استاندارد تا نارسایی شدید تنفسی.
تعدادی از بیماران مبتلا به COPD دارای سندرم آپنه خواب انسدادی هستند. به ترکیب انسداد برونش ، مشخصه COPD ، با آپنه خواب سندرم همپوشانی گفته می شود ، که در آن اختلالات تبادل گاز بیشتر مشخص است. اعتقاد بر این است که در اکثر بیماران ، هایپرکاپنیای مزمن عمدتا در شب ایجاد می شود.
این بیماری به دو شکل بالینی وجود دارد - آمفیزماتوز و برونشیت.
شکل آمفیزماتیک (نوع) COPD عمدتا با آمفیزم پاناسینار مرتبط است. به این بیماران به طور مجازی "پف صورتی" گفته می شود ، زیرا برای غلبه بر فروپاشی زودرس بازدم برونش ها ، بازدم از طریق لب های جمع شده در لوله انجام می شود و با نوعی پف کردن همراه است. در تصویر بالینی ، تنگی نفس در حالت استراحت به دلیل کاهش سطح انتشار ریه ها غالب است. چنین بیمارانی معمولاً لاغر هستند ، سرفه آنها اغلب خشک یا با مقدار کمی خلط غلیظ و چسبناک است. چهره صورتی است زیرا اکسیژن رسانی کافی خون با افزایش تهویه تا حد ممکن حفظ می شود. در حالت استراحت به حد تهویه رسیده و بیماران تحرک بدنی را به خوبی تحمل نمی کنند. فشار خون ریوی متوسط \u200b\u200bاست ، زیرا کاهش بستر شریانی ناشی از آتروفی سپتوم اینترالوولار به مقادیر قابل توجهی نمی رسد. Cor pulmonale برای مدت طولانی جبران می شود. بنابراین ، نوع آمفیزماتیک COPD با توسعه غالب نارسایی تنفسی مشخص می شود.
فرم برونشیتی (نوع) همراه با آمفیزم سانتریاسینار مشاهده می شود. بیش از حد ترشح مداوم باعث افزایش مقاومت در هنگام الهام و انقضا می شود ، که به نقض قابل توجه تهویه کمک می کند. به نوبه خود ، کاهش شدید تهویه منجر به کاهش قابل توجه محتوای O2 در آلوئول ها ، نقض بعدی نسبت پرفیوژن-نفوذ و شنت خون می شود. این همان چیزی است که رنگ آبی مشخص سیانوز منتشر را در بیماران این گروه تعیین می کند. چنین بیمارانی چاق هستند ، و در تصویر بالینی سرفه با تولید خلط زیاد مسلط است. پنوموسکلروز منتشر و از بین بردن لومن عروق خونی منجر به ایجاد سریع Cor pulmonale و جبران خسارت آن می شود. این امر با فشار خون مداوم ریوی ، هیپوکسمی قابل توجه ، اریتروسیتوز و مسمومیت مداوم به دلیل یک روند التهابی مشخص در نایژه ها تسهیل می شود.
تخصیص دو فرم ارزش پیش آگهی دارد. بنابراین ، در نوع آمفیزماتیک در مراحل بعدی ، جبران قلب ریوی در مقایسه با نوع برونشیتی COPD رخ می دهد. در شرایط بالینی ، بیماران مبتلا به یک نوع بیماری مختلط شیوع بیشتری دارند.
طبقه بندی COPD براساس شدت ، تعدادی از مراحل بیماری را مشخص می کند. مرحله 0 به معنای افزایش خطر ابتلا به COPD است. این با شروع علائم (سرفه ، تولید خلط) با عملکرد تهویه طبیعی ریه ها مشخص می شود و در واقع مربوط به برونشیت مزمن است. با COPD خفیف ( مرحله من) و حداقل علائم بالینی (سرفه ، خلط) اختلالات انسدادی ثبت شده است. با COPD متوسط \u200b\u200b( مرحله دوم) ، اختلالات انسدادی برجسته تری در تهویه ریوی ثبت می شود ، و علاوه بر سرفه و خلط ، تنگی نفس ظاهر می شود ، که نشان دهنده توسعه نارسایی تنفسی است. در COPD شدید و بسیار شدید ( مرحله III - IV) نارسایی تنفسی مزمن و علائم Cor pulmonale (نارسایی بطن راست) وجود دارد. اختلالات انسدادی شناسایی شده در مطالعه عملکرد تهویه ریه ها می تواند به مقادیر حیاتی برسد.
علائم اصلی برای شک به COPD.
سرفه مزمن
متناوب یا روزانه. این اغلب در تمام طول روز اتفاق می افتد.
ترشح مزمن خلط
هر مورد ترشح مزمن خلط ممکن است نشان دهنده COPD باشد.
تنگی نفس
پیشرو ، پایدار. با ورزش و عفونت های تنفسی تشدید می شود.
سابقه قرار گرفتن در معرض عوامل خطر
استعمال دخانیات ، آلاینده های حرفه ای و مواد شیمیایی. دود از آشپزخانه و گرمایش در خانه.
در صورت وجود هر یک از این علائم ، باید به COPD مشکوک شده و آزمایش عملکرد تنفسی انجام شود.
تاریخ سیگار کشیدن
طبق پیش بینی WHO ، پیش شرط تشخیص COPD محاسبه شاخص استعمال دخانیات است. محاسبه شاخص استعمال دخانیات به شرح زیر انجام می شود: تعداد سیگارهای دودی در روز در تعداد ماه های سال ضرب می شود ، یعنی توسط 12؛ اگر این مقدار از 160 فراتر رود ، سیگار کشیدن در این بیمار در رابطه با توسعه COPD خطری ایجاد می کند. اگر از این شاخص فراتر رود ، بیش از 200 بیمار باید به عنوان "سیگاری های سنگین" طبقه بندی شوند.
توصیه می شود سابقه استعمال سیگار را در واحد "بسته / سال" محاسبه کنید. تاریخ سیگار کشیدن باید شامل تعداد سیگارهای کشیده شده در روز ضرب در تعداد سالها باشد و بنابراین تعداد کل بسته ها / سال های سیگار کشیدن محاسبه می شود. در عین حال ، یک بسته حاوی 20 نخ سیگار است و تعداد سیگارهای کشیده شده در روز به مدت یک سال برابر با یک بسته در سال است.
بسته های کل / سال \u003d تعداد سیگارهای دودی در روز x تعداد سالها / 20
اعتقاد بر این است که اگر این مقدار بیش از 25 بسته در سال باشد ، می توان بیمار را به عنوان "سیگاری سنگین" طبقه بندی کرد. درصورتی که این رقم به 10 بسته در سال برسد ، بیمار "سیگاری بدون شرط" در نظر گرفته می شود. بیمار در صورت ترک سیگار برای مدت 6 ماه یا بیشتر "سیگاری سابق" محسوب می شود. این باید هنگام تشخیص COPD در نظر گرفته شود.
تحقیق عینی.
نتایج یک مطالعه عینی روی بیماران مبتلا به COPD به شدت انسداد برونش و آمفیزم بستگی دارد.
بازرسی. در مراحل پایانی COPD ، علائم بالینی آمفیزم ریوی (افزایش اندازه قفسه سینه قبل از خلفی ، فضای بین دنده ای متسع) وجود دارد. با آمفیزم شدید ، ظاهر بیمار تغییر می کند ، یک سینه بشکه ای ظاهر می شود. به دلیل انبساط قفسه سینه و جابجایی ترقوه ها به سمت بالا ، گردن کوتاه و ضخیم به نظر می رسد ، سوراخ های سوپراکلایوکولار بیرون زده اند (پر شده از قسمت بالای ریه ها) با ایجاد نارسایی تنفسی مزمن و فشار خون ریوی ، آکروسیانوز "گرم" ، تورم گردن متورم شده است.
کوبه ای در حضور آمفیزم - صدای جعبه کوبه ای ، گسترش مرزهای ریه ها. در موارد آمفیزم شدید ، ممکن است تیرگی مطلق قلب کاملاً مشخص نباشد. لبه های ریه ها به سمت پایین جابجا می شوند ، تحرک آنها در هنگام تنفس محدود است. در نتیجه ، از زیر لبه قوس ساحلی ، یک لبه نرم و بدون درد کبد می تواند در اندازه طبیعی خود بیرون بیاید.
سکوتدر ریه ها ، رال های خشک و پراکنده از صدای مختلف شنیده می شود. با پیشرفت بیماری ، خس خس به سرفه اضافه می شود ، که بیشتر با انقضا سریع مشاهده می شود. گاهی اوقات پدیده های سمعک در ریه ها تشخیص داده نمی شود و برای تشخیص آنها پیشنهاد می شود بیمار یک بازدم اجباری انجام دهد. تحرک دیافراگم با آمفیزم شدید محدود می شود ، که منجر به تغییر در تصویر سمعک می شود: تنفس ضعیف ظاهر می شود ، شدت خس خس سینه کاهش می یابد ، بازدم طولانی می شود.
حساسیت روشهای عینی برای تعیین شدت COPD کم است. از جمله علائم کلاسیک ، بازدم خس خس سینه و مدت زمان بازدم طولانی (بیش از 5 ثانیه) است که نشان دهنده انسداد برونش است.
عیب یابی
روشهای تشخیصی را می توان به طور شرطی به حداقل اجباری که در همه بیماران استفاده می شود و روشهای اضافی برای علائم خاص استفاده کرد.
روش های اجباری ، علاوه بر فیزیکی ، شامل تعیین عملکرد تنفس خارجی (FVD) ، آنالیز خون ، بررسی سیتولوژیک خلط ، معاینه اشعه ایکس ، آنالیز خون و نوار قلب است.
روشهای تحقیق آزمایشگاهی.
معاینه خلط.
یک بررسی سیتولوژیک خلط اطلاعاتی در مورد ماهیت روند التهابی و شدت آن فراهم می کند. ضروری.
بررسی میکروبیولوژیکی (خلط) خلط توصیه می شود که با پیشرفت کنترل نشده روند عفونی و انتخاب آنتی بیوتیک درمانی منطقی انجام شود. این یک روش معاینه اضافی است.
آزمایش خون.
آنالیز بالینی. با یک دوره پایدار COPD ، تغییرات قابل توجهی در محتوای لکوسیت های خون محیطی رخ نمی دهد. با تشدید ، لکوسیتوز نوتروفیل با تغییر چاقو و افزایش ESR اغلب مشاهده می شود. با این حال ، این تغییرات همیشه مشاهده نمی شوند.
با ایجاد هیپوکسمی در بیماران مبتلا به COPD ، سندرم پلی سیتمیک ایجاد می شود که با تغییر در هماتوکریت (هماتوکریت\u003e 47 in در زنان و\u003e 52 in در مردان) ، افزایش تعداد گلبول های قرمز خون ، سطح هموگلوبین بالا ، ESR کم و افزایش ویسکوزیته خون مشخص می شود.
معاینه با اشعه ایکس اندام های قفسه سینه یک روش معاینه اجباری است. رادیوگرافی ریه ها در پیش بینی های پیشانی و جانبی در COPD افزایش شفافیت بافت ریه ، ایستادن کم گنبد دیافراگم ، محدودیت تحرک آن ، افزایش فضای رتروسترنال ، که از ویژگی های آمفیزم است را نشان می دهد.
با COPD خفیف ، ممکن است تغییرات رادیوگرافی قابل توجهی تشخیص داده نشود. در بیماران مبتلا به COPD متوسط \u200b\u200bو شدید ، می توان ایستادن پایین گنبد دیافراگم ، صاف شدن و محدودیت تحرک آن ، بیش هوایی بودن زمینه های ریوی ، بولا و افزایش فضای رتروسترنال را تشخیص داد. باریک شدن و کشیدگی سایه قلب. در برابر پس زمینه سایه های عروقی ، تراکم زیادی از دیواره برونش ها تعیین می شود ، نفوذ در طول دوره آنها ، یعنی تعدادی از علائم مشخص می شود که روند التهابی در درخت برونش و وجود آمفیزم را مشخص می کند.
سی تی اسکن ریه ها یک روش اضافی است و با توجه به نشانه های خاص انجام می شود. این به شما امکان می دهد تا تغییرات مورفولوژیکی در ریه ها ، اول از همه ، آمفیزم را تعیین کنید تا بولها ، محل و اندازه آنها را به وضوح مشخص کنید.
الکتروکاردیوگرافی اجازه می دهد تا علائم هیپرتروفی قلب راست در تعدادی از بیماران شناسایی شود ، اما معیارهای ECG آن به دلیل آمفیزم به طور چشمگیری تغییر می کند. داده های ECG در اکثر موارد باعث می شود که پیدایش قلب علائم تنفسی کنار گذاشته نشود.
معاینه مقدماتی (فیبروبرونکوسکوپی) برای بیماران مبتلا به COPD اختیاری است. برای ارزیابی وضعیت مخاط برونش و تشخیص افتراقی با سایر بیماری های ریوی انجام می شود. در برخی موارد ، بیماری هایی که علت انسداد مزمن برونش هستند ، قابل شناسایی هستند.
تحقیقات باید شامل موارد زیر باشد:
معاینه مخاط برونش ؛
بررسی فرهنگی محتوای برونش
شستشوی برونکوآلوئولار با تعیین ترکیب سلول برای روشن شدن ماهیت التهاب ؛
بیوپسی مخاط برونش.
بررسی عملکرد تنفس خارجی (اسپیروگرافی) از اهمیت بالایی در تشخیص COPD و ارزیابی عینی شدت بیماری برخوردار است. تعیین پارامترهای حجمی و سرعت زیر ضروری است: ظرفیت حیاتی ریه ها (VC) ، ظرفیت حیاتی ریه ها (FVC) ، حجم بازدم مجبور در 1 ثانیه (FEV 1) ، حداکثر میزان جریان بازدم در 75 ، 50 و 25٪ (MSV 75-) 25) مطالعه این شاخص ها شکل می گیرد تشخیص عملکرد COPD.
اختلالات عملکردی در COPD نه تنها با اختلال در حفره برونش ، بلکه با تغییر در ساختار حجمهای ساکن ، اختلال در خاصیت ارتجاعی ، ظرفیت انتشار ریه ها و کاهش عملکرد بدنی نیز آشکار می شود. تعریف این گروه از اختلالات اختیاری است.
نقض قابلیت بازرسی برونش.مهمترین چیز برای تشخیص COPD تعیین محدودیت مزمن جریان هوا است ، به عنوان مثال. انسداد برونش معیار اصلی برای تعیین محدودیت مزمن جریان هوا یا انسداد مزمن ، افت FEV 1 به سطحی است که کمتر از 80٪ مقادیر مناسب است. انسداد برونشال اگر در طی مطالعات تکرار اسپیرومتری حداقل 3 بار در طی یک سال با وجود ادامه درمان ثبت شود ، مزمن در نظر گرفته می شود.
برای مطالعه برگشت پذیری انسداد ، از نمونه هایی با گشادکننده های برونش استنشاق استفاده می شود و تأثیر آنها بر منحنی جریان جریان ، عمدتا بر حجم بازدم مجبور در 1 ثانیه (FEV 1) ارزیابی می شود. هنگام معاینه یک بیمار خاص مبتلا به COPD ، باید به خاطر داشت که برگشت پذیر انسداد یک مقدار متغیر است. و در یک بیمار می تواند در طی دوره های تشدید و بهبودی متفاوت باشد.
آزمایش های گشاد کننده برونش... به عنوان داروهای گشاد کننده برونش هنگام انجام آزمایشات در بزرگسالان ، توصیه می شود:
بتا 2 - آگونیست های کوتاه مدت (با شروع از حداقل دوز تا حداکثر میزان مجاز: فنوترول - از 100 تا 800 میکروگرم ؛ سالبوتامول - از 200 تا 800 میکروگرم ، تربوتالین - از 250 تا 1000 میکروگرم) با اندازه گیری پاسخ برونش منبسط پس از 15 دقیقه ؛
داروهای آنتی کولینرژیک - توصیه می شود از ایپراتروپیوم بروماید به عنوان یک داروی استاندارد استفاده کنید ، از حداقل دوز 40 میکروگرم تا حداکثر دوز ممکن 80 میکروگرم شروع می شود ، با اندازه گیری پاسخ گشادی برونش پس از 30-45 دقیقه.
می توان با تجویز دوزهای بالاتر داروهایی که از طریق نبولایزرها استنشاق می شوند ، آزمایشات برونکودیلاتور انجام داد.
برای جلوگیری از تحریف نتایج و برای انجام صحیح آزمایش اتساع برونش ، لازم است درمان مطابق با خواص فارماکوکینتیک داروی مصرفی لغو شود (بتا 2) - آگونیست های کوتاه مدت - 6 ساعت قبل از شروع آزمایش ، بتا -2 با عملکرد طولانی - آگونیست ها - در 12 ساعت ، تئوفیلین های طولانی مدت - در 24 ساعت).
افزایش FEV1 بیش از 15٪ از مقادیر پایه به طور معمول به عنوان انسداد برگشت پذیر توصیف می شود.
نظارت بر FEV 1 . یک روش مهم برای تأیید تشخیص COPD ، نظارت بر FEV 1 است - اندازه گیری مکرر طولانی مدت این شاخص اسپیرومتریک. در بزرگسالی ، به طور معمول کاهش سالانه FEV 1 طی 30 میلی لیتر در سال مشاهده می شود. مطالعات گسترده اپیدمیولوژیکی انجام شده در کشورهای مختلف این امکان را فراهم کرده است که مشخص شود بیماران مبتلا به COPD با کاهش سالانه FEV1 بیش از 50 میلی لیتر در سال مشخص می شوند.
ترکیب گاز خون. COPD با نقض نسبت تهویه و پرفیوژن همراه است ، که می تواند منجر به هیپوکسمی شریانی شود - کاهش کشش اکسیژن در خون شریانی (PaO2). علاوه بر این ، نارسایی تنفسی تهویه منجر به افزایش فشار دی اکسید کربن در خون شریانی (PaCO2) می شود. در بیماران مبتلا به COPD با نارسایی تنفسی مزمن ، با افزایش تولید بی کربنات ، که می تواند سطح pH نسبتاً طبیعی را حفظ کند ، شروع اسیدوز متابولیکی جبران می شود.
اکسیمتری پالس این برای اندازه گیری و نظارت بر میزان اشباع اکسیژن خون (SaO2) استفاده می شود ، با این وجود ، امکان ثبت تنها سطح اکسیژن رسانی وجود دارد و اجازه پیگیری تغییرات PaCO2 را نمی دهد. اگر SaO2 کمتر از 94٪ باشد ، آزمایش گاز خون نشان داده می شود.
با پیشرفت COPD ، اغلب افزایش فشار شریان ریوی مشاهده می شود.
شدت فشار خون ریوی دارای ارزش پیش آگهی است. در میان روشهای غیرتهاجمی برای کنترل فشار خون ریوی ، بهترین نتایج با استفاده از این روش بدست آمد اکوکاردیوگرافی داپلر... در مدیریت روتین بیماران COPD ، استفاده از اندازه گیری فشار مستقیم شریان ریوی توصیه نمی شود.
تشخیص های افتراقی.
در مراحل اولیه توسعه COPD ، باید بین برونشیت انسدادی مزمن (COP) و آسم برونش (BA) تمایز قائل شد ، زیرا در این زمان برای درمان هر یک از این بیماریها به روشهای مختلفی نیاز است.
معاینه بالینی علائم پاروکسیسم را در AD نشان می دهد ، اغلب با ترکیبی از علائم خارج ریوی آلرژی (رینیت ، ملتحمه ، تظاهرات پوستی ، آلرژی غذایی). بیماران مبتلا به COB با علائم ثابت و کم تغییر مشخص می شوند.
یکی از عناصر مهم تشخیص افتراقی کاهش FEV 1 به میزان 50 میلی لیتر در بیماران مبتلا به COB است که در BA مشاهده نمی شود. COB با کاهش تنوع روزانه معیارهای جریان اوج مشخص می شود.< 15%. При БА разность между утренними и вечерними показателями пикфлоуметрии повышена и превышает 20%. При БА чаще наблюдается бронхиальная гиперреактивность. Из лабораторных признаков при БА чаще встречается увеличение содержания IgЕ. При появлении у больных БА необратимого компонента бронхиальной обструкции, дифференциальный диагноз этих заболеваний теряет смысл, так как можно констатировать присоединение второй болезни – ХОБ и приближение конечной фазы заболевания – ХОБЛ.
رفتار.
هدف از درمان کاهش میزان پیشرفت بیماری منجر به افزایش انسداد برونش و نارسایی تنفسی ، کاهش دفعات و مدت زمان تشدید ، افزایش تحمل ورزش و بهبود کیفیت زندگی است.
آموزش بیمار - مرحله حیاتی کار فردی با بیمار. بیمار باید به خوبی از ماهیت بیماری ، ویژگی های دوره آن آگاهی داشته باشد ، یک شرکت کننده فعال و آگاه در روند درمان باشد. برنامه های آموزشی برای بیماران لزوماً شامل آموزش استفاده صحیح از داروها (استنشاقی های جداگانه ، اسپیسرها ، نبولایزرها) است. بیماران باید در قوانین اساسی کنترل خود ، از جمله استفاده از یک جریان سنج پیک ، آموزش ببینند ، باید بتوانند وضعیت خود را به طور عینی ارزیابی کنند و در صورت لزوم ، اقدامات فوری برای کمک به خود انجام دهند. یک مرحله مهم در آموزش بیماران جهت گیری حرفه ای آنهاست ، خصوصاً در مواردی که پرخاشگری محیطی با فعالیت حرفه ای بیمار همراه است.
ترک سیگار اولین قدم مورد نیاز است بیمار باید به وضوح از تأثیرات مضر دود تنباکو بر روی سیستم تنفسی خود آگاه باشد. یک برنامه محدودیت و ترک سیگار در حال تدوین است. در موارد اعتیاد به نیکوتین توصیه می شود از داروهای جایگزین نیکوتین استفاده کنید. جذب روان درمانگران ، متخصصان طب سوزنی امکان پذیر است. اثر مثبت ترک سیگار در هر مرحله از COPD بیان می شود.
درمان گشادکننده برونش.
با توجه به مفاهیم مدرن ذات COPD ، انسداد برونش منبع اصلی و جهانی تمام وقایع آسیب شناختی است که با پیشرفت مداوم بیماری ایجاد می شود و منجر به نارسایی تنفسی می شود.
استفاده از داروهای گشاد كننده برونش ، درمان اساسی است كه در درمان بیماران مبتلا به COPD اجباری است. تمام روشها و روشهای دیگر باید فقط در ترکیب با روشهای درمانی اساسی استفاده شود.
اولویت استفاده از اشکال استنشاق کننده برونکودیلاتور است. مسیر استنشاق تجویز داروها به نفوذ سریع دارو به اندام آسیب دیده کمک می کند ، بنابراین یک اثر دارویی موثرتر است. در عین حال ، خطر بالقوه ایجاد اثرات سیستمیک جانبی به طور قابل توجهی کاهش می یابد. استفاده از اسپیسر اجازه می دهد: برای تسهیل اجرای استنشاق ، افزایش اثربخشی آن ، برای کاهش بیشتر خطر احتمالی ایجاد عوارض جانبی سیستمیک و محلی
امروزه مطلوب استفاده از استنشاق کننده های پودر یا گشاد کننده برونش در محلول های درمانی با نبولایزر است.
از بین برش دهنده های برونش موجود ، m-anticholinergics ، beta-2-agonists و methylxanthines در درمان COPD استفاده می شود. توالی استفاده و ترکیب این وجوه به شدت بیماری ، خصوصیات فردی پیشرفت آن بستگی دارد.
به طور سنتی ، گشاد کننده های برونش اساسی برای درمان COPD در نظر گرفته می شوند m-anticholinergics... آنها توسط ipratropium bromide (مدت زمان عمل 6-8 ساعت) و یک برش دهنده برونش ترکیبی - berodual (ipratropium bromide + fenoterol) نشان داده می شوند. در حال حاضر ، یک آنتی کولینرژیک جدید با اثر طولانی مدت ، تیوتروپیوم بروماید (ارواح) ظاهر شده است که یک بار در روز استفاده می شود.
استفاده می شود گزینشی سمپاتومیمتیک (آگونیست های بتا 2) عمل کوتاه (4-6 ساعت): فنوترول ، سالبوتامول ، تربوتالین. عمل سمپاتومیمتیک ها به سرعت اتفاق می افتد ، اما به دلیل تأثیر بر سیستم قلبی عروقی ، با تعدادی از عوارض جانبی سیستمیک مشخص می شود. با افزایش سن ، حساسیت گیرنده ها نسبت به علائم سمپاتیک کاهش می یابد. در سالهای اخیر ، برای تسکین انسداد برونش و درمان اساسی COPD ، داروی جدیدی از گروه آگونیستهای بتا -2 ، oxis turbuhaler ، به طور گسترده ای مورد استفاده قرار گرفته است - ماده فعال آن فرموترول است که نه تنها شروع سریع عمل دارد (بعد از 1-3 دقیقه) ، بلکه یک داروی طولانی نیز است. اثر (به مدت 12 ساعت یا بیشتر).
تئوفیلین عمل طولانی مدت (teotard ، teopec) در درمان COPD موثر است و در حال حاضر به طور گسترده ای هم به عنوان مونوتراپی و علاوه بر سمپاتومیمتیک استفاده می شود. اما با توجه به مرز باریک آنها بین دوزهای درمانی و سمی ، اولویت با گشادکننده های برونش تنفسی است.
در مرحله I COPD ، گشادکننده برونش کوتاه مدت در صورت تقاضا استفاده می شود. در مراحل II - IV ، استفاده سیستماتیک از یک گشاد کننده برونش (یا ترکیبی از داروها) ، کوتاه مدت یا طولانی مدت ، با یک اثر سریع تجویز می شود. اگر عملکرد بالینی و تهویه آنها به طور قابل توجهی بهبود یابد ، از کورتیکواستروئیدهای استنشاقی استفاده می شود.
عوامل تنظیم کننده قانون... بهبودی در ترخیص کالا از گمرک مخاطی تا حد زیادی با تأثیر هدفمند بر ترشحات برونش با استفاده از داروهای تنظیم کننده رگ به دست می آید.
استفاده از آنزیم های پروتئولیتیک به عنوان عوامل موکولیتیک به دلیل خطر بالای عوارض جانبی جدی - hemoptysis ، آلرژی ، انقباض برونش غیر قابل قبول است. آمبروکسول (آمبروسان ، لازولوان) تشکیل ترشحات تراشه برونش را کاهش می دهد که باعث کاهش ویسکوزیته می شود به دلیل دپلیمریزاسیون موکوپلی ساکاریدهای اسیدی مخاط برونش و تولید موکوپلی ساکاریدهای خنثی توسط سلول های جام.
از ویژگیهای بارز این دارو توانایی افزایش سنتز ، ترشح سورفاکتانت و جلوگیری از تجزیه ماده تحت تأثیر عوامل نامطلوب است.
آمبروکسول هنگامی که با آنتی بیوتیک ها ترکیب می شود ، نفوذ آنها را به ترشحات برونش و مخاط برونش افزایش می دهد و باعث افزایش اثربخشی درمان آنتی بیوتیکی و کاهش مدت زمان آن می شود. این دارو به صورت داخلی و استنشاق استفاده می شود.
استیل سیستئین عاری از اثرات مخرب آنزیم های پروتئولیتیک. گروه های سولفیدریل مولکول های آن پیوندهای دی سولفید موکوپلی ساکاریدهای خلط را می شکنند. تحریک سلولهای مخاطی نیز منجر به رقت خلط می شود. استیل سیستئین باعث افزایش سنتز گلوتاتیون می شود که در فرآیندهای سم زدایی نقش دارد. در داخل و در استنشاق استفاده می شود.
کربوسیستاین نسبت کمی سیالوموسین های اسیدی و خنثی ترشحات برونش را نرمال می کند. تحت تأثیر دارو ، بازسازی غشای مخاطی ، کاهش تعداد سلولهای جام ، به ویژه در برونشهای انتهایی ، یعنی این دارو دارای اثرات تنظیم کننده مخاط و موکولیتیک است. این ترشح IgA و تعداد گروه های سولفیدریل را بازیابی می کند. در داخل استفاده می شود.
گلوکوکورتیکواستروئید درمانی. نشانه استفاده از GCS در COPD بی اثر بودن حداکثر دوزهای درمان اساسی - گشادکننده برونش است. GCS ، که در درمان آسم برونش بسیار مثر است ، در درمان COPD فقط با اثر بالینی یا اسپیرومتری ثابت شده استفاده می شود. یک تست برگشت پذیری برای پیش بینی میزان تجویز کورتیکواستروئیدها فرموله شده است: پس از تعیین اولیه FEV 1 ، کورتیکواستروئیدها به صورت خوراکی (به مدت 1-2 هفته) یا استنشاق (به مدت 6-12 هفته) تجویز می شوند. افزایش FEV 1 به میزان 15٪ (یا 200 میلی لیتر) پس از استفاده آزمایشی از استروئیدها نتیجه مثبتی تلقی می شود و زمینه را برای درمان طولانی مدت با کورتیکواستروئیدهای استنشاقی فراهم می کند. این آزمایش همچنین می تواند با استفاده از حداکثر جریان سنجی انجام شود (افزایش قدرت بازدم 20٪ مثبت تلقی می شود).
استفاده از GCS در قرص ها بیش از 2 هفته نامطلوب است. استفاده از GCS استنشاقی یا محلول (سوسپانسیون) برای نبولایزرها (به عنوان مثال ، سوسپانسیون Pulmicort) مطلوب است. در COPD شدید و بسیار شدید ( مرحله III - IV) به عنوان یک روش درمانی اساسی ، توصیه می شود از داروی ترکیبی سیمبیکورت استفاده شود که شامل کورتیکواستروئیدهای بودسونید و یک فرموترول بتا 2-آگونیست با اثر طولانی مدت است.
درمان نبولایزر در درمان تشدید بیماری COPD ضروری است. نبولایزر استنشاق گشادکننده های برونش و هورمونهای گلوکوکورتیکواستروئید را در دوزهای بالا امکان پذیر می کند.
اصلاح نارسایی تنفسی با استفاده از اکسیژن درمانی ، آموزش عضلات تنفسی به دست می آید. باید تأکید کرد که شدت ، حجم و ماهیت درمان دارویی به شدت شرایط و نسبت اجزای برگشت پذیر و برگشت ناپذیر انسداد برونش بستگی دارد. با کاهش م componentلفه برگشت پذیر ، ماهیت درمان تغییر می کند. در وهله اول روشهایی با هدف اصلاح نارسایی تنفسی وجود دارد. در همان زمان ، حجم و شدت درمان اساسی حفظ می شود.
نشانه برای اکسیژن درمانی سیستماتیک کاهش کشش جزئی اکسیژن در خون است - PaO2 تا 60 میلی متر جیوه. هنر ، کاهش اشباع اکسیژن - SaO2< 85% при стандартной пробе с 6-минутной ходьбой и < 88% в покое. Предпочтение отдается длительной (18 часов в сутки) малопоточной (2-5 л в мин) кислородотерапии как в стационарных условиях, так и на дому. При тяжелой дыхательной недостаточности применяются гелиево-кислородные смеси. Для домашней оксигенотерапии используются концентраторы кислорода, а также приборы для проведения неинвазивной вентиляции с отрицательным и положительным давлением на вдохе и выдохе.
تمرین عضلات تنفسی با کمک تمرینات تنفسی جداگانه انتخاب می شود. امکان استفاده از تحریک الکتریکی از راه پوست دیافراگم وجود دارد.
در سندرم پلی سیتمیک شدید (Hb\u003e 155 گرم در لیتر) ، اریتروسیتافورز با حذف 500-600 میلی لیتر از توده گلبول قرمز تخریب شده. اگر اریتروسیتافورز از نظر فنی امکان پذیر نباشد ، خونریزی در حجم 800 میلی لیتر خون با جایگزینی مناسب با محلول کلرید سدیم ایزوتونیک یا هرودوتراپی (درمان با زالو).
ضد باکتری درمانی. آنتی بیوتیک درمانی در طول دوره COPD پایدار انجام نمی شود.
در فصل سرما ، بیماران مبتلا به COPD اغلب تشدیدهای منشا of عفونی را تجربه می کنند. شایع ترین علل آن استرپتوکوک پنومونی ، هموفیلوس آنفلوانزا ، موراکسلا کاتارالیس و ویروس ها است. آنتی بیوتیک ها در صورت وجود علائم بالینی مسمومیت ، افزایش مقدار خلط و ظهور عناصر چرکی در آن تجویز می شوند. معمولاً ، درمان بصورت تجربی با داروهای داخل تجویز می شود و 7-14 روز طول می کشد ، با تشدید شدید ، از تجویز تزریقی استفاده می شود.
با در نظر گرفتن طیف مشخص شده از میکروارگانیسم ها ، موارد زیر را اعمال کنید:
آمینوپنی سیلین های داخل (آموکسی سیلین) ،
سفالوسپورین های نسل II-III (سفوروکسیم از راه خوراکی ، سفتریاکسون - از نظر تزریق)
ماکرولیدهای جدید داخل (اسپیرامایسین ، کلاریترومایسین ، آزیترومایسین ، میدکامایسین) ،
فلوئوروکینولونهای تنفسی (پنوموتروپیک) از نسل III-IV (لووفلوکساسین).
انتخاب یک آنتی بیوتیک با توجه به حساسیت فلور در شرایط in vitro فقط در صورت بی اثر بودن آنتی بیوتیک درمانی تجربی انجام می شود.
آنتی بیوتیک استنشاقی نباید تجویز شود.
واکسیناسیوندر برابر آنفلوانزا (Vaxigrip ، آنفلوانزا ، آنفلوانزا ، بگریواک ، و غیره) ، در برابر پنوموکوک (پنومو 23) اجازه می دهد تا تعداد تشدید بیماری و شدت روند آنها را کاهش دهد ، در نتیجه تعداد روزهای ناتوانی را کاهش می دهد و قابلیت بازرسی برونش را بهبود می بخشد. توصیه می شود واکسیناسیون پیشگیرانه سالانه علیه آنفلوانزا در بیماران COPD با شدت خفیف و متوسط \u200b\u200bبیماری و تکرار عودهای عفونی بیش از 2 بار در سال باشد. یک واکسیناسیون پنومو 23 به مدت 5 سال م effectiveثر است ، سپس واکسیناسیون مجدد هر 5 سال انجام می شود.
توانبخشی درمانی.
درمان توان بخشی برای COPD از هر حدی تجویز می شود. پزشک برای هر بیمار یک برنامه توان بخشی فردی تعیین می کند. بسته به شدت ، مرحله بیماری و میزان جبران سیستم تنفسی و قلبی عروقی ، این برنامه شامل یک رژیم ، ورزش درمانی ، روشهای فیزیوتراپی و درمان آبگرم است.