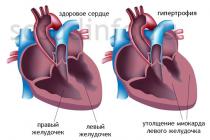
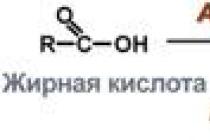
سندرم DIC یا سندرم انعقاد داخل عروقی منتشر ، یک فرایند آسیب شناختی چند جزئی پیچیده در سیستم hemostatic است ، افزایش تشکیل ترومبوس در عروق ریز عروق.
این وضعیت اغلب در عمل پزشکان از هر تخصصی رخ می دهد ، متخصصان زنان و زایمان ، احیاگران ، جراحان ، پزشکان اورژانس با آن روبرو می شوند. همچنین رایج ترین شکل اختلالات لخته شدن خون (انعقاد خون) در مراقبت های ویژه در بزرگسالان و کودکان است.
کوآگلوپاتی شرایطی است که با تغییرات خاصی از خارج همراه است. انواع اصلی انعقاد خون ، مادرزادی (ژنتیکی) و اکتسابی است که یکی از انواع آن ، انعقاد داخل عروقی منتشر است. در ادبیات ، می توان داده هایی را در مورد به اصطلاح انعقاد انعقاد خون یا سندرم ابر انعقاد پذیر پیدا کرد که با علائم آزمایشگاهی افزایش انعقاد خون مشخص می شود ، اما ترومبوز غالباً وجود ندارد.
سندرم DIC دارای مکانیسم های پیچیده ای از تکامل ، تظاهرات مختلف بالینی است و معیارهای تشخیصی دقیق آن هنوز مشخص نشده است ، که باعث ایجاد مشکلات قابل توجهی در تشخیص و درمان آن می شود. این وضعیت همیشه هر بیماری دیگری را پیچیده می کند ، بنابراین یک بیماری مستقل نیست.
ترومبوز: طبیعی یا پاتولوژیک؟
برای اینکه بفهمید دلیل چیست و مکانیسم های بروز چنین اختلالی مانند انعقاد داخل عروقی منتشر چیست ، باید مراحل اصلی انعقاد خون را بدانید.
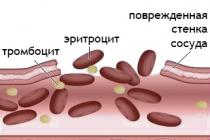
فرد به طور مداوم با خطر صدمات احتمالی ، از خراش های جزئی یا بریدگی تا آسیب های جدی روبرو می شود ، بنابراین ، طبیعت مکانیسم محافظتی خاصی را ایجاد می کند - ترومبوز ، یعنی تشکیل لخته خون در محل آسیب رساندن به رگ.
در سیستم دو سیستم مخالف وجود دارد - منعقد کننده و پادبند ، تعامل صحیح آن در صورت لزوم به تشکیل ترومب کمک می کند ، و همچنین حالت مایع خون در عروق در صورت عدم آسیب. این سیستم های هموستاتیک نقش محافظتی بسیار مهمی دارند.

هنگامی که یکپارچگی دیواره عروق نقض می شود ، سیستم انعقادی فعال می شود ، یک واکنش کامل که منجر به تشکیل (لخته در لومن عروق یا محفظه قلب) می شود. پروتئین های پلاسما مستقیماً در این امر دخیل هستند ، همچنین پلاکت ها ، فاکتورهای لخته شدن تشکیل شده در کبد و آنزیم های مختلف. نتیجه تشکیل لخته خون است که نقص دیواره عروق را می بندد و از خونریزی بیشتر جلوگیری می کند.
برای حفظ حالت مایع خون و جلوگیری از تشکیل کنترل نشده لخته های خون ، موارد خاص وجود دارد مکانیسم های ضد ترومبوتیکاجرا شده توسط عمل به اصطلاح ضدانعقاد - موادی که از بروز ترومبوز عظیم جلوگیری می کنند (پروتئین های پلاسما ، آنزیم های پروتئولیتیک ، هپارین درون زا). علاوه بر این ، با جریان سریع خون و به اصطلاح فیبرینولیز ، یعنی انحلال پروتئین فیبرین و خارج شدن آن از بستر عروقی با استفاده از آنزیم های گردش یافته در پلاسمای خون و ترشح شده توسط لکوسیت ها ، پلاکت ها و سلول های دیگر ، از بروز ترومبوز جلوگیری می شود. بقایای فیبرین پس از تخریب توسط لکوسیت ها و ماکروفاژها جذب می شود.
هنگامی که تعامل اجزای سیستم هموستاز در بیماری ها و آسیب های مختلف تغییر می کند ، در کار سیستم های انعقادی و ضد انعقاد خون ناهماهنگی وجود دارد، که به ترومبوز گسترده کنترل نشده همراه با خونریزی کمک می کند. این مکانیسم ها اساس پاتوژنز DIC را تشکیل می دهند ، که یک عارضه تهدید کننده زندگی است.
علل انعقاد داخل عروقی منتشر شده
از آنجا که DIC یک بیماری مستقل نیست ، بدون هیچ تاثیری که سیستم انعقادی را فعال کند ایجاد نمی شود. شایع ترین علل وقوع آن:
- عفونت - شوک سپتیک ، ضایعات شدید باکتریایی و ویروسی ؛
- انواع مختلف شوک (آسیب زا ، سمی عفونی ، هیپوولمیک و غیره) ، شرایط ترمینال ؛
- آسیب ها ، از جمله مداخلات جراحی آسیب زا (پیوند اعضا ، پروتز دریچه های قلب) ، استفاده از دستگاه های قلب و ریه و همودیالیز در حین مداخلات جراحی.
- بیماری های انکولوژیک ، به ویژه اشکال شایع سرطان
- سندرم DIC در زنان و زایمان - ، جدا شدن زودرس جفت ،
- در دوران بارداری در صورت بروز (اکلامپسی ، پره اکلامپسی) ، حاملگی خارج رحمی و غیره ؛
- بیماری های شدید سیستم قلبی عروقی ، فرآیندهای چرکی-التهابی اندام های داخلی.
به این ترتیب سندرم DIC در بیشتر بیماری های جدی و شرایط ترمیم همراه است (مرگ بالینی ، اقدامات احیای بعدی). در مرحله ایجاد حضور آنها ، انعقاد خون یا از قبل وجود دارد ، یا اگر اقدامات پیشگیرانه مناسبی انجام نشود ، ایجاد می شود.
DIC در نوزادان تازه متولد شده ای که سالم و به موقع به دنیا می آیند بسیار نادر است. بیشتر اوقات با ترومای شدید هنگام تولد ، آمبولی مایع آمنیوتیک اتفاق می افتد (در این حالت ، علائم آن هم در مادر و هم در جنین مشاهده می شود) ، اختلالات تنفسی.
در کودکان ، انعقاد ارثی ، به ویژه ، ممکن است و با افزایش خونریزی همراه باشد ، در حالی که سندرم ترومبوهموراژیک نسبتاً نادر است و عفونت ها و آسیب های جدی می توانند آن را ایجاد کنند.
مراحل رشد و اشکال انعقاد داخل عروقی منتشر شده
رویکردهای مختلفی برای طبقه بندی سندرم ترومبوهموراژیک وجود دارد: توسط علل ، ویژگی های پاتوژنز و تظاهرات بالینی.
بر اساس مکانیسم های وقوع ، مراحل زیر سندرم DIC مشخص می شود:
- - با ورود به خون ترومبوپلاستین مشخص می شود ، که باعث روند انعقاد خون و تشکیل ترومبوز می شود.
- انعقاد مصرفی - مصرف شدید فاکتورهای انعقادی ، افزایش بعدی فعالیت فیبرینولیتیک (به عنوان مکانیزم دفاعی در برابر ترومبوز عظیم) ؛
- مرحله کاهش انعقاد خون - در نتیجه مصرف اجزای سیستم انعقاد ، انعقاد پذیری و کمبود پلاکت رخ می دهد () ؛
- مرحله بهبودی

ترومبودینامیک لخته فیبرین در حالت های مختلف سیستم انعقادی - سایپرز ، باشگاه دانش
بنابراین ، هنگام قرار گرفتن در معرض یک عامل آسیب رسان ، به عنوان مثال ، آسیب یا خونریزی ، یک مکانیسم دفاعی ایجاد می شود ، اما مصرف کنترل نشده فاکتورهای انعقادی منجر به کمبود آنها و کاهش انعقاد خون اجتناب ناپذیر می شود ، که در خونریزی شدید بیان می شود. اگر بیمار خوش شانس باشد و همه کمک های واجد شرایط لازم به موقع ارائه شود ، مرحله بهبودی با ترومبوز باقیمانده آغاز می شود.
شایان ذکر است که روند ترومبوز در رگهای رگ رخ می دهد و از یک طبیعت کلی است ، بنابراین ، تمام اندام ها و بافت ها در روند پاتولوژیک نقش دارند ، که باعث ایجاد اختلالات جدی در کار آنها می شود.

طبقه بندی بالینی DIC به معنی انتخاب فرم های زیر است:
- حاد؛
- زیر حاد
- مزمن
- عود کننده
- نهفته
به اصطلاح وجود دارد سندرم ICS رعد و برق، برای چند دقیقه کافی است. این گزینه خصوصاً در زنان و زایمان معمول است.
انعقاد حاد داخل عروقی منتشر شده از چند ساعت تا چند روز طول می کشد و همراه با تروما ، سپسیس ، جراحی ، انتقال مقدار زیادی خون و اجزای آن است.
دوره تحت حاد معمول برای فرآیندهای عفونی مزمن ، بیماری های خود ایمنی (به عنوان مثال) و برای چندین هفته ادامه دارد.
مزمن یخ در بیماری های شدید قلب و عروق خونی ، ریه ها ، کلیه ها ، دیابت شیرین ممکن است. این فرم می تواند چندین سال دوام داشته باشد و در عمل درمانی مشاهده می شود. با افزایش علائم سندرم ترومبوهموراژیک ، پیشرفت بیماری ایجاد کننده آن رخ می دهد.
تظاهرات بالینی
علاوه بر این روشهای تحقیق آزمایشگاهی ، کلینیک از اهمیت بالایی در تشخیص انعقاد داخل عروقی منتشر برخوردار است. در موارد شدید ، هنگامی که ریه ها و کلیه ها تحت تأثیر قرار می گیرند ، تغییرات مشخص پوست و خونریزی ظاهر می شود ، تشخیص تردیدی نیست ، با این حال ، با اشکال حاد و مزمن دوره ، تشخیص دشوار است و نیاز به ارزیابی دقیق داده های بالینی دارد.
از آنجا که پیوند اصلی بیماری زایی در ایجاد سندرم DIC افزایش تشکیل ترومبوس در عروق ریز عروق است ، اندامهایی که شبکه مویرگی در آنها به خوبی توسعه یافته است ، رنج می برند ، اول از همه: ریه ها ، کلیه ها ، پوست ، مغز ، کبد. شدت دوره و پیش آگهی بستگی به درجه انسداد میکرو گردش خون توسط ترومبوس ها دارد.

تظاهرات پوستی انعقاد داخل عروقی منتشر شده بیشتر مورد توجه چشم غیرحرفه ای است
علائم اصلی بالینی کاملاً معمولی هستند و در اثر ترومبوز گسترده ، خونریزی و در نتیجه نارسایی اندام های مختلف ایجاد می شوند.
- چرم، به عنوان عضوی که به خوبی تأمین می شود ، همیشه در روند آسیب شناسی نقش دارد ، بثورات خونریزی دهنده مشخصه به دلیل خونریزی جزئی ، کانون نکروز (نکروز) در صورت و اندام در آن ظاهر می شود.
- شکست دادن ریه ها خود را با علائم نارسایی حاد تنفسی نشان می دهد ، علائم آن تنگی نفس شدید تا ایست تنفسی ، ادم ریوی به دلیل آسیب رساندن به عروق کوچک و آلوئول ها خواهد بود.
- وقتی فیبرین در رگهای خونی رسوب می کند کلیه نارسایی حاد کلیه ایجاد می شود ، که با اختلال در تشکیل ادرار تا آنوریا ، و همچنین تغییرات جدی الکترولیت آشکار می شود.
- شکست دادن مغز بیان شده ، منجر به اختلالات عصبی می شود.
علاوه بر تغییرات اعضای بدن ، تمایل به خونریزی خارجی و داخلی وجود دارد: رحم ، دستگاه گوارش و غیره ، و همچنین ایجاد هماتوم در اندام های داخلی و بافت های نرم.
به طور کلی ، تصویر بالینی سندرم DIC شامل علائم نارسایی چند عضو و پدیده های ترومبوهموراژیک است.
تشخیص انعقاد داخل عروقی منتشر شده
برای ایجاد تشخیص سندرم ترومبوهموراژیک ، علاوه بر علائم بالینی مشخص ، آزمایشات آزمایشگاهی ضروری است... با کمک تجزیه و تحلیل ها ، نه تنها وجود اختلالات هموستاز ، بلکه مرحله و فرم سندرم انعقاد داخل عروقی منتشر و همچنین پیگیری میزان موثر بودن درمان امکان پذیر است.
تشخیص آزمایشگاهی به اصطلاح شامل می شود آزمونهای جهت گیری، در دسترس تمام موسسات پزشکی (کوآگولوگرام) ، و پیچیده تر و دقیق تر است تایید کننده(تعیین خصوصیات تجمع پلاکت ، تحمل پلاسمای خون به هپارین و غیره).
کاهش تعداد پلاکت ها ، افزایش انعقاد و افزایش میزان فیبرینوژن در مرحله اول را می توان پیگیری کرد ، در حالی که در طی دوره انعقاد شدید مصرف ، کاهش قابل توجهی در فیبرینوژن ، ترومبوسیتوپنی شدید ، کاهش محتوای فاکتورهای انعقادی و بر این اساس ، افزایش زمان لخته شدن خون وجود دارد.
تشخیص پس از مرگ سندرم انعقاد داخل عروقی منتشر شده از طریق بررسی بافتی بافت ها ، علائم میکروسکوپی مشخصی را نشان می دهد: تجمع عناصر تشکیل شده در لومن عروق کوچک ، ترومبوز ، خونریزی های متعدد و نکروز در اندام های داخلی.
از آنجا که در اولین ساعات پیشرفت بیماری ، پارامترهای آزمایشگاهی می توانند در حد طبیعی باقی بمانند اطمینان از نظارت و کنترل مداوم تغییرات پارامترهای هموستاز مهم است، به ویژه در بیمارانی که احتمال ابتلا به DIC در آنها زیاد است. همچنین لازم است تغییرات در ترکیب الکترولیت خون ، سطح (شاخص های عملکرد کلیه) ، حالت اسید-باز ، ادرار را کنترل کنید.
رفتار
 با توجه به منشاtif چند عاملی مصرف انعقادی ، که انواع بیماری ها و شرایط پاتولوژیک را پیچیده می کند ، در حال حاضر هیچ استراتژی درمانی یکنواختی برای لخته شدن داخل عروقی وجود ندارد... با این حال ، با در نظر گرفتن مراحل و ویژگی های مشخصه دوره ، روش های اصلی پیشگیری و درمان چنین عارضه خطرناکی برجسته می شود.
با توجه به منشاtif چند عاملی مصرف انعقادی ، که انواع بیماری ها و شرایط پاتولوژیک را پیچیده می کند ، در حال حاضر هیچ استراتژی درمانی یکنواختی برای لخته شدن داخل عروقی وجود ندارد... با این حال ، با در نظر گرفتن مراحل و ویژگی های مشخصه دوره ، روش های اصلی پیشگیری و درمان چنین عارضه خطرناکی برجسته می شود.
از بین بردن فاکتور مسبب ایجاد سندرم ترومبوهموراژیک در اسرع وقت مهم است ، این امر اتیوتروپیک جهت درمان:
- آنتی بیوتیک درمانی کافی برای عوارض چرکی-سپتیک.
- جبران به موقع حجم خون در گردش در صورت از دست دادن خون ؛
- حفظ عملکرد سیستم قلبی عروقی و فشار خون در انواع مختلف شوک ؛
- پیشگیری از عوارض و مراقبت های جراحی به موقع در عمل های زایمان ؛
- تسکین درد کافی در صورت صدمات مختلف و شوک ضربه ای و غیره
دستورالعمل های اصلی بیماری زاو علامتی رفتار:
- استفاده از داروهای فیبرینولیتیک و داروهای ضد فیبرینولیتیک ، بسته به مرحله بیماری ؛
- تزریق درمانی جایگزین ؛
- بهبود خواص رئولوژیکی خون ، استفاده از داروها برای عادی سازی گردش خون
- سم زدایی خارج از بدن.
یک اصل مهم در درمان انعقاد داخل عروقی منتشر ، استفاده از درمان ضد انعقادی است.... غالباً برای این اهداف از هپارین استفاده می شود ، که لخته شدن خون را بازیابی می کند ، از تشکیل لخته های خون جلوگیری می کند و به از بین بردن موارد ایجاد شده کمک می کند ، در نتیجه عملکرد بافت ها و اندام های آسیب دیده را بهبود می بخشد.
برای از بین بردن کمبود فاکتورهای انعقاد خون ، درمان تزریق جایگزین انجام می شود. آماده سازی مطلوب برای این اهداف ، پلاسمای منجمد تازه است. همراه با آن ، شما همچنین می توانید هپارین ، مهار کننده های پروتئاز را وارد کنید (آنها فعالیت آنزیم ها را کاهش می دهند و از توسعه hypocoagulation جلوگیری می کنند ، از توسعه شوک جلوگیری می کنند - counterkal ، gordox).
برای بهبود گردش خون در بافتها ، از آسپیرین ، ترنتال ، کورانتیل و غیره و همچنین معرفی محلولهای رئولوژیکی (reopolyglucin ، voluven) استفاده کنید.
روش های سم زدایی خارج از بدن - پلاسمافرز ، سیتافرزیس ، همودیالیز در درمان پیچیده سندرم DIC بسیار مهم است.

به طور کلی ، درمان DIC کار بسیار دشواری است.، و گاهی اوقات تصمیم گیری در مورد رژیم مصرف مواد مخدر و دوزهای آنها باید در عرض چند دقیقه انجام شود.
درمان سندرم انعقاد داخل عروقی منتشر به صورت مرحله ای ضروری است ، زیرا انتصاب یک یا دارو دیگر کاملاً به وضعیت هموستاز بیمار در یک زمان خاص بستگی دارد. علاوه بر این ، باید نظارت مداوم آزمایشگاهی بر شاخص های انعقاد خون ، تعادل اسید و باز ، تعادل الکترولیت انجام شود.
مراقبت های اضطراری شامل تسکین درد ، مقابله با شوک ، ایجاد تزریق درمانی و تجویز هپارین در مرحله اول DIC است.
بیمارانی که مبتلا به سندرم ترومبوهموراژیک تشخیص داده شده اند ، یا خطر ابتلا به آن زیاد است ، باید بلافاصله در بیمارستان بستری و در بخش مراقبت های ویژه بستری شوند.
بر اساس منابع مختلف ، مرگ و میر در سندرم ترومبوهموراژیک در مرحله III به 70٪ می رسد ، در دوره مزمن - 100٪.
جلوگیری این عارضه خطرناک ، اول از همه ، در اولین درمان ممکن بیماری هایی است که منجر به وقوع آن شده است ، و همچنین در بازگرداندن گردش خون و گردش خون در اندام ها و بافت ها. فقط شروع اولیه درمان و روشهای صحیح به عادی شدن هموستاز و بهبودی بیشتر کمک می کند.
ویدئو: سخنرانی A.I. Vorobiev در DIC
دوم مرحله - انعقاد مصرفی- به "گنگ" و موذی اشاره دارد. وضعیت بیمار ، به عنوان یک قاعده ، نسبتاً مطلوب ارزیابی می شود. پارامترهای اصلی همودینامیکی (فشار خون ، نبض) نسبتاً ثابت باقی می مانند. با این حال ، رفاه خارجی با شدت واقعی آسیب شناسی در حال توسعه از طرف سیستم ایمنی بدن و سیستم هموستاتیک مطابقت ندارد. وضعیت زن باردار به تدریج یا به طور ناگهانی در حال بدتر شدن است. نارسایی جفت پیشرفت می کند. قبل از دوره حاملگی ، بلوغ زودرس جفت وجود دارد. آنتی بادی های خودکار در جفت ظاهر می شوند ، از نظر آنتی ژنی فعال می شود. علائم تهدید به خاتمه زودرس بارداری وجود دارد. ادم و پروتئین در ادرار پیشرفت کرده یا دوباره ظاهر می شود. به طور دوره ای ، در برابر فشار خون طبیعی یا کمی پایین ، فشار خون بالا ، تاکی کاردی یا برادی کاردی رخ می دهد.
در این مرحله ، فاکتورهای لخته شدن خون (فیبرینوژن ، ترومبین ، فاکتورهای VII ، V ، IX ، X ، پلاکت) برای تشکیل لخته های خون زیادی مصرف می شود ، که به دلیل تولید شدید پلاسمینوژن و آنتی ترومبین III ، لیزر ، فیبرینولیز آنزیمی و غیر آنزیمی لیز می شود.
تجزیه و تخریب همزمان بسیاری از پروتئین ها (پروتئولیز افزایش یافته) سیستم نظارتی حالت تجمع خون را بیشتر بدتر و شل می کند. تولید آنتی ترومبین III و پلاسمینوژن تخلیه می شود و سرانجام ، مرحله کاهش انعقاد خون آغاز می شود.
فعال سازی سیستم فیبرینولیتیک به همان روش سیستم انعقاد خون اتفاق می افتد: در طول مسیر داخلی ، هنگامی که یک فعال کننده بافت - پلاسمینوژن از اندوتلیوم آسیب دیده آزاد می شود - و در مسیر خارجی (فعال شدن فاکتور XII در هنگام تماس خون با یک سطح خارجی - ماتریس های فسفولیپید سلولهای آسیب دیده).
III صحنه- انعقاد خون- با از دست دادن یکی از اصلی ترین عملکردهای حیاتی آن مشخص می شود - توانایی لخته شدن خون. در خون در گردش خون ، عامل اصلی پیوند انعقادی ، فیبرینوژن (فاکتور I) ، به شدت کاهش می یابد و گاهی اوقات وجود ندارد. تعادل بین پیوندهای انعقادی ، فیبرینولیتیکی و ضد انعقادی هموستاز بهم می خورد. فیبرینولیز می تواند به 100٪ برسد.
کلینیک کاهش انعقاد خون با خونریزی گسترده (رحم ، کلیه ، روده) متمایز می شود. در صورت تشکیل لخته ، آنها به راحتی متلاشی شده ، حل می شوند. بثورات کششی و خونریزی های متعدد روی پوست ایجاد می شود. محل های تزریق ، برش ، پارگی مانند "رگ های باز" خونریزی می کند.
برخلاف خونریزی هیپوتونیک ، که غالباً دارای ویژگی موجی مانند است ، خونریزی هیپو یا آفیرینوژنمیک مداوم و گسترده است. خون خارج از رحم لخته نمی شود. خونریزی حتی از رحم منقبض نیز ادامه دارد.
خونریزی انعقادی غالباً با هیپوتونیک همراه است (از آنجا که محصولات پروتئولیز فعالیت پروتئین های انقباضی رحم را مهار می کنند). یک وضعیت جدی نه تنها به دلیل از دست دادن خون حاد ، بلکه به دلیل اثرات سمی محصولات پروتئولیز و فیبرینولیز به سرعت ایجاد می شود.
در اندام های پارانشیمی (کبد ، کلیه ، لوزالمعده) ، فرآیندهای ترومبوز و خونریزی همزمان وجود دارد.
این کلینیک با کاهش فشار خون ، تاکی کاردی ، نارسایی ریوی کلیوی ، کبدی ، کم خونی شدید مشخص می شود.
اگر این مرحله در حین جراحی رخ دهد ، خونریزی از کل سطح زخم شروع می شود و تلاش برای بستن رگ های خونریزی دهنده یا انعقاد دیاترمی آنها وضعیت را بهبود نمی بخشد. گاهی حتی "پس از خارج شدن از شکم" حتی پس از خارج شدن رحم و بستن شریان های ایلیاک داخلی نیز نمی توان چندین ساعت "از شکم خارج شد".
23.4.5. اشکال تظاهرات سندرم DIC (کامل ، حاد ، تحت حاد ، مزمن)
وجود دارد اختلافات زمانی
در پاتوژنز توسعه انعقاد داخل عروقی منتشر - سایپرز ، باشگاه دانش شدت ، بنابراین ، شدت DIC بستگی دارد از سرعتورود خون و تعداد
فعال کننده ها
هموستاز - ترومبوپلاستین بافتی و مواد مشابه. در این راستا ، سندرم انعقاد داخل عروقی منتشر شده نه تنها با مرحله بندی (مرحله به مرحله) رشد ، بلکه همچنین به صورت تظاهرات بالینی طبقه بندی می شود:
رعد و برق سریع
تیز؛
زیر حاد
مزمن
شکل رعد و برق سریع.اغلب در آسیب شناسی زنان و زایمان یافت می شود. این آمبولی ریوی یا شوک سپتیک است که با یک تصویر بالینی به سرعت در حال رشد مشخص می شود: افت فشار خون ، از بین رفتن نبض ، از دست دادن هوشیاری و اغلب ، مرگ ناگهانی. کالبد شکافی نه تنها وجود ترومبوس در ورید اجوف تحتانی را نشان می دهد ، بلکه همچنین تصویری از انعقاد داخل عروقی منتشر شده در ترکیب با دیاتوز منتشر خونریزی دهنده و بسیاری از خونریزی ها در اندام های حیاتی را نشان می دهد. اکلامپسی یک نمونه کلاسیک از شکل حاد یا کامل DIC است. این همیشه غیر منتظره است و مطابق نام خود - رعد و برق است.
عوارض نادرتر شامل ترومبوز شریان مزانتریک با نکروز بعدی حلقه های روده (پدیده "شکم حاد") است. ترومبوز ورید ساب کلاوین یا ترومبوز کاتتر وریدی بسیار شایع تر است.
به نظر می رسد شکل کامل سندرم خونریزی دهنده شامل خونریزی شدید ناگهانی در دوره بعد از زایمان متوالی است. آنها گاهی اوقات به چنان قدرت می رسند که در طی 30-40 دقیقه زن 2.5-3 لیتر خون از دست می دهد.
اقدامات متعارف برای جلوگیری از خونریزی رحم (معرفی عوامل انقباضی رحم ، ماساژ دستی ترکیبی ، گیره های دهانه رحم و غیره) تأثیری ندارد. خونریزی ادامه دارد.
تصویر بالینی شوک هموراژیک به سرعت ایجاد می شود. و فقط یک عمل فوری از بین بردن رحم ، بستن شریان های ایلیاک داخلی با تزریق همزمان تزریق می تواند زندگی یک زن را نجات دهد.
فرم حاداین بیماری با آمبولی مایع آمنیوتیک ، جدا شدن زودرس جفت ، پارگی رحم ، کوریوآمنیونیت در زایمان ، شوک از هر منشا ، از دست دادن خون گسترده ، زایمان سریع آسیب زا ایجاد می شود.
تمام مراحل (افزایش انعقاد خون ، انعقاد مصرفی) به چند دقیقه کوتاه شده و پس از آن سندرم خونریزی دهنده ایجاد می شود.
یک نمونه کلاسیک از مرحله حاد DIC PONRP جزئی یا کلی است.
فرم زیر حاداین یک نفروپاتی شدید ، پره اکلامپسی است ، در یک ویژگی متفاوت است: یک فرم تحت حاد برای مدت طولانی وجود ندارد(چند ساعت یا چند دقیقه) ، پس از آن یا به حالت مزمن تبدیل می شود ، یا به صورت حاد تحقق می یابد.
با فشار خون بالا (بحرانی ، با فشار خون 170/110 میلی متر جیوه و بالاتر) ، الیگوریا یا آنوریا ، خونریزی های اولیه (بثورات پتشیال ، استفراغ با خون ، سوزش معده ، احساس سوزش در مری) مشخص می شود. اغلب علائم عصبی وجود دارد: سردرد ، تاری دید ، درد در ناحیه اپی گاستریک ، هایپر رفلکسی. پره اکلامپسی نوعی حاد لخته شدن داخل عروقی منتشر است.
فرم مزمن(ژستوز جریان طولانی مدت ، حضور طولانی مدت جنین مرده در رحم ، بارداری با تضاد ایمنی ، FPI پیش رونده). این فرم مدت زمان زیادی طول می کشد و اصطلاحاً دوره تحت بالینی DIC است.
تشخیص بالینی این فرم به دلیل پاک شدن علائم ، ذخایر عملکردی زیاد ارگانیسم جوان و قابلیت های جبرانی و انطباقی عظیم در سن باروری (فوق جبران خسارت) همیشه امکان پذیر نیست.
انعقاد مزمن داخل عروقی منتشر می تواند هفته ها یا ماه ها ادامه داشته باشد. فعال شدن پیوندهای پلاکتی عروقی و انعقادی از مرزهای مصرف فراتر نمی رود. عواملی که برای فرآیندهای تشکیل ترومبوس داخل عروقی صرف می شود ، به طور فعال توسط کبد سنتز شده و در پلاسمای خون بازیابی می شود.
با این حال ، همانطور که یکی از مشهورترین متخصصان خون گفت ، تعادل قابل مشاهده پیوندهای سیستم هموستاز در شکل مزمن سندرم DIC حفظ نمی شود نه به عنوان "یک سرباز قلع پایدار" ، یعنی قدرت این سیستم ، بلکه به عنوان "Vanka-vstanka" (ترمیم مواد منعقد کننده از دست رفته) پروتئین ها).
در صورت پیوستن یک عامل تحریک کننده (زایمان ، استرس ، درد ، بیماری حاد ، جراحی و غیره) ، جبران خسارت اتفاق می افتد و انعقاد داخل عروقی مزمن منتشر (DIC) تحت حاد و سپس به شکل حاد تبدیل می شود ، و این یکی از نتایج معمول آن است (ترومبوز ، سندرم خونریزی دهنده) ، نارسایی ارگان ها).
بنابراین ، سندرم های اصلی بالینی انعقاد خون داخل عروقی عبارتند از:
عوارض ترومبوتیک ؛
سندرم خونریزی دهنده
اختلالات میکروسیرکولاسیون
نارسایی ارگان ها؛
کم خونی
نقض همودینامیک ، اغلب از نوع هیپوکینتیک.
خون چسبناک حاوی PDF ، RKFM , مونومرهای فیبرین ، محصولات پروتئولیز در ترکیب با کاهش توانایی گلبول های قرمز در تغییر شکل ، اختلال میکرو گردش خون عملکردهای حیاتی بافت ها و اندام ها را مختل می کند.
اختلالات میکروسیرکولاسیون که در مرحله افزایش انعقاد خون ایجاد می شوند ، نقش مهمی در تصویر بالینی اشکال مزمن و حاد DIC و عواقب آن دارند. در آینده ، آنها بیماری های سوماتیک یا عصب اعصاب و غدد را تشدید می کنند.
توسعه ref مقاوم به درمان در فشار خون شریانی ، هنگامی که کاهش فشار خون بالا و مداوم امکان پذیر نیست ، یا مقاومت در برابر دیورتیک درمانی در الیگوریا در ترکیب با آناسارکا ، همچنین می تواند با نقض میکروسیرکولاسیون همراه باشد. فقط پر کردن BCC و VCP و همچنین از بین بردن اختلالات میکرو گردش خون (روش های فعال سم زدایی خون) منجر به کاهش مقاومت و بازگرداندن عملکردهای حیاتی می شود.
سندرم DIC با اختلالات متعدد میکرو گردش خون مشخص می شود: تخریب جریان خون محیطی ، کاهش اکسیژن رسانی بافت و پرفیوژن ناکافی اندام ها و بافت ها. یک افزایش مداوم در مقاومت عروق محیطی و سپس کاهش شدید آن به دلیل ترشح خون از طریق شنت های شریانی - عروقی (متمرکز شدن جریان خون) وجود دارد.
نقض میکروسیرکولاسیون با رسوب ریز لخته ها ، ظهور هماتوم های متعدد و همچنین اختلال در عملکرد ایمنی سلولی و هومورال ، پیش نیازهای ایجاد عوارض چرکی-سپتیک (پریتونیت ، سپسیس) را ایجاد می کند. عفونت می تواند مداوم شود.
حتی اگر کنار آمدن با سندرم DIC امکان پذیر باشد ، ترمیم بافت در دوره بعد از احیا دچار اختلال می شود. همانطور که قبلاً ذکر شد ، پلاکتها هنگام فعال شدن ، ترومبوکسان را آزاد می کنند که رگهای خونی را منقبض می کند. این امر باعث ترمیم بافت می شود. بنابراین ، در بیمارانی که تحت این سندرم قرار گرفته اند ، بهبودی ضعیف بافت ها ، سطوح زخم و خم شدن زخم مشاهده می شود.
همولیز داخل عروقی گلبول های قرمز همراه با از دست دادن خون زیاد و آسیب سمی به مغز استخوان زمینه ساز سندرم کم خونی است. تجمع یک مهار کننده گلبول قرمز در خون و وجود آنتی بادی های ضد گلبول قرمز از اهمیت بیشتری برخوردار است که باعث کم خونی شدید ، مزمن و درمان آن می شود.
23.4.6. تشخیص انعقاد داخل عروقی منتشر شده
اگرچه تشخیص انعقاد داخل عروقی منتشر شده مشکل خاصی ایجاد نمی کند و به طور واضح توسط علائم بالینی و آزمایشگاهی مستند شده است ، اما تشخیص آن به تأخیر می افتد ، بیشتر در مرحله خونریزی شدید و عدم انعقاد خون.
درک شرایطی که احتمالاً ایجاد این سندرم به احتمال زیاد ممکن است لازم است.
برای پزشک بالینی ، تشخیص این سندرم موقعیتی است ، یعنی مبتنی بر دانش فرآیندهای آسیب شناختی است که به ناچار منجر به توسعه DIC می شود.
مجموعه تست های آزمایشگاهی موجود تشخیص تأیید شده را تأیید می کند و می توان شدت و مرحله توسعه DIC را مشخص کرد تا مشخص شود کدام یک از انواع آن رخ می دهد.
از میان این شاخص ها ، مهمترین موارد زیر است:
تعیین بصری تعداد زیادی از لخته های کوچک و سلولهای خونی در پلاسمای بیمار ، یک نشانه مشخص از طبقه بندی خون است.
مصرف ترومبوسیتوپنی ؛
وجود گلبول های قرمز "تکه تکه" آسیب دیده در خون ، که با میکروسکوپ اسمیر خون مشخص می شود.
تغییر در هموستازیوگرام با قابلیت انعقاد پذیری زیاد - علائم کوتاه شدن VKK و VK (کمتر از 5 دقیقه) ، APTT ، افزایش تعداد هماتوکریت (بیش از 32)) ، مقدار فیبرینوژن (بیش از 4 گرم در لیتر) ، شاخص پروترومبین (بیش از 100)) ، زمان محاسبه مجدد پلاسما (بیش از 45 ثانیه) ، زمان ترومبین (بیش از 10 ثانیه) ، وجود PDF و RCFM.
در مرحله کاهش انعقاد خون تظاهرات بالینی واضح وجود دارد: خون جاری از رحم لخته نمی شود یا شل نمی شود ، لخته هایی که به راحتی متلاشی می شوند تشکیل می شوند که در عرض 10-15 دقیقه به طور کلی به خون مایع تبدیل می شوند. همه شاخص ها نشان دهنده کاهش انعقاد خون هستند: VKK و VK طولانی تر (بیش از 10-12 دقیقه) ، افزایش فعالیت فیبرینولیتیک خون ، کاهش (کمتر از 2 گرم در لیتر) محتوای فیبرینوژن (خونریزی هیپو یا آفیرینوژنمیک) ، شاخص پروترومبین ، هموگلوبین ، تعداد هماتوکریت ، مقدار گلبول های قرمز ، فاکتورهای پلاسما IV ، VIII ، I ، II ، V ، XIII ، ATSh ، پلاسمینوژن.
برای شناسایی آزمایشگاهی و ارزیابی پویایی انعقاد داخل عروقی ، تعیین محتوای مارکرهای انعقاد داخل عروقی در پلاسمای خون از اهمیت بیشتری برخوردار است: تعیین پدیده paracoagulation و سطح پلاسما RCFM ، محصولات تبدیل فیبرینوژن به فیبرین (آزمایشات اتانول و سولفات پروتامین) ، تعیین مقدار RCFM به روش آزمون و روش های دیگر ، تعیین محتوای فیبرینوپپتید A و کمپلکس ترومبین-آنتی ترومبین در پلاسما ، ارزیابی سریع وضعیت سیستم فیبرینولیتیک توسط محتوای محصولات تخریب فیبرینوژن در پلاسما - آنزیم های D و فیبرین D-dimer.
روش های تعیین محتوای داروهای ضد انعقاد اصلی در پلاسما - پروتئین C ، پروتئین آزاد S و آنتی ترومبین III - مهم هستند ، اما پیچیده ترند. با این حال ، از آنجا که کاهش آنها برای اکثر انواع DIC معمول است ، پر کردن این داروهای ضد انعقاد باید در همه موارد DIC به صورت پیشینی انجام شود ، صرف نظر از اینکه این اجزا در پلاسمای بیمار تعیین شده باشند.
با توجه به این واقعیت که نارسایی چند اندام به طور طبیعی در سندرم DIC رخ می دهد ، یک مطالعه پویا از پارامترهای همودینامیک ، تبادل گاز ، CBS ، سطح الکترولیت خون ، کنترل ادرار ، تعیین کراتینین ، اوره ، بیلی روبین ، هموگلوبین آزاد در سرم خون ، یعنی همه آن شاخص هایی که ثبت آنها برای مدیریت بیماران "مهم" در بخش های مراقبت ویژه ضروری است.
23.4.7. درمان انعقاد داخل عروقی منتشر شده
درمان انعقاد داخل عروقی منتشر شده بسته به موارد زیر باید چند جز component باشد.
مراحل (بیش از حد ، کاهش انعقاد خون) ؛
اشکال (رعد و برق سریع ، حاد ، مزمن) ؛
ماهیت آسیب شناسی همزمان.
به منظور جلوگیری از توسعه و پیشرفت DIC ، هدف از درمان باید موارد زیر باشد:
افزایش فعالیت ضد انعقادی خون (هپارین ، ATSh ، پلاسمای منجمد تازه) ؛
بهبود فعالیت ضد پلاکت (عوامل ضد پلاکت ، ضد اسپاسم ، آنتی اکسیدان ها ، ویتامین ها) ؛
سرکوب پروتئولیز (گوردوکس ، کانتریکال ، ترسیلول) ؛
دفع سموم از بدن (عوامل سم زدایی ، پلاسمافرز).
در روند درمان سندرم DIC ، شاخص های زیر به شدت کنترل می شوند:
ادرار ساعتی
اکسیژن رسانی خون شریانی ؛
سطح پروتئین ها ، اوره ، کراتینین ؛
تعداد پلاکت ، گلبول های قرمز ، تعداد هماتوکریت ؛
مقدار فشار خون و CVP ؛
ضربان قلب؛
کواگولوگرام
در مرحله انعقاد مصرفی ، مهمترین م componentلفه درمان ترمیم همودینامیک سیستمیک است. برای این منظور ، استفاده از محلولهای نشاسته هیدروکسی اتیلات 6٪ و 10٪ 500.0-1000.0 میلی لیتر ، رئوپلی گلوسین ، پلی گلوسین ، آلبومین 5٪ ، ژلاتینول نشان داده شده است.
برای بازگرداندن نسبت مایع در بستر عروقی و فضای بین سلولی ، تزریق محلول های بلوری نیز ضروری است: محلول گلوکز 5-10٪ ، محلول کلرید سدیم ایزوتونیک ، محلول Ringer-Locke ، lactasol.
یکی از م componentsلفه های اصلی درمان تزریق تزریق در درمان انعقاد داخل عروقی منتشر شده ، معرفی سریع FFP تا 1.5-2 لیتر است. مصلحت معرفی آن به این دلیل است که پتانسیل هموستاتیک را بازیابی می کند ، پیوندهای سیستم hemostatic را متعادل می کند. این شامل بیشتر اجزای سیستم های آنزیمی پلاسما در حالت متعادل است.
برای جبران مجدد از دست دادن خون ، توده گلبول قرمز یا سوسپانسیون گلبول های قرمز شسته شده به میزان 3 حجم از دست دادن خون - 1 حجم توده گلبول قرمز تزریق می شود.
حجم تزریق تزریق درمانی باید بیش از حجم از دست دادن خون باشد (1.5-2.5 بار) ، که به دلیل موارد زیر است:
رسوب پاتولوژیک خون با DIC ؛
کاهش اولیه BCC ، VCP.
ترسیب و تخریب گلبولهای قرمز.
برای تحریک پیوند عروقی و پلاکتی هموستاز ، دیسینون ، اتامزیلات ، ترانسامچو تجویز می شود.
با از دست دادن خون گسترده ، تجویز گلوکوکورتیکواستروئیدها نشان داده شده است: هیدروکورتیزون 125-250 میلی گرم (10 میلی گرم در کیلوگرم در ساعت). پردنیزولون 400 میلی گرم (10 میلی گرم در کیلوگرم در 1 ساعت).
با فشار خون پایدار ، ضد اسپاسم تجویز می شود (آمینوفیلین 2.4 - - 5.0 میلی لیتر هر 3 ساعت).
در صورت ایجاد سندرم انعقاد داخل عروقی منتشر در برابر زمینه ژستوز ، همراه با هیپوپروتئینمی ، فعال سازی اولیه پروتئولیز ، استفاده از مهارکننده های پروتئولیز: گوردوکس ، کنتریکال ، ترازیلول ، آپروتینین ضروری است.
با هیپو ، آفیبرینوژنمی ، از انجماد به جای فیبرینوژن استفاده می شود (هر دوز حاوی 300 میلی گرم فیبرینوژن است).
با ترومبوسیتوپنی عمیق - انتقال کنسانتره پلاکت - 6-8 دوز.
در اولین ساعات پس از هموستاز جراحی بدست آمده ، استفاده از پلاسمفرز برای حذف محصولات PDP و پارا انعقاد توصیه می شود. در همان زمان ، حداقل 70٪ VCP با جایگزینی مناسب FFP برداشته می شود.
در دوره بعد از احیا ، عوارض مختلفی اغلب رخ می دهد.
در مورد افت قند خون ، محلول های گلوکز تزریق می شود. در صورت اختلال در عملکرد کبد ، محافظهای کبدی تجویز می شوند. اختلال در عملکرد کلیه نیاز به تحریک دقیق دارد. به دلیل کاهش ایمنی ، باید آنتی باکتریال و ویتامین درمانی تجویز شود. در صورت بروز مسمومیت با اندوتوکسین ، درمان سم زدایی انجام می شود. برای جلوگیری از عوارض ترومبوتیک ، از آسپرین ، هپارین و فرکمین استفاده می شود.
23.5 جنبه های پاتوفیزیولوژیک از دست دادن خون و اصول دوباره پر کردنش با خونریزی زنان و زایمان
بسته به میزان از دست دادن خون و وضعیت توانایی های محافظتی و انطباقی بدن ، انواع زیر واکنش های بدن را تشخیص می دهد:
پاسخ جبران شده
تمرکز گردش خون ؛
عدم تمرکز گردش خون.
شوک خونریزی دهنده
اصول کلی درمان تزریق - تزریق در هنگام جبران از دست دادن خون به شرح زیر است.
▲ ترمیم BCC و گردش میکرو موثر.
▲ حفظ اکسیژن کافی (در صورت ایجاد شوک تا تهویه مکانیکی).
use استفاده به موقع از هورمونهای استروئیدی (مقاومت ضد استرس) ، عوامل قلبی عروقی.
▲ رفع تخلفات:
فشار اسمزی کلوئیدی ؛
حالت اسید باز
همو انعقاد و خواص رئولوژیکی خون ؛
تعادل آب و الکترولیت.
اختلالات متابولیکی.
23.5.1 از دست دادن خون جبران شده
با از دست دادن خون 500-700 میلی لیتر ، مکانیسم های محافظ و انطباقی فعال می شوند که از همودینامیک و هموستاز پشتیبانی می کنند. از دست دادن خون باعث کاهش BCC می شود ، که اختلاف بین توده خون کل و ظرفیت بستر عروقی را تهدید می کند.
نظارت اجباری منوط به شاخص های کلینیکی عمومی مانند فشار خون ، CVP ، نبض ، رنگ و درجه حرارت پوست ، میزان تنفس ، خروج ساعتی ادرار است.
علاوه بر پارامترهای بالینی عمومی ، باید یک ثبت دقیق از دست دادن خون انجام شود ، سطح هموگلوبین ، تعداد هماتوکریت ، تعداد گلبول های قرمز و پلاکت ها ، سطح پروتئین در خون ، فیبرینوژن ، ATSh مشخص شود ، HSC و شاخص های انعقادی تعیین می شود.
اهداف اصلی اقدامات درمانی در این مرحله عبارتند از:
خونریزی را متوقف کنید
برای فراهم کردن زمان و حجم مناسب از درمان تزریق تزریق ؛
تثبیت همودینامیک ؛
کنترل خروجی ساعتی ادرار ؛
جلوگیری از ایجاد هیپوولمی.
اطمینان از حفظ بستر عروقی ، ترویج همودیلوسیون (کاهش ویسکوزیته خون ، بهبود جریان خون و گردش میکرو).
قطره داخل وریدی (60 قطره در 1 دقیقه) با معرفی یک مجموعه ویتامین انرژی انجام می شود: محلول گلوکز 10 150 150 میلی لیتر (زیر جلدی - 3 واحد انسولین) ، محلول 5 acid اسید اسکوربیک 15 میلی لیتر ، گلوکون کلسیم 10 10 10.0 میلی لیتر ، محلول 1 ATP 2.0 میلی لیتر ، کوکاربوکسیلاز 100-150 میلی گرم.
اگر خونریزی متوقف نشود ، همراه با راه حل های کریستالوئیدی و کلوئیدی به نسبت 1: 2 ، از دست دادن خون با پلاسمای منجمد تازه (300-350 میلی لیتر) جبران می شود.
کسری جبران خسارت از دست دادن خون بیش از 500 میلی لیتر مجاز نیست.
23.5.2. متمرکز شدن گردش خون
از دست دادن خون بیش از 10-15 the BCC (1000-1500 میلی لیتر) ، و در حضور پره اکلامپسی ، آسیب شناسی اولیه جسمی و غدد درون ریز ، کم خونی مزمن ، افت فشار خون (هیپوولمی ، هیپوپروتئینمی ، DIC و غیره) - 800 میلی لیتر ، شامل یک واکنش پریشانی جبرانی است تمرکز گردش خون.
مرکزیت گردش خون به دلیل تحریک و تحریک بیش از حد عملکرد قشر آدرنال ، سمپاتوآدرنال ، هیپوتالاموس هیپوفیز ، سیستم های قلبی عروقی و تنفسی است. در خون ، محتوای کاتکول آمین ها ، آدرنالین و نوراپی نفرین افزایش می یابد ، که منجر به اسپاسم عروقی عمومی می شود و مطابق با کاهش BCC منجر به کاهش ظرفیت بستر عروقی می شود. به دلیل آزاد شدن خون از انبارهای طبیعی در بستر عروقی ، جریان خون توزیع مجدد می شود. تخلیه لنفاوی در بستر وریدی انجام می شود که باعث هجوم پروتئین ها به خون می شود و فشار اسمزی کلوئیدی را افزایش می دهد.
جنبه های مثبت تمرکز گردش خون عبارتند از:
حفظ جریان خون در اندام های حیاتی (مغز ، قلب ، کبد) ؛
تحریک گردش خون و عملکردهای قلب ، کبد ، کلیه ها ، ایمنی بدن.
کاهش ویسکوزیته خون ، شستن گلبول های قرمز راکد از انبار ؛
جبران همودینامیک مرکزی و محیطی ؛
تقویت فرآیندهای ردوکس ؛
ترمیم تعادل بین ظرفیت بستر عروقی و کاهش BCC.
متمرکز شدن گردش خون منجر به تغییرات منفی می شود:
محدودیت جریان خون در کلیه ها ، مدولای فوق کلیه ، ماهیچه ها ، روده ها ، معده ، عروق مزانتریک ، لوزالمعده.
کاهش جریان خون مویرگی.
کاهش بازگشت وریدی به قلب ، کاهش خروجی قلب ؛
افزایش تدریجی هیپوکسی بافت و تجمع اسید لاکتیک (اسیدوز) ؛
انتقال به گلیکولیز بی هوازی غیر اقتصادی ، که با از دست دادن گلیکوژن و مصرف زیاد گلوکز همراه است.
نقض پیوند عروقی-پلاکتی هموستاز ؛
افزایش نفوذپذیری دیواره عروق ؛
کاهش فشار خون تورمی.
اهداف اصلی اقدامات درمانی برای تمرکز گردش خون عبارتند از:
توقف خونریزی
ارائه درمان کافی برای تزریق و تزریق
تثبیت همودینامیک ؛
عادی سازی هموستاز ؛
از بین بردن هیپوولمی.
حذف تمرکز گردش خون ؛
بهبود گردش خون میکروبی
جلوگیری از پیشرفت کاهش انعقاد خون.
23.5.3. عدم تمرکز گردش خون
با تمرکززدایی از گردش خون ، اختلاف بین حجم خون در گردش و ظرفیت بستر عروقی افزایش می یابد. سرکوب عملکرد قشر آدرنال وجود دارد. جابجایی جریان خون و تشکیل اندام های شوک (کبد ، کلیه ها و غیره) وجود دارد. به دلیل فلج مویرگ ها ، انقباض عروقی با گشاد شدن عروق جایگزین می شود ، که منجر به رسوب پاتولوژیک در سیستم عروق خازنی (رگ ها ، مویرگ ها) می شود. همزمان فاکتورهای انعقادی پلاسما (فیبرینوژن ، گلبول های قرمز ، پلاکت ها ، پروتئین ها) از بین می روند و سندرم DIC ایجاد می شود. در این حالت ، یک انباشت گلبول قرمز و پلاکت ، کاتابولیسم پروتئین ها ، لیپوپروتئین ها ، پلی ساکاریدها وجود دارد.
تنظیم مجدد اندام ها و سیستم های حیاتی مختل می شود. خونرسانی به کبد مختل می شود. عملکردهای سنتز و سم زدایی پروتئین آن کاهش می یابد. جریان خون در کلیه ها به شدت کاهش می یابد.
تظاهرات منفی عدم تمرکز گردش خون عبارتند از: کاهش BCC ، VCP ، OCE ، حجم گلبول های خون در گردش ، فشار خون (افت فشار خون) ؛ هیپوپروتئینمی ظرفیت اکسیژن خون کاهش یافته است. افزایش هیپوکسی کم خونی ؛ کاهش سرعت گردش میکرو هیپوکسی اسیدوز کمبود گلوکز انعقاد مصرفی ؛ hypocoagulation عمیق افزایش شدید نفوذ پذیری دیواره عروق ؛ بیش از حد تهویه آلکالوز تنفسی ترومبوسیتوپنی و ترومبوسیتوپاتی ؛ از دست دادن فیبرینوژن ، ATS ؛ فاکتورهای انعقادی پلاسما ؛ عدم تمرکز گردش خون. این تغییرات در ارائه زمان و حجم مناسب کمک برگشت پذیر هستند.
اهداف اصلی اقدامات درمانی برای عدم تمرکز گردش خون عبارتند از:
قطع و فوری خونریزی
از بین بردن اختلالات حاد گردش خون (افزایش فشار خون) ؛
خاتمه عدم تمرکز گردش خون.
ترمیم همودینامیک و میکروسیرکولاسیون.
بازپرداخت فوری هیپوولمی ، هیپوپروتئینمی ، از دست دادن گلبول های قرمز ، پلاکت ها ؛
جبران کسری ATS ؛
جلوگیری از کاهش انعقاد عمیق
انتقال اکسیژن بهبود یافته است.
در روند انجام درمان تزریق - تزریق ، نسبتهای زیر از مایعات تزریق شده باید رعایت شود:
کلوئیدها 1.5 لیتر
کریستالوئیدها 0.5 لیتر ؛
جرم گلبول قرمز 1.0 لیتر.
23.5.4. شوک خونریزی دهنده
با شوک هموراژیک در نتیجه از دست دادن فاجعه بار خون ، بحران میکروسیرکولاسیون و همودینامیک رخ می دهد. یک اختلال عمیق در هموستاز وجود دارد که به صورت 100٪ فیبرینولیز ، پروتئولیز ، دفیبریناسیون خون بیان می شود. در نتیجه فلج مویرگ ، رسوب خون پاتولوژیک رخ می دهد. کمبود گلبول های قرمز ، پلاکت ها ، فیبرینوژن ، آنتی ترومبین III وجود دارد. بین BCC و ظرفیت بستر عروقی اختلاف وجود دارد. همراه با درجه شدید هیپوکسی بافت و اسیدوز ، نارسایی چند عضو (نارسایی حاد تنفسی ، نارسایی حاد کلیوی و کبدی ، نارسایی حاد آدرنال و ...) ایجاد می شود. فرآیندهای برگشت ناپذیر مخرب در سطح سلولی به صورت زخم حاد و نکروز کانونی در معده ، روده ، کبد ، کلیه ها ، پانکراس تشکیل می شود. خرابی مکانیسم های محافظتی و انطباقی وجود دارد.
اختلالات رخ داده از نظر بالینی با کاهش فشار خون ، کاهش CVP کمتر از 6 میلی متر آب آشکار می شود. هنر ، نبض مانند نخ ، تاکی پنه ، آنوریا ، سیانوز ، گیجی.
اهداف اصلی درمان شوک خونریزی دهنده عبارتند از:
تثبیت سریع همودینامیک و ترمیم میکرو گردش خون.
از بین بردن هیپوولمی.
افزایش حجم دقیقه قلب؛
انحلال موتورهای احتراق داخلی ؛
ترمیم BCC ، VCP ، حجم گلبول های قرمز در گردش و تعادل الکترولیت ها.
اطمینان از ادرار کافی.
23.5.5. اصول کلی درمان تزریق - انتقال خون
در روند انجام درمان تزریق تزریق ، قوانین زیر باید دنبال شود.
1. هنگام پر کردن BCC و از بین بردن هیپوولمی ، لازم است که نسبت کمی محیط تزریق ، میزان حجمی و مدت زمان انتقال را در نظر گرفت. برای انجام موفقیت آمیز درمان تزریق - تزریق ، باید از نظر میزان رفتار ، حجم و کیفیت محیط استفاده شده کافی باشد.
2. داروهای مورد استفاده اولیه برای خونریزی زنان و زایمان محلول های نشاسته هیدروکسی اتیل شده 6-10 هستند که دارای خواص زیر هستند:
توزیع وزن مولکولی بهینه داشته باشید.
مولکول های دارویی منافذ مویرگ ها را می بندند.
بازگرداندن شاخص های اصلی کلان و میکرودینامیک ؛
بهبود خواص رئولوژیکی خون ؛
عملکرد مانع دیواره رگ های خونی را بازیابی کنید.
جلوگیری از از دست دادن آلبومین.
جلوگیری و اصلاح سندرم DIC.
ادم ریوی ؛
وخیم شدن میوکارد ؛
ایجاد ادم بافتی
5- هیچ نشانه ای برای انتقال خون اهدا کننده کامل کنسرو شده وجود ندارد ، مگر در مواردی که از دست دادن خون گسترده حاد است و هیچ جایگزین خون وجود ندارد. خون اهدایی آلوژنیک پیوند است. سازگاری بدون توجه به سازگاری بافتی تعیین می شود ، که باعث عوارض انتقال خون می شود. وجه دیگر این مسئله ، خطر بالای عفونت در هنگام انتقال خون است (هپاتیت ویروسی ، ایدز). علاوه بر این ، خواص عملکردی خون حفظ شده زیاد نیست. در طی 2 روز اول ذخیره سازی ، لکوسیت ها و پلاکت ها در آن می میرند. در روز 3-4 ام ، عملکرد انتقال گاز به شدت کاهش می یابد و میل به اکسیژن در گلبول های قرمز تقریباً به نصف کاهش می یابد. در حین ذخیره سازی ، فرآورده های متابولیسم گلبول قرمز در خون حفظ شده تجمع می یابد و همولیز جزئی رخ می دهد.
در این راستا بیشتر توصیه می شود از اجزای خون استفاده شود.
معرفی توده گلبول قرمز (با ماندگاری بیش از 3 روز) با از دست دادن خون 25-30 of از BCC (1500 میلی لیتر یا بیشتر) ، کاهش سطح هموگلوبین زیر 70-80 گرم در لیتر و تعداد هماتوکریت زیر 25 indicated نشان داده شده است.
مقدار تزریق گلبول قرمز متناسب با حجم از دست دادن خون افزایش می یابد:
2000 میلی لیتر - 750 میلی لیتر
2500 میلی لیتر - 1250 میلی لیتر
3000 میلی لیتر و بیشتر - 1500 میلی لیتر.
6. حداکثر دوزهای مجاز داروها بر اساس دکستران 800.0-1000.0 میلی لیتر است. با دوزهای زیاد نمی توان به گردش عادی گردش خون و اکسیژن رسانی دست یافت.
The- نسبت محلولهای کلوئیدی و کریستالوئیدی با از دست دادن خون 800-1000 باید 1: 1 و با از دست دادن خون 5/2 - 2 لیتر ، -2: 1 باشد. هرچه از دست دادن خون بیشتر باشد ، میزان کریستالوئید کمتری تزریق می شود.
8- اگر طی 1-2 ساعت اول 70٪ از حجم خون از دست رفته دوباره پر شود ، باید امیدوار بود که نتیجه مطلوبی داشته باشید. در دوره درمان ، معیارهای تأثیر درمان ، رنگ پوست و درجه حرارت ، نبض ، فشار خون ، CVP ، خروج ساعتی ادرار ، هماتوکریت ، CBS خون است.
سندرم DIC یا سندرم انعقاد داخل عروقی منتشر ، یک فرایند آسیب شناختی چند جزئی پیچیده در سیستم hemostatic است ، افزایش تشکیل ترومبوس در عروق ریز عروق.
این وضعیت اغلب در عمل پزشکان از هر تخصصی رخ می دهد ، متخصصان زنان و زایمان ، احیاگران ، جراحان ، پزشکان اورژانس با آن روبرو می شوند. همچنین رایج ترین شکل اختلالات لخته شدن خون (انعقاد خون) در مراقبت های ویژه در بزرگسالان و کودکان است.
انعقاد خون وضعیتی است که همراه با تغییر در انعقاد خون است. انواع اصلی انعقاد خون ، مادرزادی (ژنتیکی) و اکتسابی است که یکی از انواع آن ، انعقاد داخل عروقی منتشر است. در ادبیات ، می توان داده هایی را در مورد به اصطلاح انعقاد انعقاد خون یا سندرم ابر انعقاد پذیر پیدا کرد که با علائم آزمایشگاهی افزایش انعقاد خون مشخص می شود ، اما ترومبوز غالباً وجود ندارد.
سندرم DIC دارای مکانیسم های پیچیده ای از تکامل ، تظاهرات مختلف بالینی است و معیارهای تشخیصی دقیق آن هنوز مشخص نشده است ، که باعث ایجاد مشکلات قابل توجهی در تشخیص و درمان آن می شود. این وضعیت همیشه هر بیماری دیگری را پیچیده می کند ، بنابراین یک بیماری مستقل نیست.
ترومبوز: طبیعی یا پاتولوژیک؟
برای اینکه بفهمید دلیل چیست و مکانیسم های بروز چنین اختلالی مانند انعقاد داخل عروقی منتشر چیست ، باید مراحل اصلی انعقاد خون را بدانید.
فرد به طور مداوم با خطر صدمات احتمالی ، از خراش های جزئی یا بریدگی تا آسیب های جدی روبرو می شود ، بنابراین ، طبیعت مکانیسم محافظتی خاصی را ایجاد می کند - ترومبوز ، یعنی تشکیل لخته خون در محل آسیب رساندن به رگ.
در سیستم دو سیستم مخالف وجود دارد - منعقد کننده و پادبند ، تعامل صحیح آن در صورت لزوم به تشکیل ترومب کمک می کند ، و همچنین حالت مایع خون در عروق در صورت عدم آسیب. این سیستم های هموستاتیک نقش محافظتی بسیار مهمی دارند.

تشکیل ترومبوس
در صورت نقض یکپارچگی دیواره عروق ، سیستم انعقاد فعال می شود ، یک مجموعه واکنش کامل منجر به تشکیل ترومبوس (لخته در لومن عروق یا اتاق قلب) می شود. پروتئین های پلاسما ، به ویژه فیبرینوژن ، و همچنین پلاکت ها ، عوامل لخته کننده تولید شده در کبد و آنزیم های مختلف به طور مستقیم در این امر دخیل هستند. نتیجه تشکیل لخته خون است که نقص دیواره عروق را می پوشاند و از خونریزی بیشتر جلوگیری می کند.
برای حفظ حالت مایع خون و جلوگیری از تشکیل کنترل نشده لخته های خون ، موارد خاص وجود دارد مکانیسم های ضد ترومبوتیکاجرا شده توسط عمل به اصطلاح ضدانعقاد - موادی که از بروز ترومبوز عظیم جلوگیری می کنند (پروتئین های پلاسما ، آنزیم های پروتئولیتیک ، هپارین درون زا). علاوه بر این ، با جریان سریع خون و به اصطلاح فیبرینولیز ، یعنی انحلال پروتئین فیبرین و خارج شدن آن از بستر عروقی با استفاده از آنزیم های گردش یافته در پلاسمای خون و ترشح شده توسط لکوسیت ها ، پلاکت ها و سلول های دیگر ، از بروز ترومبوز جلوگیری می شود. بقایای فیبرین پس از تخریب توسط لکوسیت ها و ماکروفاژها جذب می شود.
هنگامی که تعامل اجزای سیستم هموستاز در بیماری ها و آسیب های مختلف تغییر می کند ، در کار سیستم های انعقادی و ضد انعقاد خون ناهماهنگی وجود دارد، که به ترومبوز گسترده کنترل نشده همراه با خونریزی کمک می کند. این مکانیسم ها اساس پاتوژنز DIC را تشکیل می دهند ، که یک عارضه تهدید کننده زندگی است.
علل انعقاد داخل عروقی منتشر شده
از آنجا که DIC یک بیماری مستقل نیست ، بدون هیچ تاثیری که سیستم انعقادی را فعال کند ایجاد نمی شود. شایع ترین علل وقوع آن:
- عفونت ها - سپسیس ، شوک سپتیک ، ضایعات شدید باکتریایی و ویروسی ؛
- انواع مختلف شوک (آسیب زا ، سمی عفونی ، هیپوولمیک و غیره) ، شرایط ترمینال ؛
- آسیب ها ، از جمله مداخلات جراحی آسیب زا (پیوند اعضا ، پروتز دریچه های قلب) ، استفاده از دستگاه های قلب و ریه و همودیالیز در حین مداخلات جراحی.
- بیماری های انکولوژیک ، به ویژه سرطان خون و اشکال رایج سرطان ؛
- سندرم DIC در زنان و زایمان - خونریزی گسترده ، جدا شدن زودرس جفت ، آمبولی مایع آمنیوتیک ؛
- در دوران بارداری در صورت سمیت دیررس (اکلامپسی ، پره اکلامپسی) ، درگیری Rh بین مادر و جنین ، حاملگی خارج رحمی و غیره.
- بیماری های شدید سیستم قلبی عروقی ، فرآیندهای چرکی-التهابی اندام های داخلی.
به این ترتیب سندرم DIC در بیشتر بیماری های جدی و شرایط ترمیم همراه است (مرگ بالینی ، اقدامات احیای بعدی). در مرحله ایجاد حضور آنها ، انعقاد خون یا از قبل وجود دارد ، یا اگر اقدامات پیشگیرانه مناسبی انجام نشود ، ایجاد می شود.
DIC در نوزادان تازه متولد شده ای که سالم و به موقع به دنیا می آیند بسیار نادر است. بیشتر اوقات با هیپوکسی شدید ، ضربه به هنگام تولد ، آمبولی مایع آمنیوتیک اتفاق می افتد (در این حالت مادر و جنین علائم آن را دارند) ، اختلالات تنفسی.
در کودکان ، انعقاد ارثی ، به ویژه هموفیلی و بیماری فون ویلبراند ، همراه با افزایش خونریزی امکان پذیر است ، در حالی که سندرم ترومبوهموراژیک نسبتاً نادر است و علل آن می تواند عفونت های شدید و ضربه باشد.
مراحل رشد و اشکال انعقاد داخل عروقی منتشر شده
رویکردهای مختلفی برای طبقه بندی سندرم ترومبوهموراژیک وجود دارد: توسط علل ، ویژگی های پاتوژنز و تظاهرات بالینی.
بر اساس مکانیسم های وقوع ، مراحل زیر سندرم DIC مشخص می شود:
- افزایش انعقاد خون - با ورود به خون ترومبوپلاستین مشخص می شود ، که روند انعقاد خون و تشکیل ترومبوس را تحریک می کند.
- انعقاد مصرفی - مصرف شدید فاکتورهای انعقادی ، افزایش بعدی فعالیت فیبرینولیتیک (به عنوان مکانیزم دفاعی در برابر ترومبوز عظیم) ؛
- مرحله کاهش انعقاد خون - در نتیجه هزینه اجزای سیستم انعقاد ، انعقاد پذیری و کمبود پلاکت (ترومبوسیتوپنی) رخ می دهد.
- مرحله بهبودی
بنابراین ، هنگامی که در معرض یک عامل آسیب رسان قرار می گیرید ، به عنوان مثال ، آسیب یا خونریزی ، یک مکانیسم محافظتی ایجاد می شود - ترومبوز ، اما مصرف کنترل نشده فاکتورهای انعقادی منجر به کمبود آنها و کاهش انعقاد خون اجتناب ناپذیر می شود که در خونریزی شدید بیان می شود. اگر بیمار خوش شانس باشد و همه کمک های واجد شرایط لازم به موقع ارائه شود ، مرحله بهبودی با ترومبوز باقیمانده آغاز می شود.
شایان ذکر است که روند ترومبوز در رگهای رگ رخ می دهد و از یک طبیعت کلی است ، بنابراین ، تمام اندام ها و بافت ها در روند پاتولوژیک نقش دارند ، که باعث ایجاد اختلالات جدی در کار آنها می شود.

عوامل آغازین و پیوندهای اصلی در پاتوژنز انعقاد داخل عروقی منتشر شده
طبقه بندی بالینی DIC به معنی انتخاب فرم های زیر است:
- حاد؛
- زیر حاد
- مزمن
- عود کننده
- نهفته
به اصطلاح وجود دارد سندرم ICS رعد و برق، برای چند دقیقه کافی است. این گزینه خصوصاً در زنان و زایمان معمول است.
انعقاد حاد داخل عروقی منتشر شده از چند ساعت تا چند روز طول می کشد و همراه با تروما ، سپسیس ، جراحی ، انتقال مقدار زیادی خون و اجزای آن است.
دوره تحت حاد ویژگی فرآیندهای عفونی مزمن ، بیماری های خود ایمنی (به عنوان مثال ، لوپوس اریتماتوز سیستمیک) و چندین هفته طول می کشد.
مزمن یخ در بیماری های شدید قلب و عروق خونی ، ریه ها ، کلیه ها ، دیابت شیرین ممکن است. این فرم می تواند چندین سال دوام داشته باشد و در عمل درمانی مشاهده می شود. با افزایش علائم سندرم ترومبوهموراژیک ، پیشرفت بیماری ایجاد کننده آن رخ می دهد.
تظاهرات بالینی
علاوه بر این روشهای تحقیق آزمایشگاهی ، کلینیک از اهمیت بالایی در تشخیص انعقاد داخل عروقی منتشر برخوردار است. در موارد شدید ، هنگامی که ریه ها و کلیه ها تحت تأثیر قرار می گیرند ، تغییرات مشخص پوست و خونریزی ظاهر می شود ، تشخیص تردیدی نیست ، با این حال ، با اشکال حاد و مزمن دوره ، تشخیص دشوار است و نیاز به ارزیابی دقیق داده های بالینی دارد.
از آنجا که پیوند اصلی بیماری زایی در ایجاد سندرم DIC افزایش تشکیل ترومبوس در عروق ریز عروق است ، اندامهایی که شبکه مویرگی در آنها به خوبی توسعه یافته است ، رنج می برند ، اول از همه: ریه ها ، کلیه ها ، پوست ، مغز ، کبد. شدت دوره و پیش آگهی بستگی به درجه انسداد میکرو گردش خون توسط ترومبوس ها دارد.

تظاهرات پوستی انعقاد داخل عروقی منتشر شده بیشتر مورد توجه چشم غیرحرفه ای است
علائم اصلی بالینی کاملاً معمولی هستند و در اثر ترومبوز گسترده ، خونریزی و در نتیجه نارسایی اندام های مختلف ایجاد می شوند.
- چرم، به عنوان عضوی که به خوبی تأمین می شود ، همیشه در روند آسیب شناسی نقش دارد ، بثورات خونریزی دهنده مشخصه به دلیل خونریزی جزئی ، کانون نکروز (نکروز) در صورت و اندام در آن ظاهر می شود.
- شکست دادن ریه ها خود را با علائم نارسایی حاد تنفسی نشان می دهد ، علائم آن تنگی نفس شدید تا ایست تنفسی ، ادم ریوی به دلیل آسیب رساندن به عروق کوچک و آلوئول ها خواهد بود.
- وقتی فیبرین در رگهای خونی رسوب می کند کلیه نارسایی حاد کلیه ایجاد می شود ، که با اختلال در تشکیل ادرار تا آنوریا ، و همچنین تغییرات جدی الکترولیت آشکار می شود.
- شکست دادن مغز بیان شده در خونریزی ، منجر به اختلالات عصبی می شود.
علاوه بر تغییرات اعضای بدن ، تمایل به خونریزی خارجی و داخلی وجود دارد: بینی ، رحم ، دستگاه گوارش و غیره ، و همچنین ایجاد هماتوم در اندام های داخلی و بافت های نرم.
به طور کلی ، تصویر بالینی سندرم DIC شامل علائم نارسایی چند عضو و پدیده های ترومبوهموراژیک است.
تشخیص انعقاد داخل عروقی منتشر شده
برای ایجاد تشخیص سندرم ترومبوهموراژیک ، علاوه بر علائم بالینی مشخص ، آزمایشات آزمایشگاهی ضروری است... با کمک تجزیه و تحلیل ها ، نه تنها وجود اختلالات هموستاز ، بلکه مرحله و فرم سندرم انعقاد داخل عروقی منتشر و همچنین پیگیری میزان موثر بودن درمان امکان پذیر است.
تشخیص آزمایشگاهی به اصطلاح شامل می شود آزمونهای جهت گیری، در دسترس تمام موسسات پزشکی (کوآگولوگرام) ، و پیچیده تر و دقیق تر است تایید کننده(تعیین خصوصیات تجمع پلاکت ، تحمل پلاسمای خون به هپارین و غیره).
در انعقاد ، کاهش تعداد پلاکت ها ، افزایش انعقاد و افزایش میزان فیبرینوژن در مرحله اول قابل ردیابی است ، در حالی که در طول دوره انعقاد شدید مصرف ، کاهش قابل توجهی در فیبرینوژن ، ترومبوسیتوپنی شدید ، کاهش محتوای فاکتورهای انعقادی و ، بر این اساس ، افزایش زمان لخته شدن خون وجود دارد.
تشخیص پس از مرگ سندرم انعقاد داخل عروقی منتشر شده از طریق بررسی بافتی بافت ها ، علائم میکروسکوپی مشخصی را نشان می دهد: تجمع عناصر تشکیل شده در لومن عروق کوچک ، ترومبوز ، خونریزی های متعدد و نکروز در اندام های داخلی.
از آنجا که در اولین ساعات پیشرفت بیماری ، پارامترهای آزمایشگاهی می توانند در حد طبیعی باقی بمانند اطمینان از نظارت و کنترل مداوم تغییرات پارامترهای هموستاز مهم است، به ویژه در بیمارانی که در معرض خطر بالای انعقاد داخل عروقی منتشر هستند. همچنین لازم است تغییرات در ترکیب الکترولیت خون ، میزان اوره ، کراتینین (شاخص های عملکرد کلیه) ، حالت اسید-باز و ادرار کنترل شود.
رفتار
با توجه به منشاtif چند عاملی مصرف انعقادی ، که انواع بیماری ها و شرایط پاتولوژیک را پیچیده می کند ، در حال حاضر هیچ استراتژی درمانی یکنواختی برای لخته شدن داخل عروقی وجود ندارد... با این حال ، با در نظر گرفتن مراحل و ویژگی های مشخصه دوره ، روش های اصلی پیشگیری و درمان چنین عارضه خطرناکی برجسته می شود.
از بین بردن فاکتور مسبب ایجاد سندرم ترومبوهموراژیک در اسرع وقت مهم است ، این امر اتیوتروپیک جهت درمان:
- آنتی بیوتیک درمانی کافی برای عوارض چرکی-سپتیک.
- جبران به موقع حجم خون در گردش در صورت از دست دادن خون ؛
- حفظ عملکرد سیستم قلبی عروقی و فشار خون در انواع مختلف شوک ؛
- پیشگیری از عوارض و مراقبت های جراحی به موقع در عمل های زایمان ؛
- تسکین درد کافی در صورت صدمات مختلف و شوک ضربه ای و غیره
دستورالعمل های اصلی بیماری زاو علامتی رفتار:
- ضد انعقاد درمانی ؛
- استفاده از داروهای فیبرینولیتیک و داروهای ضد فیبرینولیتیک ، بسته به مرحله بیماری ؛
- تزریق درمانی جایگزین ؛
- بهبود خواص رئولوژیکی خون ، استفاده از داروها برای عادی سازی گردش خون
- سم زدایی خارج از بدن.
یک اصل مهم در درمان انعقاد داخل عروقی منتشر ، استفاده از درمان ضد انعقادی است.... غالباً برای این اهداف از هپارین استفاده می شود ، که لخته شدن خون را بازیابی می کند ، از تشکیل لخته های خون جلوگیری می کند و به از بین بردن موارد ایجاد شده کمک می کند ، در نتیجه عملکرد بافت ها و اندام های آسیب دیده را بهبود می بخشد.
برای از بین بردن کمبود فاکتورهای انعقاد خون ، درمان تزریق جایگزین انجام می شود. آماده سازی مطلوب برای این اهداف ، پلاسمای منجمد تازه است. همراه با آن ، شما همچنین می توانید هپارین ، مهار کننده های پروتئاز را وارد کنید (آنها فعالیت آنزیم ها را کاهش می دهند و از توسعه hypocoagulation جلوگیری می کنند ، از توسعه شوک جلوگیری می کنند - counterkal ، gordox).
برای بهبود گردش خون در بافتها ، از آسپیرین ، ترنتال ، کورانتیل و غیره و همچنین معرفی محلولهای رئولوژیکی (reopolyglucin ، voluven) استفاده کنید.
روش های سم زدایی خارج از بدن - پلاسمافرز ، سیتافرزیس ، همودیالیز در درمان پیچیده سندرم DIC بسیار مهم است.

به طور کلی ، درمان DIC کار بسیار دشواری است.، و گاهی اوقات تصمیم گیری در مورد رژیم مصرف مواد مخدر و دوزهای آنها باید در عرض چند دقیقه انجام شود.
درمان سندرم انعقاد داخل عروقی منتشر به صورت مرحله ای ضروری است ، زیرا انتصاب یک یا دارو دیگر کاملاً به وضعیت هموستاز بیمار در یک زمان خاص بستگی دارد. علاوه بر این ، باید نظارت مداوم آزمایشگاهی بر شاخص های انعقاد خون ، تعادل اسید و باز ، تعادل الکترولیت انجام شود.
مراقبت های اضطراری شامل تسکین درد ، مقابله با شوک ، ایجاد تزریق درمانی و تجویز هپارین در مرحله اول DIC است.
بیمارانی که مبتلا به سندرم ترومبوهموراژیک تشخیص داده شده اند ، یا خطر ابتلا به آن زیاد است ، باید بلافاصله در بیمارستان بستری و در بخش مراقبت های ویژه بستری شوند.
طبق منابع مختلف ، مرگ و میر در سندرم ترومبوهموراژیک در مرحله III به 70٪ می رسد ، در دوره مزمن - 100٪.
جلوگیری این عارضه خطرناک ، اول از همه ، در اولین درمان ممکن بیماری هایی است که منجر به وقوع آن شده است ، و همچنین در بازگرداندن گردش خون و گردش خون در اندام ها و بافت ها. فقط شروع اولیه درمان و روشهای صحیح به عادی شدن هموستاز و بهبودی بیشتر کمک می کند.
انعقاد مصرف K. ، به دلیل کاهش شدید سطح خون در فاکتورهای I ، II ، V ، VII ، VIII ، XIII و تعداد پلاکت ها ، ناشی از از دست دادن خون گسترده ، با شوک ، بیماری سوختگی ، همولیز داخل عروقی و برخی شرایط دیگر
فرهنگ لغت پزشکی بزرگ. 2000 .
ببینید "انعقاد مصرفی" در دیکشنری های دیگر چیست:
قبل از حذف PLACENTAL - عسل. جدا شدن زودرس جفت جدا شدن جفت واقع شده از دیواره رحم قبل از تولد کودک است. علامت اصلی خونریزی است. خونریزی خارجی هنگامی اتفاق می افتد که قسمت محیطی جفت جدا شود. خون می ریزد ... ... کتاب راهنمای بیماری ها
- (انتشار انعقاد داخل عروقی) ICD 10 D65.65. ICD 9 286.6286.6 DiseasesDB ... ویکی پدیا
سندرم DIC (انعقاد داخل عروقی منتشر) ICD 10 D65. ICD 9 286.6 DiseasesDB ... ویکی پدیا
- (کم خونی ؛ پیشوند منفی یونانی + خون haima ؛ مترادف کم خونی) کاهش میزان هموگلوبین در خون ، که معمولاً با گلبول قرمز همراه است. الف - یک بیماری پاتولوژیک رایج که بیشتر اوقات به صورت سندرم رخ می دهد ... ... دائرlopالمعارف پزشکی
شوک تروما یک بیمار جدی ، تهدید کننده زندگی است ، یک بیماری پاتولوژیک ناشی از آسیب های شدید ، مانند شکستگی استخوان های لگن ، زخم های شدید ناشی از گلوله ، آسیب مغزی آسیب دیده ، آسیب شکمی با آسیب ...
شوک تروماتیک یک وضعیت پاتولوژیک شدید و تهدید کننده زندگی است که در طی آسیب های شدید ، عمل جراحی ، از دست دادن خون زیاد اتفاق می افتد. از نظر پاتوژنز ، شوک آسیب زا مربوط به شوک هیپوولمیک است. مطالب 1 علت و مکانیسم ... ... ویکی پدیا
من فروپاشی (به ضعف Collapsus ضعیف ، افتاده) نارسایی حاد عروقی ، که در درجه اول با افت در تن عروق و همچنین در حجم خون در گردش مشخص می شود. در همان زمان ، جریان خون وریدی به قلب کاهش می یابد ، کاهش می یابد ... ... دائرlopالمعارف پزشکی
ماده فعال ›› فاکتور لخته شدن خون IX (عامل ضد هموفیلی IX) نام لاتین Bebulin TIM 4 ATC: ›› B02BD04 فاکتور لخته شدن خون IX گروه دارویی: مواد منعقد کننده (از جمله فاکتورهای لخته شدن خون) ، خونریزی ... ... فرهنگ لغت داروها
سندرم انعقاد داخل عروقی منتشر با تشکیل گسترده لخته های خون کوچک (فیبرین ، اریتروسیت ، هیالین) در رگ عروق کل ارگانیسم همراه با عدم انعقاد خون ، منجر به خونریزی های گسترده متعدد می شود. این یک عارضه جدی و اغلب کشنده از بیماری های متعدد است و نیاز به تشخیص و درمان به موقع دارد. این بر اساس عدم هماهنگی عملکرد سیستم های انعقاد خون و ضد انعقاد خون است که مسئول هموستاز هستند.
در بسیاری از موارد ، علت انعقاد منتشر داخل عروقی ناشناخته است. شایعترین دلایل DIC:
بیماری های عفونی:
باکتریمی گرم منفی و گرم مثبت
سپسیس مننگوکوک
انتشار عفونت قارچی
ریکتزیوز
ویرمی شدید (به عنوان مثال تب خونریزی دهنده)
مالاریای پلاسمودیوم فالسیپاروم
عفونت های نوزادی یا داخل رحمی
بیماری های زنان:
آمبولی مایع آمنیوتیک
مرگ داخل رحمی جنین
قطع جفت
بیماری های کبدی:
نکروز گسترده کبدی
سیروز کبدی
تومورهای بدخیم
سرطان خون حاد پرومیلوسیتیک
متاستاز سرطان ، معمولاً آدنوکارسینوماها
بیماری های دیگر
واسکولیت عروق کوچک (به عنوان مثال ، با ایجاد سیتوتوکسیک و ایمونوکامپلکس (II و III) انواع حساسیت بیش از حد)
ترومای گسترده
تب
گرمازدگی
جراحی بای پس قلبی - ریوی
گزش مار
شوک شدید
همولیز داخل عروقی
لخته شدن خون بیشمار در رگهای رگ در سندرم DIC منجر به اختلال در پرفیوژن بافت با تجمع اسید لاکتیک در آنها و ایجاد ایسکمی و همچنین تشکیل ریز انقباض در تعداد زیادی از اندام ها می شود. لخته شدن خون به ویژه در ریز رگ ها ، کلیه ها ، کبد ، غدد فوق کلیوی ، غده هیپوفیز ، مغز ، دستگاه گوارش ، پوست و همراه با خونریزی های متعدد ، دیستروفی و \u200b\u200bنکروز اندام ها و بافت ها (نکروز قشر کلیه ، نکروز و خونریزی در ریه ها ، مغز) و غیره.). لازم است بدانید که در برخی موارد در هنگام کالبد شکافی ، به دلیل عملکرد موازی و غالب سیستم فیبرینولیتیک ، ممکن است میکروتروب ها شناسایی نشوند (اصطلاحاً فیبرینولیز).
لازم به ذکر است که ترومبوز منتشر نیز با ایجاد انعقاد مصرف منجر به مصرف فاکتورهای انعقادی خون می شود. در این حالت ، ترومبوسیتوپنی مشاهده می شود ، که همراه با کاهش فیبرینوژن و سایر عوامل انعقادی ، منجر به ایجاد خونریزی پاتولوژیک می شود. این تمایل به خونریزی با فعال شدن بیش از حد سیستم فیبرینولیتیک (فعال شدن فاکتور XII هاگمن که باعث انعقاد داخلی خون می شود و منجر به تبدیل پلاسمینوژن به پلاسمین می شود) تشدید می شود. محصولات تخریب فیبرین ، ناشی از عملکرد پلاسمین بر فیبرین ، همچنین دارای خواص ضد انعقادی هستند و خونریزی را بیشتر می کنند.
شکل: 2. علل و مکانیسم های توسعه انعقاد داخل عروقی منتشر شده
تفاوت اصلی بین انعقاد داخل عروقی منتشر و ترومبوز موضعی این است که با انعقاد داخل عروقی منتشر تعمیم یافتههم سیستم انعقادی و هم سیستم فیبرینولیز فعال می شوند و با ترومبوز این تغییرات فقط مشاهده می شود به صورت محلی
در بعضی موارد ، با سندرم DIC ، ترومبوز غالب است ، که منجر به ایسکمی بافتی می شود ، در موارد دیگر ، فیبرینولیز ، که منجر به ظهور خونریزی می شود.
مقدار
نارسایی حاد چند عضو ایجاد می شود ، که باعث مرگ بیماران می شود.
پیش بینی
با به موقع بودن تشخیص و شروع درمان تعیین می شود ، که شامل معرفی هپارین برای جلوگیری از تشکیل لخته های خون و معرفی پلاکت و پلاسما برای بازگرداندن فاکتورهای انعقادی مصرف شده است. نظارت بر سطح تجزیه فیبرین ، تعداد فیبرینوژن و پلاکت برای تشخیص و نظارت بر اثربخشی درمان استفاده می شود.