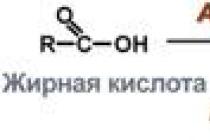
آنزیم های ردوکس که انتقال الکترون و فسفوریلاسیون اکسیداتیو را کاتالیز می کنند در لایه لیپیدی غشای میتوکندری داخلی سلول ها قرار دارند.
انتقال الکترون به اکسیژن در میتوکندری (شکل 13.3) در چندین مرحله اتفاق می افتد و زنجیره ای از حامل های الکترون است که در آن با نزدیک شدن اکسیژن ، پتانسیل اکسایش کاهش می یابد (به ترتیب ، پتانسیل کاهش نیز کاهش می یابد). این سیستم های حمل و نقل نامگذاری شده اند زنجیرهای تنفسی
شکل: 13.3
بیشتر جفت الکترون ها به دلیل عملکرد آنزیم ها (دهیدروژنازها) که از کوآنزیم های NAD + و NADP + به عنوان گیرنده الکترون استفاده می کنند ، وارد زنجیره تنفسی می شوند. به کل این گروه از آنزیم ها دهیدروژناز وابسته به NaAO (P) گفته می شود.
کوآنزیم های NAD + (نیکوتین آمید آدنین دینوکلئوتید) ، FAD و FMN (فلاوین آدنین دینوکلئوتید و فلاوین مونونوکلئوتید) ، کوآنزیم Q (CoQ) ، خانواده ای از پروتئین های حاوی هم - سیتوکروم ها (به عنوان سیتوکروم های b ، Q ، C ، A ، A3 تعیین شده) آهن غیر هِم هستند بردارهای میانی در زنجیره تنفسی در موجودات بالاتر. این فرآیند با انتقال پروتون ها و الکترون ها از بستر اکسید شده به کوآنزیم های NAD + یا FAD و تشکیل NADH و FADH2 آغاز می شود.
حرکت بعدی الکترونها از NADH و FADH 2 به سمت اکسیژن را می توان به لغزش به سمت پله ای تشریح کرد که مراحل آن حامل های الکترون هستند. با هر مرحله ، بخشی از انرژی آزاد از مرحله به مرحله آزاد می شود (شکل 13.3 را ببینید).
سه مجتمع پروتئینی (I ، III ، IV) و دو مولکول حامل متحرک: یوبی کوینون (کوآنزیم Q) و سیتوکروم C در انتقال الکترون از بسترهای آلی به اکسیژن مولکولی نقش دارند.

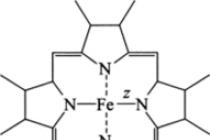
شکل: 13.4ساختار مولکول Heme ، z \u003d 2* یا 3+
سوسینات دهیدروژناز ، که متعلق به خود چرخه کربس است ، همچنین می تواند به عنوان پیچیده II زنجیره تنفسی در نظر گرفته شود.
مجتمع های زنجیره ای تنفسی از انواع پلی پپتیدها ساخته می شوند و حاوی تعدادی کوآنزیم ردوکس مختلف مرتبط با پروتئین ها هستند.
حامل های الکترون سیتوکروم ها (به این دلیل به دلیل رنگشان نامگذاری شده اند) پروتئین هایی هستند که به عنوان یک گروه پروتز حاوی گروه های مختلف هستند سنگهای قیمتی نوع همس ب با هموگلوبین ها مطابقت دارد. هم به صورت کووالانسی به یک پروتئین متصل می شود (شکل 13.4).
مشترک سیتوکروم ها توانایی یون آهن است که در هم وجود دارد ، برای تغییر حالت اکسیداسیون هنگام انتقال الکترون: 
دهیدروژنازهای وابسته به فلاوین - اینها پروتئینهایی هستند که در آنها گروههای سولفیدریل سیستئین ، که بخشی از پروتئین است ، به اتمهای آهن متصل می شوند ، در نتیجه مجتمع های آهن و گوگرد (مراکز) تشکیل می شوند. همانند سیتوکروم ها ، اتم های آهن در چنین مراکزی قادر به دادن و دریافت الکترون هستند و به طور متناوب به حالت های fer- (Fe +3) و ferro- (Fe +2) می روند.
مراکز گوگرد آهن همراه با آنزیمهای حاوی فلاوین FAD یا FMN عمل می کنند.
FPavinadenine dinucleotide (FAD) مشتق ویتامین B 2 (ریبوفلاوین) است. FAD (فرم اکسید شده) ضمن کاهش ، دو اتم هیدروژن متصل می کند و به FADH 2 (شکل کاهش یافته) تبدیل می شود:

حامل الکترون دیگر متعلق به این گروه ، فلاوین مونونوکلئوتید (FMN) نیز مشتق ویتامین B2 است (فقط در حضور یک گروه فسفات از ویتامین B2 متفاوت است).
هر دو کوآنزیم فلاوین می توانند به صورت اصطلاحاً وجود داشته باشند نیمه کوینون ها - رادیکال های آزاد ، که در نتیجه انتقال تنها یک الکترون به FAD یا FMN تشکیل می شوند:

مشخصات کلی فلاوپروتئین های مختلف که در ترکیب پروتئین آنزیم متفاوت هستند FP „است.
دهیدروژنازهای وابسته به پیریدین این نام را گرفت زیرا کوآنزیم برای آنها NAD + و NADP + است که در مولکول های آن یک مشتق وجود دارد پیریدین - نیکوتین آمید:

واکنش های کاتالیز شده توسط این آنزیم ها را می توان به شرح زیر نشان داد:

دهیدروژنازهای مرتبط با NAD + در درجه اول در فرآیند تنفس نقش دارند ، یعنی در فرآیند انتقال الکترون از بسترها به اکسیژن ، در حالی که دهیدروژنازهای مرتبط با NADP + عمدتا در انتقال الکترون از بسترهای ناشی از واکنش های کاتابولیکی به واکنش های احیا کننده بیوسنتز نقش دارند.
تنها حامل غیر پروتئینی الکترون ، یوبی کینون است که به این دلیل نامگذاری شده است زیرا این کینون در همه جا یافت می شود (از همه جا - همه جا). این ماده با اختصار CoQ یا به سادگی Q. در هنگام کاهش ، یوبی کینون نه تنها الکترون بلکه پروتون را نیز متصل می کند. با انتقال یک الکترون ، تبدیل می شود نیمه کوینون ، دو الکترون - در هیدروکینون
توالی حامل های الکترون در زنجیره تنفسی میتوکندری را می توان با نمودار زیر نشان داد:

این طرح با زنجیره ای از واکنش های متوالی توصیف می شود: 

به این ترتیب ، از طریق زنجیره تنفسی ، الکترون ها از لایه های زیرین به گیرنده نهایی - اکسیژن اتمسفر می رسند. به آب حاصل آب متابولیک گفته می شود.
جداسازی هیدروژن به پروتون ها و الکترون ها در غشای میتوکندری یک زنجیره انتقال الکترون است که مانند پمپ پروتون کار می کند و یون های هیدروژن را از فضای بین سلولی به خارج غشاing می رساند.
سخنرانی در BH
برای دانش آموزان _ 2 __ دوره شفابخش دانشکده
موضوع اکسیداسیون بیولوژیکی 2. تنفس بافتی. فسفوریلاسیون اکسیداتیو.
زمان 90 دقیقه
اهداف آموزشی و تربیتی:
ایده بدهید:
در ساختار زنجیره تنفسی (DC) ، بازدارنده ها ؛ مکانیسم های عملکرد DC نقاط رابط ، مقادیر ORP از اجزای DC. در مورد نسبت P / O ، معنی آن.
تنفس آزاد و قطع. درباره نظریه های صرف در OF.
در مکانیسم نسل Н +.
درباره ساختار و عملکردهای ATPase پروتون ؛ در مورد مکانیزم جدایی
در فسفوریلاسیون اکسیداتیو (pH و) ؛ در مورد مکانیسم های ترموژنز ، نقش بافت چربی قهوه ای.
در مورد نقش متابولیسم انرژی ؛ راه های استفاده از H + و ATP. در مورد جنبه های کاربردی انرژی زیستی.
در مورد راه های مصرف O 2 در بدن (میتوکندری ، میکروزومی ، پراکسید). در مورد ویژگی های DC میکروزومی در مقایسه با میتوکندری در مورد ویژگی های سیتوکروم P 450 ، عملکرد.
درباره پراکسیداسیون. درباره مکانیسم تشکیل گونه های اکسیژن فعال O 2 - ، O 2 ، O 2. در مورد نقش فرآیندهای پراکسید در سلامت و بیماری ها. در مورد پراکسیداسیون لیپیدها (LPO): (NEFA → R → diene conjugates → hydroperoxides → MDA). در مورد روش های ارزیابی فعالیت LPO.
در مورد محافظت از آنتی اکسیدان: آنزیمی و غیر آنزیمی. در مورد ویژگی های SOD ، کاتالاز ، گلوتاتیون پراکسیداز ، GSH- ردوکتاز ، سیستم های تولید مثل NADPH. درباره AOS غیر آنزیمی: ویتامین های E ، A ، C ، کاروتنوئیدها ، هیستیدین ، \u200b\u200bکورتیکواستروئیدها ، بیلی روبین ، اوره و غیره
ادبیات
Berezov T. T.، Korovkin B. F. شیمی بیولوژیک. م.: پزشکی ، 1990. S. 213–220؛ 1998 S. 305–317.
نیکولایف A. یا. شیمی بیولوژیک. م.: مدرسه عالی ، 1989. S. 199-221.
اضافی
فیلیپوویچ یو.ب.مبانی بیوشیمی. م.: مدرسه عالی ، 1993. S. 403-438.
موری R. و همکارانبیوشیمی انسان. مسکو: میر ، 1993. T. 1. S. 111–139.
آ. مبانی بیوشیمی. مسکو: میر ، 1985. T. 2. ص. 403–438 ، 508–550.
آلبرت ها ب و و غیره.، زیست شناسی سلول مولکولی. مسکو: میر ، 1994 ، ت. 1. ص 430–459.
اسکولاچف V.P.انرژی غشاهای بیولوژیکی. م.: علم. 1989
پشتیبانی از مواد
1. ارائه چندرسانه ای.
محاسبه زمان یادگیری
|
لیست سوالات آموزشی |
مقدار زمان اختصاص داده شده در دقیقه |
|
|
ساختار زنجیره تنفسی (DC) ، کمپلکس های آن ، بازدارنده ها. مکانیسم عملکرد DC. نقاط اتصال ، مقدار ORP از اجزای DC. نسبت R / O ، مقدار آن. |
||
|
تنفس آزاد و قطع. تئوری اتصال (OP) (شیمیایی ، ساختاری ، شیمی سموتیک - P. میچل). |
||
|
مکانیسم تولید H + ، اجزای آن ، استوکیومتری H + / e. |
||
|
ساختار و عملکرد پروتون ATPase. مکانیسم تفکیک |
||
|
OF (حذف pH و ). مکانیسم های ترموژنز. نقش بافت چربی قهوه ای. |
||
|
نقش اساسی متابولیسم انرژی. مسیرهای استفاده برای H + و ATP. جنبه های کاربردی انرژی زیستی. |
||
|
راه های مصرف O 2 در بدن (میتوکندری ، میکروزوم ، پراکسید). ویژگی های DC میکروزومی ، مقایسه آن با میتوکندری. ویژگی های سیتوکروم P 450 ، عملکرد آنها. |
||
|
پراکسیداسیون مکانیسم تشکیل گونه های اکسیژن فعال O 2 - ، O 2 ، O 2. نقش فرآیندهای پراکسید در سلامتی و بیماری ها. درک عمومی LPO (NEFA → R → diene ترکیبات → هیدروپراکسیدها → MDA). روشهای ارزیابی فعالیت LPO. |
||
|
محافظت از آنتی اکسیدان: آنزیمی و غیر آنزیمی. خصوصیات SOD ، کاتالاز ، گلوتاتیون پراکسیداز ، GSH- ردوکتاز ، سیستم های تولید مثل NADPH. AOS غیر آنزیمی: ویتامین های E ، A ، C ، کاروتنوئیدها ، هیستیدین ، \u200b\u200bکورتیکواستروئیدها ، بیلی روبین ، اوره و غیره |
فقط 90 دقیقه
ساختار زنجیره تنفسی (DC) ، مجتمع ها ، بازدارنده ها. مکانیسم کار نقاط صرف ، مقدار تخم مرغ از اجزای dts. ضریب R / o ، مقدار آن.
زنجیره تنفسی.
مرحله ای "احتراق کنترل شده" با روشن شدن متوسط \u200b\u200bآنزیم های تنفسی با پتانسیل اکسایش مختلف به دست می آید. پتانسیل Redox (پتانسیل اکسایش) جهت انتقال پروتون ها و الکترون ها توسط آنزیم های زنجیره تنفسی را تعیین می کند (عکس. 1).
پتانسیل Redox بیان می شود مقدار نیروی الکتریکی (در ولت) ، که در محلول بین ماده اکسید کننده و عامل احیا کننده وجود دارد ، در غلظت 1.0 mol / L در 25 درجه سانتیگراد وجود دارد (در pH \u003d 7.0 ، هر دو در تعادل با الکترود هستند ، که می تواند الکترون ها را به طور برگشت پذیر از عامل احیا کننده دریافت کند). در pH \u003d 7.0 ، پتانسیل اکسایش ردوکس سیستم H2 / 2H + + 2ē است – 0.42 v. امضا کردن – به این معنی است که این جفت اکسیداسیون به راحتی الکترونها را اهدا می کند ، یعنی نقش یک ترمیم کننده ، علامت گذاری را بازی می کند + نشانگر توانایی یک جفت اکسیداسیون برای پذیرش الکترون است ، به عنوان مثال نقش یک ماده اکسید کننده را بازی می کنند. به عنوان مثال ، پتانسیل کاهش اکسیداسیون جفت NADH ∙ H + / NAD + برابر است با - 0.32 ولت ، که نشان دهنده توانایی بالای آن در اهدای الکترون است و جفت اکسایش اکسیداسیون doO 2 / H 2 O دارای بیشترین مقدار مثبت +0.81 ولت ، آنهایی که اکسیژن بالاترین توانایی پذیرش الکترون را دارد.
در طی اکسیداسیون AcCoA در CTX ، اشکال کاهش یافته NADH2 و FADH2 وارد DC می شوند ، جایی که انرژی الکترون ها و پروتون ها به انرژی پیوندهای ATP با انرژی بالا تبدیل می شود.
DC مجموعه ای از دهیدروژنازها است که الکترون ها و پروتون ها را از بستر به اکسیژن منتقل می کند.
اصول عملکرد DC بر اساس قوانین 1 و 2 ترمودینامیک است.
نیروی محرکه DC تفاوت ORP است. اختلاف کل کل DC 1.1 ولت است. نقاط فسفوریلاسیون باید دارای افت ORP \u003d 0.25 - 0.3 V باشند.
1. جفت NAD-H دارای ORP \u003d 0.32 V است.
2. جفت Q-b - / - / - - 0 ولت
3.O2 - دارای 0/82 ولت است.
DC در غشای میتوکندری داخلی قرار دارد و دارای 2 روش معرفی الکترون و پروتون یا 2 ورودی است. DC 4 مجموعه را تشکیل می دهد.
1 ورودی: وابسته به NAD (الکترون ها و پروتون ها از همه واکنش های وابسته به NAD ناشی می شوند).
2 ورودی: وابسته به FAD
بیش از ----\u003e FP
Q ---\u003e b ---\u003e c 1 ---\u003e c ---\u003e aa 3 ----\u003e 1 / 2O 2
اسید سوکسینیک ----\u003e FP
زنجیره تنفسی - نوعی اکسیداسیون بیولوژیکی.
تنفس بافتی دنباله ای از واکنش های کاهش اکسیداسیون است که در غشای داخلی میتوکندری با مشارکت آنزیم های زنجیره تنفسی رخ می دهد. زنجیره تنفسی دارای یک ساختار ساختاری روشن است ، اجزای آن تشکیل می شود مجتمع های تنفسی، ترتیب آن به مقدار پتانسیل اکسایش ردوکس آنها بستگی دارد (شکل 5.1). تعداد زنجیره های تنفسی در یک میتوکندری منفرد از سلولهای بافتهای مختلف یکسان نیست: در کبد - 5000 ، در قلب - حدود 20000 ، بنابراین ، میوکاردیوسیت ها با تنفس شدیدتر از سلولهای کبدی متمایز می شوند.
شکل: 5.1 ترتیب آرایش مجموعه های زنجیره تنفسی در غشای داخلی میتوکندری
قبل از پرداختن به مشخصات هر یک از اجزای زنجیره تنفسی ، با لایه های تنفس بافت آشنا شویم.
بسترهای تنفسی بافتی به 2 گروه تقسیم می شوند:
وابسته به بیش از حد - بسترهای چرخه ایوبوسیترات ، α-ketoglutarate و مالات. این ماده همچنین پیروات ، هیدروکسی بوتیرات و β-هیدروکسی-آسیل ~ CoA ، گلوتامات و برخی دیگر از اسیدهای آمینه است. هیدروژن از بسترهای وابسته به NAD با استفاده از دهیدروژنازهای وابسته به NAD به مجتمع اول زنجیره تنفسی منتقل می شود.
وابسته به FAD - سوکسینات ، گلیسرول-3-فسفات ، آسیل ~ CoA و برخی دیگر. هیدروژن از بسترهای وابسته به FAD به مجموعه دوم زنجیره تنفسی منتقل می شود.
هنگام از بین بردن لایه های زیر آب دهیدروژنازهای وابسته به بیش از حد شکل کاهش یافته NAD (NADH ∙ H +) تشکیل می شود.

فرم اکسید شده کوآنزیم NAD + نشان داده شده است. این کوآنزیم یک دینوکلئوتید است ( nایکوتینامید-آجین-داینوکلئوتید): یک نوکلئوتید حاوی ویتامین PP (نیکوتینامید) است ، دیگری AMP است. توانایی یک کوآنزیم برای ایفای نقش یک حامل هیدروژن میانی با وجود ویتامین PP در ساختار آن ارتباط دارد. در فرم الکترون-پروتون ، روند برگشت پذیر هیدروژناسیون-دهیدروژناسیون را می توان با معادله نشان داد (R بقیه کوآنزیم است):

NADH ∙ H + نه تنها در میتوکندری بلکه در سیتوزول سلول در طی فرآیندهای متابولیکی خاص نیز می تواند تشکیل شود. با این حال ، کوآنزیم سیتوپلاسمی نمی تواند به میتوکندری نفوذ کند. هیدروژن کوآنزیم کاهش یافته ابتدا باید به لایه هایی منتقل شود ممکن است به میتوکندری نفوذ کند. این لایه های انتقال دهنده H2 عبارتند از:
اگزالات استات → مالات
استواستات → β-هیدروکسی بوتیرات
دی هیدروکسی استون فسفات → گلیسرول-3-فسفات

سپس NADH ∙ H توسط کمپلکس 1 زنجیره تنفسی اکسید می شود. بیایید عملکرد این مجموعه را در نظر بگیریم.
من - NADH ∙ H + -ubiquinone-oxidoductase.
اولین مجموعه بزرگترین در زنجیره تنفسی است (که توسط 23-30 زیر واحد نشان داده می شود). انتقال هیدروژن از NADH ∙ H + به ubiquinone را کاتالیز می کند (شکل 5.1 و شکل 5.3). این ماده حاوی کوآنزیم FMN (مونونوکلئوتید فلاوین) و پروتئین های گوگرد آهن حاوی آهن غیر هم است. عملکرد این پروتئین ها است در جداسازی جریان پروتونها و الکترونها:الکترون ها از FMN-H2 به سطح داخلی غشای میتوکندری داخلی (رو به ماتریس) منتقل می شوند و پروتون ها به سطح خارجی غشای داخلی منتقل می شوند و سپس در ماتریکس میتوکندری آزاد می شوند.
در حین انتقال پروتون ها و الکترون ها ، پتانسیل اکسایش اکسیداسیون کمپلکس اول 0.38 ولت کاهش می یابد ، که برای سنتز ATP کاملاً کافی است. با این حال ، در خود مجتمع ، ATP تشکیل نمی شود و انرژی آزاد شده در نتیجه عملکرد مجتمع جمع می شود (شکل زیر را ببینید): تشکیل پتانسیل الکتروشیمیایی را ببینید) و تا حدی به صورت گرما پراکنده می شود.
با توجه به ساختار خود ، FMN یک مونونوکلئوتید است که در آن پایه نیتروژن توسط هسته ایزوالوکسازین ریبوفلاوین نشان داده می شود ، و پنتوز ریبیتول است (به عبارت دیگر ، FMN یک شکل فسفریله شده از ویتامین B2 است).

عملکرد FMN پذیرش 2 اتم هیدروژن از NADH ∙ H + و انتقال آنها به پروتئین های گوگرد آهن است. هیدروژن (2 الکترون و 2 پروتون) به اتم های نیتروژن حلقه ایزوالوکسازین متصل است ، در حالی که بازآرایی درون مولکولی پیوندهای دوتایی با تشکیل یک نیمه کوئینون میانی رخ می دهد - ترکیبی از طبیعت رادیکال آزاد (نمودار نشان می دهد جمع معادله واکنش ، جایی که R بقیه مولکول است)

دوم بافت پیچیده زنجیره تنفس - سوکسینات-یوبی کوینون-اکسیدورودکتاز.
این مجموعه وزن مولکولی کمتری دارد و همچنین دارای پروتئین های گوگرد آهن است. سوکسینات-یوبی کوینون-اکسیدورودکتاز انتقال هیدروژن از را کاتالیز می کند همسر شدن به ubiquinone. این مجموعه شامل کوآنزیم FAD (دینوکلئوتید فلاوین-آدنین) و آنزیم سوکسینات دهیدروژناز است که در عین حال آنزیمی از چرخه کربس است. آسیلSCoA ، 3-فسفو-گلیسرات و دیوکسی استون فسفاتهمچنین بسترهای تنفسی بافتی وابسته به FAD هستند و با کمک این کوآنزیم با کمپلکس دوم تماس می گیرند.

شکل: 5.3 اولین مجموعه زنجیره تنفسی
انرژی ورود هیدروژن زیرلایه ها به کمپلکس II زنجیره تنفس بافتی عمدتا به صورت گرما پراکنده می شود ، زیرا در این قسمت از زنجیره پتانسیل اکسایش کمی کاهش می یابد و این انرژی برای سنتز ATP کافی نیست.

روند بازیابی FAD مشابه فرآیند FMN پیش می رود.
کوآنزیم Q یا ubiquinone یک ترکیب آبگریز است که یکی از اجزای غشای سلول است ، با غلظت بالا یافت می شود ، به گروه ویتامین ها تعلق دارد. متعلق به گروه ویتامین ها است.
Ubiquinone (کوآنزیم Q). Ubiquinone یک مولکول لیپوفیلی کوچک است ، از نظر شیمیایی یک بنزوکینون با یک زنجیره جانبی طولانی است (تعداد واحدهای ایزوپروئید از 6 باکتری تا 10 پستاندار است).
در زنجیره تنفسی ، کوآنزیم Q نوعی انبار هیدروژن (استخر) است که آن را از انواع فلاوپروتئین ها دریافت می کند. ماهیت لیپوفیلی مولکول یوبی کینون توانایی حرکت آزادانه آن در فاز لیپیدی غشا membrane میتوکندری را تعیین می کند ، پروتون ها و الکترون ها را نه تنها از مجتمع های I و II زنجیره تنفسی رهگیری می کند ، بلکه پروتون ها را از ماتریس میتوکندری نیز می گیرد. در این حالت ، یوبی کینون با تشکیل یک محصول رادیکال آزاد میانی - نیمه کوینون کاهش می یابد.
شکل کاهش یافته یوبی کینون - یوبی کینول - پروتون ها و الکترون ها را به کمپلکس III زنجیره تنفسی منتقل می کند.

سیتوکروم اکسیداز میل زیادی به اکسیژن دارد و می تواند در غلظت های کم کار کند.
aa 3 - شامل 6 زیر واحد است که هر کدام حاوی هم و یک اتم مس است. 2 زیر واحد سیتوکروم a را تشکیل می دهد و 4 واحد باقی مانده متعلق به سیتوکروم a 3 است.
بین NAD و FP ، b-c ، a-a3 ، حداکثر افت ORP وجود دارد. این نقاط محل سنتز ATP (محل فسفوریلاسیون ADP) هستند.
III مجموعه زنجیره تنفس بافتی – ubiquinol-cytochrome C-oxidoreductase. مجموعه III شامل سیتوکروم هاب و از جانب 1 متعلق به گروه پروتئین های پیچیده است کروموپروتئین ها... گروه پروتز این پروتئین ها رنگی (کروما - رنگ) است و از نظر ساختار شیمیایی نزدیک به هموگلوبین هم است. با این حال ، بر خلاف هموگلوبین و اکسی هموگلوبین ، که در آن آهن باید فقط به شکل 2 ظرفیتی باشد ، آهن در سیتوکروم ها در طول کار زنجیره تنفسی از حالت دو ظرفیتی به یک حالت سه ظرفیتی (و بالعکس) منتقل می شود.
همانطور که از نامش پیداست ، III پیچیده الکترونها را از ubiquinol به سیتوکروم C منتقل می کند. ابتدا الکترون ها به فرم اکسید شده سیتوکروم b (Fe 3+) وارد می شوند که کاهش می یابد (Fe 2+) ، سپس سیتوکروم کاهش یافته الکترون ها را به شکل اکسید شده سیتوکروم c منتقل می کند ، که همچنین ترمیم می شود و به نوبه خود ، الکترون ها را به سیتوکروم C منتقل می کند.
غشای میتوکندری از کمپلکس III تا IV و بالعکس. در این حالت ، 1 مولکول سیتوکروم C ، به طور متناوب اکسید و کاهش می یابد ، 1 الکترون را منتقل می کند.

چهارم مجتمع زنجیره تنفسی – سیتوکروم C اکسیداز.این مجموعه نامگذاری شده است اکسیدازبه دلیل توانایی تعامل مستقیم با اکسیژن. در پستانداران ، این پروتئین بزرگ غشایی (~ 200 کیلو دالتونی) از 6 تا 13 زیر واحد تشکیل شده است که برخی از آنها توسط DNA میتوکندری کدگذاری می شوند. کمپلکس IV شامل 2 کروموپروتئین است - سیتوکرومآ و سیتوکرومآ 3 . برخلاف سایر سیتوکروم ها ، سیتوکروم ها آ و آ 3 هر کدام نه تنها حاوی یک اتم آهن بلکه یک اتم مس نیز هستند. مس در ترکیب این سیتوکروم ها در حین انتقال الکترون نیز به طور متناوب به حالت اکسید شده (Cu 2+) و کاهش یافته (Cu +) منتقل می شود.
سیتوکروم از جانب-اکسیداز اکسیداسیون یک الکترون از 4 مولکول سیتوکروم کاهش یافته را کاتالیز می کند از جانبو همزمان همزمان كاهش كامل (4 الكتروني) مولكول اکسيژن را انجام مي دهد:
4 سیتوکروم از جانب(Fe 2+) + 4 H + + O 2 4 سیتوکروم از جانب(Fe 3+) + H 2 O
پروتون های تشکیل مولکول های آب از ماتریس می آیند. لازم به ذکر است که این واکنش بسیار پیچیده است و طی مراحل میانی تشکیل رادیکال های آزاد اکسیژن ادامه می یابد.
پتانسیل اکسایش ردوکس کمپلکس IV بزرگترین (57/0 + v) است ، انرژی آن برای سنتز 3 مولکول ATP کاملاً کافی است ، با این حال ، بیشتر این انرژی برای "پمپاژ" پروتون ها از ماتریس میتوکندری به فضای بین غشایی استفاده می شود. به دلیل انتقال فعال پروتون ها ، سیتوکروم از جانب-اکسیداز نامگذاری شد "پمپ پروتون".
بنابراین ، تنفس بافتی فرآیند انتقال الکترونها و پروتون ها از بسترهای وابسته به NAD یا FAD به اکسیژن و همچنین پروتون های ارائه شده توسط ماتریس میتوکندری است. در حین حمل و نقل ، پتانسیل اکسایش کاهش می یابد ، که با آزاد سازی انرژی موجود در لایه های تنفس بافت همراه است. کاهش کامل اکسیژن مولکولی در هوا در زنجیره تنفسی با تشکیل آب همراه است.
در یک زنجیره تنفسی کوتاه ، بستر اکسید می شود ، که برای آن فلپروتئین گیرنده اولیه الکترون است (هیچ مرحله اکسیداسیون بستر با NAD-DH وجود ندارد). مواد با زنجیره کوتاه: اسید سوکسینیک ، فرمهای فعال اسیدهای چرب ، گلیسروفسفات).
اولین واکنش اکسیداسیون:
پس از آن ، FADN 2 ، با مشارکت (FeS *) + KoQ ، اکسید می شود:
CoQ کاهش یافته در طول زنجیره تنفسی توسط سیستم سیتوکروم:

این زنجیره های تنفسی را می توان به قطعات ساختاری و عملکردی تقسیم کرد که مجتمع های اکسیداتیو نامیده می شوند. در زنجیره بلند ، 3 مجموعه جدا شده است و در کوتاه 2.
1. بین NADH 2 و CoQ واقع شده و شامل مجموعه های FP و FeS است.
2. KoQH 2 -DH (کمپلکس سیتوکروم C-ردوکتاز) بین KoQ و cC واقع شده و شامل cV ، FeS ، پروتئین ها ، cC 1 می باشد.
3. کمپلکس سیتوکروم اکسیداز - اکسیداسیون cS و شامل caa 3
4- مجموعه سوکسینات دهیدروژناز شامل EP * و FeS ، سوکسینات DG است
هر مجموعه تنفسی را می توان توسط مواد خاص - مهارکننده ها - از زنجیره تنفسی خاموش کرد.
اولین مجموعه - آمیتال ، باربیتورات ، روتنول
کمپلکس دوم مونونات است
سومین کمپلکس آنتیمایسین A است
مجتمع چهارم - H 2 S ، سیانیدها ، CO
اکسیداسیون داخل میتوکندری ارتباط نزدیکی با متابولیسم انرژی دارد. تبادل انرژی - تعادل روند واکنشهای شکل گیری و واکنشهای استفاده از انرژی.
به واکنشهایی که با آزادسازی انرژی انجام می شود گفته می شود عجیب واکنش های جذب غیر آلی فرآیند اصلی غیر عادی در بدن انتقال الکترونها در امتداد زنجیره تنفسی است. اجزای اولیه NAD اکسید شده ، NAD کاهش می یابد:
 بنابراین ، در CPE یک حرکت الکترون با انرژی بالا وجود دارد ، در روند انتقال الکترون ، انرژی آزاد می شود. آن انرژی که می تواند برای انجام برخی کارها استفاده شود - انرژی آزاد... در زنجیره تنفسی ، انرژی محاسبه می شود.
بنابراین ، در CPE یک حرکت الکترون با انرژی بالا وجود دارد ، در روند انتقال الکترون ، انرژی آزاد می شود. آن انرژی که می تواند برای انجام برخی کارها استفاده شود - انرژی آزاد... در زنجیره تنفسی ، انرژی محاسبه می شود.
ΔF \u003d -23 * n * Δе,
جایی که n تعداد الکترون های منتقل شده در هر اتم О 2 (2е) است ، Δе افت ORP بین ابتدا و انتهای CPE است.
Δе \u003d 0.82 - (- - 0.32) \u003d 1.14 ولت
ΔF \u003d -23 * 2 * 1.14 \u003d -52 کیلو کالری در مول
این انرژی می تواند توسط بدن برای انجام فرایندهای مختلف استفاده شود:
- انقباض مکانیکی - عضلانی
- شیمیایی - برای سنتز مواد جدید
- حمل و نقل اسمزی - یون در برابر شیب غلظت
- الکتریکی - ظهور پتانسیل ها در سیستم عصبی
همه موجودات ، بسته به انرژی مورد استفاده ، به دو نوع تقسیم می شوند: فوتوتروف - می تواند از انرژی نور خورشید استفاده کند ، هموار - فقط می تواند از انرژی پیوندهای شیمیایی مواد ویژه با انرژی بالا استفاده کند.
مواد ماکرورژیک- موادی در حین هیدرولیز پیوندها که انرژی آنها بیش از 5 کیلو کالری در مول است. اینها شامل فسفنول پیروات ، کراتین فسفات ، فسفات 1،3-دی فسفوگلیسرول ، اسیدهای چرب اسیدها ، ATP (GTP ، CTP ، UCP) هستند. در میان کلان های ذکر شده ، ATP جایگاه اصلی را به خود اختصاص داده است. ATP یک باتری و منبع انرژی شیمیایی است. ATP مولکولی حاوی انرژی 3.3 کیلوکالری در مول (در شرایط استاندارد) و در شرایط فیزیولوژیکی تا 12 کیلو کالری در مول است. ترکیب ATP: آدنیل-ریبوز-H 3 PO 4 - H 3 PO 4 -H 3 PO 4. ATP از ADP سنتز می شود. تجزیه ATP یک فرآیند ارگانیک است. منبع اصلی انرژی برای سنتز ATP انتقال الکترون ها در امتداد زنجیره تنفسی است. افزودن H 3 PO 4 را فسفوریلاسیون می نامند.
فسفوریلاسیون اکسیداتیو
فرآیند سنتز ATP از ADP و H 3 PO 4 ، به دلیل انرژی حمل و نقل در امتداد CPE. فرآیندهای اکسیداسیون زنجیره تنفسی و سنتز ATP ارتباط تنگاتنگی دارند. در این حالت ، فرآیند اصلی انتقال الکترون ها است که همراه با فسفوریلاسیون است. قسمتهایی از زنجیره تنفسی که سنتز ATP در آنها اتفاق می افتد ، محلهای مزدوج نامیده می شود. سه تا از آنها در زنجیره بلند وجود دارد (1 ، 3 ، 4 مجتمع های اکسیداتیو هستند) ، در زنجیره تنفسی کوتاه دو تا وجود دارد (3،4). اگر ماده ای در زنجیره تنفسی اکسید شود ، حداکثر سه مولکول ATP ساخته می شود. کارایی ترکیب فسفوریلاسیون اکسیداتیو با ضریب فسفوریلاسیون بیان می شود. این نشان می دهد که هنگام انتقال دو الکترون به ازای هر اتم اکسیژن ، چند مولکول H 3 PO 4 به ADP متصل شده است ، یعنی چند مولکول ATP در هر اتم اکسیژن ساخته می شود. برای یک زنجیره بلند ، ضریب \u003d 3 برای 2 کوتاه.
مکانیسم فسفوریلاسیون اکسیداتیو.
برای اولین بار در دهه سی ، عمل سنتز ATP در فرآیند اکسیداسیون توسط بیگل شیمیست روسی Engelhardt آشکار شد. فرضیه اصلی برای توضیح مکانیسم فسفوریلاسیون اکسیداتیو ، شیمیاسموتیک بود  نظریه میچل. بر اساس آن ، در حین انتقال الکترونها در امتداد زنجیره تنفسی ، یک پتانسیل پروتون بوجود می آید ، که انرژی آزاد شده هنگام انتقال الکترون را جمع می کند. پس از آن ، از پتانسیل پروتون برای سنتز ATP استفاده می شود. ظهور پتانسیل پروتون با نفوذ ناپذیری پروتون های غشای میتوکندری داخلی همراه است. در نتیجه حمل و نقل الکترونها در امتداد زنجیره تنفسی ، H + به طور همزمان از ماتریس به فضای بین غشایی خارج می شود. منتقل شده 6 - 10 H +.
نظریه میچل. بر اساس آن ، در حین انتقال الکترونها در امتداد زنجیره تنفسی ، یک پتانسیل پروتون بوجود می آید ، که انرژی آزاد شده هنگام انتقال الکترون را جمع می کند. پس از آن ، از پتانسیل پروتون برای سنتز ATP استفاده می شود. ظهور پتانسیل پروتون با نفوذ ناپذیری پروتون های غشای میتوکندری داخلی همراه است. در نتیجه حمل و نقل الکترونها در امتداد زنجیره تنفسی ، H + به طور همزمان از ماتریس به فضای بین غشایی خارج می شود. منتقل شده 6 - 10 H +.
ETC در CPM ، در یوکاریوت ها - روی غشای میتوکندری داخلی قرار دارد. حامل ها با توجه به پتانسیل اکسایش Redox خود واقع شده اند ، انتقال الکترون در کل طول زنجیره به صورت خودجوش انجام می شود.
پتانسیل پروتون توسط ATP سنتاز به انرژی پیوندهای شیمیایی ATP تبدیل می شود. کار مزدوج سنتاز ETC و ATP فسفوریلاسیون اکسیداتیو نامیده می شود.
زنجیره انتقال الکترون میتوکندریایی
تأثیر پتانسیل اکسیداتیو
| عامل کاهنده | اکسید کننده | ائو ، ب |
|---|---|---|
| H2 | 2 + | - 0,42 |
| بیش از H + H + | بیش از + | - 0,32 |
| NADP H + H + | NADP + | - 0,32 |
| فلاوپروتئین (کاهش یافته) | فلاوپروتئین (اکسید) | - 0,12 |
| کوآنزیم Q H2 | کوآنزیم Q | + 0,04 |
| سیتوکروم B (Fe2 +) | سیتوکروم B (Fe3 +) | + 0,07 |
| سیتوکروم C 1 (Fe2 +) | سیتوکروم C 1 (Fe3 +) | + 0,23 |
| سیتوکروم A (Fe2 +) | سیتوکروم A (Fe3 +) | + 0,29 |
| سیتوکروم A3 (Fe2 +) | سیتوکروم A3 (Fe3 +) | +0,55 |
| H2O | ½ O2 | + 0,82 |
بازدارنده های زنجیره تنفسی
برخی از مواد مانع انتقال الکترون از طریق مجتمع های I ، II ، III ، IV می شوند.
- مهارکننده های پیچیده I - باربیتورات ها ، روتنون ، پیرسیدین
- مهار کننده Complex II - مالونات.
- مهار کننده کمپلکس III - آنتیمایسین A ، میکسوتیازول ، استگماتلین
- مهار کننده های پیچیده IV - سولفید هیدروژن ، سیانیدها ، مونوکسید کربن ، اکسید نیتریک ، آزید سدیم
زنجیره انتقال الکترون از باکتری ها
باکتری ها ، بر خلاف میتوکندری ، از مجموعه زیادی از اهدا کنندگان و پذیرنده های الکترون و همچنین مسیرهای مختلف برای انتقال الکترون بین آنها استفاده می کنند. این مسیرها می توانند همزمان انجام شوند ، به عنوان مثال ، اشرشیاکلی وقتی روی محیطی حاوی گلوکز به عنوان منبع اصلی مواد آلی رشد کند ، از دو دهیدروژناز NADH و دو اکسیداز کینول استفاده می شود ، به این معنی که 4 مسیر انتقال الکترون وجود دارد. بیشتر آنزیم های ETC قابل القا هستند و تنها در صورت نیاز به راهی که وارد آن می شوند ، سنتز می شوند.
علاوه بر مواد آلی موجود در باکتری ها ، دهنده دهنده الکترون می تواند هیدروژن مولکولی ، مونوکسیدکربن ، آمونیوم ، نیتریت ، گوگرد ، سولفید ، آهن دو ظرفیتی باشد. به جای NADH و سوکسینات دهیدروژناز ، می توان فرمات - ، لاکتات - ، گلیسرآلدئید-3-فسفات دهیدروژناز ، هیدروژناز و غیره را جای داد. به جای اکسیداز ، که در شرایط هوازی استفاده می شود ، در غیاب اکسیژن ، باکتری ها می توانند از ردوکتازها استفاده کنند که گیرنده های مختلف الکترون های انتهایی را کاهش می دهد: و نیتریت ردوکتاز و غیره
همچنین ببینید
درباره مقاله "زنجیره حمل و نقل الکترون تنفسی" یک نظر بنویسید
یادداشت
گزیده ای مشخص کننده زنجیره انتقال الکترون تنفسی
- افتخار شما ، به ژنرال. آنها در کلبه اینجا ایستاده اند. "آتش بازی ها گفتند و به سمت توشین رفتند.- حالا عزیزم.
توشین بلند شد و با پوشیدن دکمه بزرگ لباس خود و بهبودی ، از آتش دور شد ...
در فاصله ای دور از آتش توپخانه ها ، در كلاهی كه برای او آماده شده بود ، شاهزاده باگراسیون هنگام صرف شام نشسته و با برخی از ر theسای واحدهایی كه در محل وی جمع شده بودند صحبت می كرد. پیرمردی بود با چشمانی نیمه بسته ، با حرص استخوان بره را می خزید و ژنرالی بی عیب و نقص بیست و دو ساله ، از یک لیوان ودکا و شام ، و یک افسر ستاد با یک حلقه شخصی ، و ژرکوف ، بی قرار به اطراف همه نگاه می کرد ، و شاهزاده آندری ، رنگ پریده و با لبهای جمع شده چشم ها.
در این کلبه یک بنر فرانسوی بود که در گوشه ای از آن گرفته شده بود و حسابرس با چهره ای ساده لوح پارچه بنر را احساس کرد و سرش را بهت زد و تکان داد ، شاید به این دلیل که او واقعاً به ظاهر بنر علاقه مند بود و شاید به این دلیل که برایش سخت بود گرسنه به ناهار نگاه می کند ، که برای آن وسیله ای ندارد. در یک کلبه نزدیک یک سرهنگ فرانسوی بود که توسط اژدها به اسارت درآمد. افسران ما دور او جمع شدند و او را معاینه کردند. شاهزاده باگراتیون از روسای انفرادی تشکر کرد و در مورد جزئیات پرونده و خسارات وارد شده س askedال کرد. فرمانده هنگ ، که خود را در براونائو معرفی کرد ، به شاهزاده گزارش داد که به محض شروع پرونده ، او از جنگل عقب نشینی کرد ، هیزم شکن ها را جمع کرد و به آنها اجازه داد تا از کنار او عبور کنند ، با دو گردان ، فرانسوی ها را خنجر زد و سرنگون شد.
- همانطور که دیدم ، عالیجناب ، گردان اول ناراحت است ، من در جاده ایستادم و فکر کردم: "من اینها را رها می کنم و با آتش جنگ ملاقات می کنم". و چنین کرد
فرمانده هنگ آنقدر خواهان این کار بود ، از این که وقت نکرده بود این کار را پشیمان کرد ، به نظر او همه اینها مطمئناً بود. حتی ، شاید ، واقعاً چنین بود؟ آیا می توان در این سردرگمی فهمید که چه بود و چه نبود؟
- و من باید توجه داشته باشم ، عالیجناب ، - وی با یادآوری گفتگوی دولوخوف با کوتوزوف و آخرین ملاقاتش با مقام تنزل یافته ادامه داد ، - که دولوخوف خصوصی و تنزل یافته ، جلوی چشمان من ، یک افسر فرانسوی را به اسارت گرفت و خصوصاً خود را برجسته کرد.
- در اینجا ، جناب عالی ، حمله مردم پاولوگراد را دیدم ، - ژرکوف با نگرانی به اطراف نگاه کرد ، دخالت کرد ، که آن روز هوسارها را نمی دید ، اما فقط از افسر پیاده در مورد آنها شنید. - دو مربع مچاله شده ، عالیجناب.
برخی از سخنان ژرکوف لبخند زدند ، زیرا همیشه انتظار شوخی از او را داشتند. اما ، با توجه به اینکه آنچه او می گفت به شکوه سلاحهای ما و امروز متمایل است ، آنها بیان جدی کردند ، گرچه بسیاری به خوبی می دانستند آنچه که ژرکوف می گوید دروغ است ، بر اساس هیچ چیز نیست. شاهزاده باگراتیون به سرهنگ پیر برگشت.
- از همه شما آقایان متشکرم ، همه واحدها قهرمانانه عمل کردند: پیاده نظام ، سواره نظام و توپخانه. چگونه دو اسلحه در مرکز مانده است؟ او با چشمانش به دنبال کسی گشت. (شاهزاده باگراسیون در مورد اسلحه های جناح چپ نپرسید ؛ او قبلاً می دانست که در ابتدای پرونده همه اسلحه ها به آنجا پرتاب شده است.) "من فکر می کنم من از شما خواسته ام" ، به افسر وظیفه در مقر مراجعه کرد.
- یک نفر ضربه خورد ، - افسر وظیفه پاسخ داد ، - و دیگری ، من نمی توانم درک کنم. من خودم تمام وقت آنجا بودم و دستور می دادم و تازه رفته بودم ... هوا داغ بود ، "متواضعانه افزود.
شخصی گفت که کاپیتان توشین در اینجا نزدیک خود روستا ایستاده است و آنها قبلاً برای او فرستاده اند.
- بله ، آنجا بودید ، - شاهزاده باگراسیون با اشاره به شاهزاده آندری گفت.
- چرا ، ما کمی دور هم جمع نشده ایم ، - افسر وظیفه گفت ، و به بولکانسکی خوش لبخند زد.
پرنس اندرو با خونسردی و ناگهانی گفت: "من از دیدن تو لذت نبردم."
همه ساکت بودند. توشین در آستانه ظاهر شد و با ترسو از پشت ژنرال ها راه خود را باز کرد. توشین ، مثل همیشه ، با دیدن مافوق خود ، گیج و محو در اطراف ژنرال ها در کلبه ی تنگ ، قدم در میان این تیرک پرچم قرار نداد و روی آن لغزید. چند صدا خندیدند.
- چطور اسلحه مانده بود؟ - باگراشن از او پرسید ، و نه به کاپیتان اخم کرد ، بلکه به خنده هایی که صدای ژرکوف در میان آنها بلندتر بود ، اخم کرد.
توشین اکنون فقط ، از نگاه مافوق مهیب ، با کمال وحشت خود را با گناه و شرمندگی خود نشان داد که او ، زنده مانده ، دو سلاح از دست داده است. او آنقدر هیجان زده بود که تاکنون فرصت نکرده بود به آن فکر کند. خنده مأموران او را بیشتر گیج کرد. با فک پایین لرزان جلوی باگراسیون ایستاد و به سختی حرف زد:
"من نمی دانم ... عالیجناب ... هیچ کسی نبود ، جناب عالی.
- می توانی از جلد بگیری!
توشین نگفت که هیچ پوششی وجود ندارد ، گرچه این حقیقت مطلق بود. او می ترسید با این کار رئیس دیگر را زمین بیندازد و در سکوت ، با چشمانی ثابت ، مستقیم به صورت باگریشن نگاه کرد ، همانطور که یک دانش آموز ولگرد به چشمان ممتحن نگاه می کند.
سکوت به اندازه کافی طولانی بود. شاهزاده باگراسیون ، ظاهراً مایل به سختگیری نبود ، حرفی برای گفتن نداشت. دیگران جرات نمی کردند در مکالمه دخالت کنند. شاهزاده آندری با عبوس به توشین نگاه کرد و انگشتانش عصبی حرکت کردند.
- عالیجناب ، - شاهزاده آندری سکوت را در صدای تند خود قطع کرد ، - شما فرمان دادید که مرا به باتری کاپیتان توشین بفرستید. من آنجا بودم و دو سوم مردان و اسبهای کشته شده ، دو قبضه سلاح را تاب گرفتند و هیچ پوششی نداشتم.
شاهزاده باگراسیون و توشین اکنون با همان لجبازی به Bolkonsky مهار و هیجان زده نگاه می کردند.
شاهزاده آندری گفت: "و اگر جنابعالی اجازه دهید نظر خود را ابراز كنم ،" پس موفقیت روزانه را بیشتر از همه مدیون عملکرد این باتری و قاطعیت قهرمانانه کاپیتان توشین و شرکت او هستیم. "، شاهزاده آندری گفت و بدون انتظار برای پاسخ ، بلافاصله بلند شد و از میز دور شد.
مجتمع های زنجیره ای تنفسی
- کمپلکس III (کمپلکس سیتوکروم bc1) الکترون ها را از ubiquinone به دو سیتوکروم محلول در آب c واقع در غشای داخلی میتوکندری منتقل می کند. Ubiquinone 2 الکترون را منتقل می کند و سیتوکروم ها در هر سیکل یک الکترون منتقل می کنند. در این حالت ، 2 پروتون یوبی کینون نیز به آنجا می رود و توسط مجموعه پمپ می شود.
NADPH + NAD + ↔ NADP + + NADH.
FeS - مراکز گوگرد آهن.
بیشتر ببین:
... تنفسی زنجیره انتقال الکترون
تنفسی زنجیره حمل و نقل الکترون (ETC ، ETC ،) سیستمی از پروتئین های غشایی و حامل های الکترونی از نظر ساختاری و عملکردی است. ETC به شما امکان می دهد انرژی آزاد شده در طی اکسیداسیون NAD ∙ H و FADH2 توسط اکسیژن مولکولی (در صورت تنفس هوازی) یا سایر مواد (در صورت تنفس بی هوازی) را به صورت پتانسیل پروتون غشایی به دلیل انتقال پی در پی الکترون در طول زنجیره ، همراه با پمپاژ پروتون ها از طریق ذخیره کنید. غشاء. اجزای زنجیره تنفسی. زنجیره تنفسی شامل سه مجتمع پروتئینی (مجتمع های I ، III و IV) است که در غشا inner میتوکندری داخلی قرار گرفته و دو مولکول حامل متحرک - یوبی کوینون (کوآنزیم Q) و سیتوکروم c. سوسینات دهیدروژناز ، که متعلق به خود چرخه سیترات است ، همچنین می تواند به عنوان پیچیده II زنجیره تنفسی در نظر گرفته شود. سنتاز ATP گاهی اوقات V پیچیده نامیده می شود ، اگرچه در انتقال الکترون شرکت نمی کند. مجتمع های زنجیره ای تنفسی از بسیاری از پلی پپتیدها ساخته شده اند و حاوی تعدادی کوآنزیم ردوکس مختلف مرتبط با پروتئین ها هستند. اینها شامل فلاوین [FMN (FMN) یا FAD (FAD) ، در مجتمع های I و II] ، مراکز گوگرد آهن (در I ، II و III) و گروه های هم (در II ، III و IV) است. ساختار دقیق اکثر مجموعه ها هنوز ایجاد نشده است. الکترون ها از طرق مختلف وارد زنجیره تنفسی می شوند. در طی اکسیداسیون NADH + H + ، کمپلکس I الکترونها را از طریق مراکز FMN و Fe / S به یوبی کینون منتقل می کند. الکترونهایی که در طی اکسیداسیون سوکسینات ، آسیل CoA و سایر بسترها تشکیل می شوند توسط کمپلکس II یا دهیدروژناز میتوکندری دیگر از طریق FADH2 یا فلاوپروتئین متصل به آنزیم به ubiquinone منتقل می شوند (نگاه کنید به.
زنجیره انتقال الکترون (cpe).
از جانب. 166) ، در حالی که فرم اکسید شده کوآنزیم Q به ubi-hydroquinone معطر کاهش می یابد. دومی الکترون ها را به کمپلکس III منتقل می کند ، که آنها را از طریق دو hemes b ، یک مرکز Fe / S و هم c1 به یک سیتوکروم c حاوی پروتئین کم هم می رساند. دومی الکترون ها را به کمپلکس IV ، سیتوکروم c اکسیداز منتقل می کند. سیتوکروم c- اکسیداز حاوی دو مرکز حاوی مس (CuA و CuB) و hemes a و a3 برای انجام واکنش های اکسیداسیون اکسایش است که در نهایت الکترون ها از طریق آنها وارد اکسیژن می شوند. وقتی O2 کاهش می یابد ، آنیون اصلی قوی O2- تشکیل می شود که دو پروتون را به هم متصل کرده و به آب منتقل می کند. شار الکترون توسط گرادیان پروتون با کمپلکسهای تشکیل شده I ، III و IV همراه می شود. سازمان زنجیره تنفسی. انتقال پروتون ها توسط مجتمع های I ، III و IV به صورت برداری از ماتریس به فضای بین غشایی ادامه می یابد. با انتقال الکترونها در زنجیره تنفسی ، غلظت یونهای H + افزایش می یابد ، به عنوان مثال ، مقدار pH کاهش می یابد. در میتوکندری های دست نخورده ، اساساً فقط سنتاز ATP اجازه حرکت معکوس پروتون ها به داخل ماتریس را می دهد. این اساس رابطه نظارتی مهم انتقال الکترون با تشکیل ATP است. Ubiquinone ، به دلیل زنجیره جانبی غیر قطبی ، آزادانه در غشا moves حرکت می کند. سیتوکروم c محلول در آب در قسمت خارجی غشای داخلی واقع شده است. اکسیداسیون NADH (NADH) توسط کمپلکس I در قسمت داخلی غشا و همچنین در ماتریس رخ می دهد ، جایی که چرخه سیترات و اکسیداسیون β نیز رخ می دهد - مهمترین منابع NADH. علاوه بر این ، کاهش O2 و تشکیل ATP (ATP) در ماتریس صورت می گیرد. ATP بدست آمده توسط مکانیسم ضد پورت (در برابر ADP) به فضای بین غشایی منتقل می شود (به صفحه 214 مراجعه کنید) ، از آنجا که از طریق porins به داخل سیتوپلاسم نفوذ می کند
مجتمع های زنجیره ای تنفسی
- کمپلکس I (NADH دهیدروژناز) NAD-H را اکسید می کند ، دو الکترون از آن گرفته و آنها را به یوبی کینون محلول در لیپیدها منتقل می کند ، که در داخل غشا به کمپلکس III منتشر می شود. در همان زمان ، کمپلکس I 2 پروتون و 2 الکترون را از ماتریس به فضای بین غشایی میتوکندری پمپ می کند.
- کمپلکس II (سوکسینات دهیدروژناز) پروتون ها را پمپ نمی کند ، اما به دلیل اکسید شدن سوکسینات ، الکترون های اضافی برای ورود به زنجیره فراهم می کند.
- کمپلکس III (کمپلکس سیتوکروم bc1) الکترون ها را از ubiquinone به دو سیتوکروم محلول در آب c واقع در غشای داخلی میتوکندری منتقل می کند. Ubiquinone 2 الکترون را منتقل می کند و سیتوکروم ها در هر سیکل یک الکترون منتقل می کنند.
زنجیره انتقال الکترون میتوکندریایی
در این حالت ، 2 پروتون یوبی کینون نیز به آنجا می رود و توسط مجموعه پمپ می شود.
- کمپلکس IV (سیتوکروم c اکسیداز) انتقال 4 الکترون از 4 مولکول سیتوکروم به O2 را کاتالیز می کند و 4 پروتون را به فضای بین غشایی پمپ می کند. این مجموعه از سیتوکروم های a و a3 تشکیل شده است که علاوه بر هم ، حاوی یون های مس نیز هستند.
اکسیژن وارد شده از میتوکندری از خون به شکل یک مولکول O2 به اتم آهن موجود در سیتوکروم a3 هم تبدیل می شود. هر یک از اتمهای اکسیژن به دو الکترون و دو پروتون متصل شده و به یک مولکول آب تبدیل می شود.
بستر تشکیل شده در چرخه کربس دچار کمبود آب بدن (از بین بردن هیدروژن) می شود ، در نتیجه انرژی برای تشکیل ATP آزاد می شود و الکترون ها و پروتون های تشکیل شده در این فرآیند با اکسیژن ترکیب می شوند و آب تشکیل می دهند. بازیابی مولکول O2 در نتیجه انتقال 4 الکترون اتفاق می افتد. با هر اتصال 2 الکترون به اکسیژن ، که از طریق زنجیره حامل وارد آن می شود ، 2 پروتون از ماتریس جذب می شود و در نتیجه یک مولکول H2O تشکیل می شود.
الکترونها در امتداد یک زنجیره حامل منتقل می شوند که در خود غشا قرار دارد. حامل ها ، الکترون ها را می پذیرند ، اکسید می شوند و با دادن به حامل بعدی ، حامل کاهش می یابد. در پایان CPE ، الکترون ها به اکسیژن منتقل می شوند.
پروتون ها در خارج از غشای میتوکندری جابجا می شوند.
جابجایی پروتون ها به دلیل انرژی حرکت الکترون ها در داخل غشا رخ می دهد.
پروتونها نمی توانند خود به خود به غشا برگردند ، بنابراین یک بار مثبت در قسمت خارجی آن جمع می شود.
پروتون ها در انتهای CPE ، دوباره از طریق یک پروتئین خاص - ATP سنتتاز (عامل 5) عبور می کنند و در تشکیل آب شرکت می کنند. هنگامی که یک پروتون از طریق ATP سنتتاز عبور می کند ، انرژی آزاد می شود که صرف سنتز ATP می شود.
در نتیجه واکنش ORP حامل های ADP و فسفات معدنی ، ATP تشکیل می شود.
مهم: بدون وجود ADP ، اکسیداسیون رخ نمی دهد!
بسترهای دهیدروژناز وابسته به NAD و NADP در ماتریس میتوکندری و سیتوزول یافت می شوند.
حامل های اصلی الکترون در غشای داخلی میتوکندری تعبیه شده و به 4 مجتمع واقع در یک توالی خاص (بردار) سازمان یافته اند. در این توالی ، با نزدیک شدن به اکسیژن ، پتانسیل های کاهش اکسید استاندارد آنها مثبت می شود.
1. بستر ابتدا توسط دهیدروژناز اکسید می شود - NAD + ، در نتیجه ، کوآنزیم NAD + یک پروتون می گیرد و به NADH منتقل می شود.
اکثر دهیدروژنازهایی که الکترون را به CPE می رسانند حاوی NAD + هستند. آنها واکنشهایی مانند:
R-CHOH-R1 + NAD + ↔ R-CO-R1 + NADH + H +.
NADPH اهدا کننده مستقیم الکترون در CPE نیست ، اما تقریباً استفاده می شود
منحصراً در بیوسنتز احیائی. با این حال ، ممکن است به دلیل عملکرد ترانشیدروژناز پیریدین نوکلئوتید ، که واکنش را کاتالیز می کند ، الکترونهایی از NADPH را به CPE وارد کنیم:
NADPH + NAD + ↔ NADP + + NADH.
فلاوین دهیدروژنازها به عنوان کوآنزیم حاوی FAD یا FMN هستند.
FAD به عنوان یک گیرنده الکترون از بسیاری از لایه ها در واکنش هایی مانند:
R-CH2-CH2-R1 + E (FAD) ↔ R-CH \u003d CH-R1 + E (FADH2) ،
که در آن E قسمت پروتئینی آنزیم است.
بیشتر دهیدروژنازهای وابسته به FAD پروتئین های محلول هستند که در ماتریس میتوکندری موضعی هستند. استثنا سوکسینات دهیدروژناز است که در غشای داخلی میتوکندری واقع شده است.
یا بستر توسط دهیدروژناز اکسید می شود - FAD + ، در نتیجه آن کوآنزیم FAD یک پروتون می گیرد و به FADH2 تبدیل می شود.
اگر سوکسینات (اسید سوکسینیک) اکسید شود ، پس از آن اکسیداسیون توسط سوکسینات دهیدروژناز بلافاصله توسط FAD + انجام می شود.
FAD از طریق FES الکترون ها را به کوآنزیم Q (یوبی کینون) منتقل می کند.
مهم: یوبی کینون پروتئین نیست. همه ناقلین دیگر پروتئین هستند!
FeS - مراکز گوگرد آهن.
قبلی 12345678910111213 بعدی
بیشتر ببین:
به طور کلی ، کار زنجیره تنفسی به شرح زیر است:
تنفسی زنجیره انتقال الکترون
NADH و FADH2 که در واکنش های کاتابولیسم تشکیل شده اند ، اتم های هیدروژن (یعنی پروتون ها و الکترون های هیدروژن) را به آنزیم های زنجیره تنفسی منتقل می کنند.
2. الکترون ها در امتداد آنزیم های زنجیره تنفسی حرکت کرده و انرژی خود را از دست می دهند.
3- این انرژی برای پمپاژ پروتونهای H + از ماتریس به فضای بین غشایی استفاده می شود.
4- در انتهای زنجیره تنفسی ، الکترون ها وارد اکسیژن شده و آن را به آب کاهش می دهند.
5- پروتونهای H + به سمت ماتریس تمایل پیدا کرده و از طریق سنتاز ATP عبور می کنند.
6. همزمان ، آنها انرژی را که برای سنتز ATP استفاده می شود ، از دست می دهند.
اصل کلی فسفوریلاسیون اکسیداتیو
فرم های NAD و FAD را بازیابی کرد اکسید شدهتوسط آنزیم های زنجیره تنفسی ، به همین دلیل ، فسفات به ADP اضافه می شود ، یعنی فسفوریلاسیون... بنابراین ، کل فرآیند نامگذاری شد فسفوریلاسیون اکسیداتیو.
زنجیره تنفسی
جمع زنجیره انتقال الکترون شامل حدود 40 پروتئین مختلف است که در 4 مجتمع بزرگ مولنزیم متصل به غشا سازمان یافته اند. همچنین یک مجموعه دیگر وجود دارد که در انتقال الکترون مشارکت ندارد ، اما ATP را سنتز می کند.

نمودار بلوک مدار تنفسی

حامل های الکترون
1. سیتوکروم c1 ، c ، a ، a3 (گروه پروتز - هم) در قسمتهای مختلف زنجیره تنفسی واقع شده است ، سیتوکروم c یک پروتئین محلول در آب متحرک است که در امتداد قسمت خارجی غشای بین کمپلکسهای 3 و 4 حرکت می کند. سیتوکروم aa3 حاوی همگ A. است و به ترتیب شامل گروه های متیل (-CH3) و وینیل (-CH \u003d CH2) ، به ترتیب یک گروه فرمیل (-CH3H) و یک زنجیره هیدروکربنی است. ویژگی دوم وجود یون های مس در مراکز ویژه پروتئین است.
مس +<-> Cu2 + + e و Fe2 +<-> Fe3 + + e
2. پروتئین های گوگرد آهن (FeS) - پروتئین های غیر هم ، همراه با آنزیم های فلاوین (مجتمع های 1 ، 2 ، 3) 

3. FMN (مجموعه 1): FMN + NADH + H + ——— FMNH2 + NAD +
(NAD + + 2e + 2H + ————- NADH + H +)
KoQ (ubiquinone) - حامل غیر پروتئینی ، پیچیده 3.
"دم" آبگریز طولانی ایزوپرن تحرک یوبی کینون را در لایه دو لایه چربی فراهم می کند.
KoQ و سیتوکروم c متحرک هستند ، بقیه پروتئین های انتگرال هستند.



ساختار مجتمع های آنزیمی زنجیره تنفسی
مجتمع NADH-CoQ-ردوکتاز
این مجموعه همچنین دارای یک عنوان کاربردی است NADH دهیدروژناز، حاوی 1PMN ، 6 پروتئین آهن گوگرد است.
1. NADH + H + + FMN ——— 2e + 2H + ——— NAD + + FMNH2
2. FMNH2 ———— 2e ——— Fex Sx (Fe2 +<-> Fe3 + + e)
3. Fex Sx ———— 2e ——— KoQ
تابع
1- الکترونها را از NADH می پذیرد و آنها را به آنجا منتقل می کند کوآنزیم Q (اوبی کینون)
2. 4H + را به سطح خارجی غشای داخلی میتوکندری انتقال دهید.