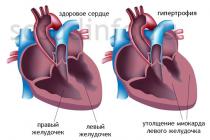
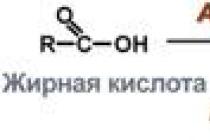
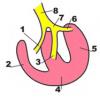
مولکول اسید چرب با تجزیه تدریجی قطعات دو کربنی به شکل استیل کوآنزیم A (استیل-CoA) به میتوکندری تجزیه می شود.
توجه داشته باشید که اولین مرحله اکسیداسیون بتا برهم کنش یک مولکول اسید چرب با کوآنزیم A (CoA) برای تشکیل یک اسید چرب آسیل-CoA است. در معادلات 2 ، 3 و 4 ، کربن بتا (کربن دوم از سمت راست) اسید چرب آسیل-CoA با مولکول اکسیژن در تعامل است و در نتیجه کربن بتا را اکسید می کند.
در سمت راست معادله 5 قسمت دو کربنی از مولکول جدا شده و استیل-CoA تشکیل شده و در مایع خارج سلول آزاد می شود. در همان زمان ، یک مولکول CoA دیگر با انتهای قسمت باقیمانده مولکول اسید چرب برهم کنش می کند و دوباره آسیل-CoA اسید چرب را تشکیل می دهد. مولکول اسید چرب در این زمان با 2 اتم کربن کوتاهتر می شود ، زیرا اولین استیل-کوآ از ترمینال خود جدا شده است.
سپس این کوتاه شد مولکول اسید چرب acyl-CoA 1 مولکول استیل-CoA دیگر آزاد می کند ، که منجر به کوتاه شدن مولکول اسید چرب اصلی توسط 2 اتم کربن دیگر می شود. علاوه بر آزاد سازی مولکول های استیل-CoA از مولکول های اسید چرب ، 4 اتم کربن نیز در طی این فرآیند آزاد می شود.
اکسیداسیون استیل-CoA... مولکولهای استیل-CoA در طی فرآیند اکسیداسیون بتا اسیدهای چرب در میتوکندری تشکیل شده و بلافاصله وارد چرخه اسید سیتریک می شوند و در تعامل اصلی با اسید اگزالیک-استیک ، اسید سیتریک تشکیل می دهند که متعاقباً توسط اسید شیمیوزیته اکسید می شود. سیستم های اکسیداسیون میتوکندری. عملکرد خالص واکنش چرخه اسید سیتریک در هر 1 مولکول استیل-CoA:
CH3COCoA + اسید اگزالیک استیک + 2H20 + ADP \u003d\u003e 2CO2 + 8H + HCoA + ATP + اسید اگزالیک استیک.
بنابراین ، پس از مقدماتی تجزیه اسیدهای چرب با تشکیل استیل-CoA ، تجزیه نهایی آنها به همان روش تجزیه استیل-CoA تشکیل شده از اسید پیرویک در طول متابولیسم گلوکز انجام می شود. اتمهای هیدروژن حاصل توسط همان سیستم اکسیداسیون میتوکندریایی که در اکسیداسیون کربوهیدراتها با تشکیل مقدار زیادی آدنوزین تری فسفات استفاده می شود ، اکسید می شوند.
وقتی اسیدهای چرب اکسید می شوند مقدار زیادی ATP تشکیل می شود. شکل نشان می دهد که 4 اتم هیدروژن آزاد شده در طی جداسازی استیل-CoA از زنجیره اسیدهای چرب به صورت FADH2 ، NAD-H و H + آزاد می شود ، بنابراین ، هنگام تجزیه 1 مولکول اسید استئاریک ، علاوه بر 9 مولکول استیل-CoA ، 32 مورد دیگر یک اتم هیدروژن. در روند تقسیم هر یک از 9 مولکول استیل-CoA در چرخه اسید سیتریک ، 8 اتم هیدروژن دیگر آزاد می شود که در نهایت 72 اتم هیدروژن می دهد.
در مجموع در تجزیه 1 مولکول اسید استئاریک ، 104 اتم هیدروژن آزاد می شود. از این مجموع ، 34 اتم هنگام اتصال به فلاوپروتئین ها آزاد می شوند و 70 باقیمانده به صورت متصل به نیكوتین آمید آدنین دینوكلئوتید ، یعنی به صورت NAD-H + \u200b\u200bو H +.
اکسیداسیون هیدروژنمرتبط با این دو نوع ماده در میتوکندری انجام می شود ، اما آنها در نقاط مختلف وارد فرآیند اکسیداسیون می شوند ، بنابراین ، اکسیداسیون هر یک از 34 اتم هیدروژن مرتبط با فلاوپروتئین ها منجر به آزاد شدن 1 مولکول ATP می شود. 1.5 مولکول ATP دیگر از هر 70 NAD + و H + سنتز می شود. این در طی اکسیداسیون هیدروژن ، 34 مولکول ATP دیگر (یعنی به طور کلی 139 مولکول) را در اختیار شما قرار می دهد ، که در طی اکسیداسیون هر مولکول اسید استئاریک جدا می شود.
9 مولکول ATP اضافی در چرخه اسید سیتریک (علاوه بر ATP حاصل از اکسیداسیون هیدروژن) ، 1 برای هر یک از 9 مولکول استیل-CoA متابولیزه شده تشکیل می شود. بنابراین ، با اکسیداسیون کامل 1 مولکول اسید استئاریک ، در مجموع 148 مولکول ATP تشکیل می شود. با توجه به اینکه اثر متقابل اسید استئاریک با CoA در مرحله اولیه متابولیسم این اسید چرب ، 2 مولکول ATP را مصرف می کند ، بازده خالص ATP 146 مولکول است.
بازگشت به فهرست بخش ""
اسیدهای چرب بالاتر غیر اشباع (اولئیک ، لینولئیک ، لینولنیک و غیره) از قبل به اسیدهای اشباع تقلیل می یابند.
علاوه بر اکسیداسیون β ، که فرآیند اصلی تخریب اسیدهای چرب در حیوانات و انسان است ، اکسیداسیون α و اکسیداسیون ω نیز وجود دارد. α-اکسیداسیون در هر دو گیاه و حیوانات رخ می دهد ، با این حال ، کل فرآیند در پراکسی زوم ها اتفاق می افتد. ω-اکسیداسیون در میان حیوانات (مهره داران) کمتر مشاهده می شود و عمدتا در گیاهان اتفاق می افتد. روند اکسیداسیون ω در شبکه آندوپلاسمی (ER) صورت می گیرد.
تاریخ
اکسیداسیون β در سال 1904 توسط یک شیمی دان آلمانی کشف شد فرانتس نوپ (فرانتس نوپ) در آزمایش با تغذیه سگها با اسیدهای چرب مختلف ، که در آن یک اتم هیدروژن در انتهای اتم کربن ω-C گروه متیل -CH3 با رادیکال فنیل -C6 H5 جایگزین شد.
فرانتس نوپ پیشنهاد کرد که اکسیداسیون یک مولکول اسید چرب در بافت های بدن در موقعیت β رخ می دهد. در نتیجه ، قطعات بی کربن در کنار گروه کربوکسیل به ترتیب از مولکول اسید چرب جدا می شوند.
تئوری اکسیداسیون β اسیدهای چرب ، پیشنهاد شده توسط F. Knoop ، تا حد زیادی به عنوان پایه ای برای مفاهیم مدرن مکانیسم اکسیداسیون اسیدهای چرب عمل می کند.
فرآیندهای متابولیک
β-اکسیداسیون دنباله ای از فرآیندها است:
فعال سازی اسیدهای چرب
اسیدهای چرب که در اثر هیدرولیز تری اسیل گلیسیرید در سلول ایجاد می شوند یا از خون وارد آن می شوند ، باید فعال شوند ، زیرا آنها خود ماده بی اثر متابولیکی هستند و بنابراین نمی توانند تحت واکنش های بیوشیمیایی ، از جمله اکسیداسیون قرار بگیرند. روند فعال سازی آنها در سیتوپلاسم با مشارکت ATP ، کوآنزیم A (HS-CoA) و یون های Mg 2+ رخ می دهد. این واکنش توسط آنزیم اسید چرب زنجیره بلند acyl-CoA سنتتاز کاتالیز می شود ( لیگاز زنجیره بلند-اسید چرب-CoA، EC 6.2.1.3) ، فرآیند درون زا است ، یعنی به دلیل استفاده از انرژی هیدرولیز مولکول ATP رخ می دهد:
R - C O O H + A T P + C o A - S H → M g 2 + R - C O S - C o A + A M P + H 4 P 2 O 7. (\\ displaystyle (\\ mathsf (R-COOH + ATP + CoA-SH (\\ xrightarrow [()] (Mg ^ (2 +))] R-COS-CoA + AMP + H_ (4) P_ (2) O_ ( 7))).)سنتزهای acyl-CoA هم در سیتوپلاسم و هم در ماتریس میتوکندری یافت می شوند. ویژگی این آنزیم ها برای اسیدهای چرب با طول های مختلف زنجیره هیدروکربن متفاوت است. اسیدهای چرب زنجیره کوتاه و متوسط \u200b\u200b(4 تا 12 اتم کربن) می توانند در ماتریس میتوکندری پخش شوند. فعال شدن این اسیدهای چرب در ماتریس میتوکندری رخ می دهد.
اسیدهای چرب با زنجیره بلند ، که در بدن انسان غالب هستند (12 تا 20 اتم کربن) ، توسط سنتزهای اسیل-کوآ واقع در خارج از غشا میتوکندری خارجی فعال می شوند.
پیرو فسفات آزاد شده در طی واکنش توسط آنزیم پیروفسفاتاز هیدرولیز می شود (EC 3.6.1.1):
H 4 P 2 O 7 + H 2 O → 2 H 3 P O 4. (\\ displaystyle (\\ mathsf (H_ (4) P_ (2) O_ (7) + H_ (2) O \\ rightarrow 2H_ (3) PO_ (4)).)در این حالت ، تعادل واکنش به سمت تشکیل آسیل-CoA تغییر جهت می دهد.
از آنجا که روند فعال سازی اسیدهای چرب در سیتوپلاسم رخ می دهد ، انتقال بیشتر آسیل CoA از طریق غشا به داخل میتوکندری مورد نیاز است.
انتقال اسیدهای چرب از طریق غشای میتوکندریایی
سیستم حمل و نقل کارنیتین. نمودار ساختار و مکانیسم انتقال اسیدهای چرب به شکل آسیل-CoA را نشان می دهد. اسیدهای چرب آزاد (FFA) با طول زنجیره کوتاه و متوسط \u200b\u200bبه شکل استرها - آسیل-کوآ به راحتی از طریق غشاهای میتوکندری پخش می شوند ، با این حال ، بیشتر این اسیدهای چرب دارای زنجیره هیدروکربن طولانی هستند که اجازه عبور آزاد از آنها را نمی دهد. این به یک حامل نیاز دارد ، کارنیتین نقش آن را بازی می کند - 1 ... در سطح غشای خارجی میتوکندری ، یک آنزیم وجود دارد - کارنیتین-پالمیتوئیل ترانسفراز I (CPT1) ، که کارنیتین آزاد را به آسیل کارنیتین (کارنیتین-COR) استیل می کند - 2 ، که متعاقباً از طریق غشا outer خارجی پخش می شود و به فضای بین غشایی نفوذ می کند. غشا inner میتوکندری داخلی برای آسیل کارنیتین نفوذ ناپذیر است ؛ برای عبور از آن ، ترانسلوکاز کاریلیتین آسیل کارنیتین (CACT) وجود دارد ، که اجازه می دهد آن را به ماتریکس منتقل کنیم. علاوه بر این ، آسیل کارنیتین تحت فرآیند معکوس قرار می گیرد - شکاف تحت اثر آنزیم کارنیتین palmitoyltransferase II (CPT2) و پوشش A به کارنیتین آزاد و آسیل CoA ، که برای اکسیداسیون β ارائه می شود. کارنیتین رایگان 1 توسط همان ترانسلوكاز از طریق غشای داخلی به فضای بین غشایی میتوكندری منتقل می شود و سپس در سیتوپلاسم پخش می شود.
انتقال اسیدهای چرب زنجیره بلند از طریق غشا membrane متراکم میتوکندری از طریق کارنیتین انجام می شود. در غشای خارجی میتوکندری یک آنزیم کارنیتین آسیل ترانسفراز I (کارنیتین پالمیتوئیل ترانسفراز I ، CPT1 ، EC 2.3.1.21) وجود دارد ، که واکنش را با تشکیل آسیل کارنیتین کاتالیز می کند (گروه آسیل از اتم گوگرد CoA به گروه هیدروکسیل کارینین کارینین تبدیل می شود) در غشای داخلی میتوکندری منتشر می شود:
R-CO ~ SCoA + کارنیتین ↔ کارنیتین-COR + CoA-SH
آسیل کارنیتین حاصل از فضای بین غشایی به خارج غشا inner داخلی منتقل می شود و توسط آنزیم کارنیتین آسیل کارنیتین ترانسلوکاز (CACT) منتقل می شود.
پس از عبور آسیل کارنیتین (کارنیتین-COR) از غشا mit میتوکندری ، عکس العمل متفاوتی رخ می دهد - تجزیه آسیل کارنیتین با مشارکت CoA-SH و آنزیم carnitinacyl-CoA-transferase یا carnitine acyltransferase II (carnitine palmitoyltransferase II)
CoA-SH + کارنیتین-COR ↔ R-CO ~ S CoA + کارنیتین
بنابراین ، آسیل CoA برای آنزیم های اکسیداسیون β در دسترس قرار می گیرد. کارنیتین آزاد توسط همان ترانسلوکاز به سمت سیتوپلاسمی غشا mit میتوکندری داخلی برگردانده می شود.
پس از آن ، آسیل CoA در واکنش اکسیداسیون β قرار می گیرد.
روند انتقال اسیدهای چرب غشایی را می توان توسط مالونیل-CoA مهار کرد.
اکسیداسیون اسیدهای چرب داخل میتوکندریایی
در ماتریس میتوکندری ، اسیدهای چرب در چرخه Knoopp - Linen اکسید می شوند. این شامل چهار آنزیم است که به ترتیب بر روی acyl-CoA عمل می کنند. متابولیت نهایی این چرخه استیل-CoA است. این فرایند خود شامل چهار واکنش است.
| نام واکنش | طرح واکنش | آنزیم | محصول حاصل |
|---|---|---|---|
| دهیدروژناسیون اسید چرب فعال شده (acyl-CoA)... اکسیداسیون β با کم آبی هیدروژناسیون آسیل CoA توسط اسید چرب دهیدروژناز زنجیره بلند وابسته به FAD (LCAD) با تشکیل پیوند دوگانه بین اتم های α- و β-کربن (C-2 و C-3) در محصول واکنش آغاز می شود. -KoA کوآنزیم FADH 2 کاهش یافته در این واکنش ، اتم های هیدروژن موجود در ETC را به کوآنزیم Q منتقل می کند. در نتیجه ، 2 مولکول ATP سنتز می شود. | acyl-CoA دهیدروژناز (EC 1.3.99.3) | ترانس-Δ 2 -نویل-CoA | |
| واکنش هیدراتاسیون... آسیل-CoA غیر اشباع (enoyl-CoA) ، با مشارکت آنزیم enoyl-CoA هیدراتاز ، یک مولکول آب را متصل می کند. نتیجه β-hydroxyacyl-CoA است. واکنش برگشت پذیر و کلیشه ای است ؛ محصول حاصل فرم L دارد. | Enoyl-CoA-hydratase (EC 4.2.1.17) | L-β-هیدروکسی آسیل-CoA | |
| NAD + - اکسیداسیون وابسته یا واکنش دهیدروژناسیون دوم... سپس L-β-هیدروکسیاسیل-CoA حاصل اکسید می شود. واکنش توسط دهیدروژناز وابسته به NAD + کاتالیز می شود. | L-β-هیدروکسی استیل دهیدروژناز (EC 1.1.1.35) | L-β-ketoacyl-CoA | |
| واکنش تیولاز... در این واکنش ، β-ketoacyl-CoA با کوآنزیم A تعامل می کند. در نتیجه ، β-ketoacyl-CoA شکافته شده و آسیل-CoA توسط دو اتم کربن کوتاه و یک قطعه دو کربنی به شکل استیل-CoA تشکیل می شود. این واکنش توسط استیل-CoA آسیل ترانسفراز (یا β-ketothiolase) کاتالیز می شود. | β-ketothiolase (EC 2.3.1.9) | آسیل CoA و استیل CoA |
استیل CoA تشکیل شده در چرخه کربس دچار اکسیداسیون می شود و آسیل CoA که توسط دو اتم کربن کوتاه می شود ، مجدداً کل مسیر اکسیداسیون β را چندین بار طی می کند تا تشکیل بوتیریل-CoA (ترکیب 4 کربنی) ، که به نوبه خود به 2 مولکول اکسید می شود. استیل-CoA. FADH 2 و NADH · H مستقیماً به زنجیره تنفسی می روند.
برای تخریب کامل یک اسید چرب با زنجیره بلند ، چرخه باید چندین بار تکرار شود ، به عنوان مثال ، برای استریل-کوآ (C 17 H 35 CO ~ SCoA) ، هشت چرخه لازم است.
ویژگی های اکسیداسیون اسیدهای چرب با تعداد عجیب اتم های کربن
در نتیجه اکسیداسیون اسیدهای چرب با تعداد عجیب و غریب اتم های کربن ، نه تنها استیل-CoA ، FAD H2 و NADH بلکه یک مولکول پروپیونیل-CoA (C 2 H 5 -CO ~ SCoA) نیز تشکیل می شود.
اکسیداسیون اسیدهای چرب اشباع نشده
اکسیداسیون اسیدهای چرب با دو پیوند غیر اشباع (-C \u003d C-C-C \u003d C-) و بیشتر به یک آنزیم اضافی دیگر β-hydroxyacyl-CoA-epimerase (EC 1.1.1.35) احتیاج دارد.
میزان اکسیداسیون اسیدهای چرب اشباع نشده بسیار بیشتر از اسیدهای چرب اشباع نشده است که به دلیل وجود پیوندهای دوتایی است. به عنوان مثال ، اگر میزان اکسیداسیون اسید استئاریک اشباع شده را به عنوان استاندارد در نظر بگیریم ، در این صورت میزان اکسیداسیون اسید اولئیک در 11 ، لینولئیک در 114 ، لینولنیک در 170 و اسید آراشیدونیک تقریباً 200 برابر بیشتر از اسید استئاریک است.
اکسیداسیون بتا در گیاهان
تراز انرژی فرآیند
در نتیجه انتقال الکترون از طریق ETC از FAD H 2 و NADH ، 5 مولکول ATP سنتز می شود (2 مولکول از FADH 2 و 3 مولکول از NADH). در مورد اکسیداسیون اسید پالمیتیک ، 7 چرخه اکسیداسیون β (7 / 16-1 / 2-16) طی می شود که منجر به تشکیل 5 مولکول ATP \u003d 7 7 \u003d 35 می شود. در فرآیند اکسیداسیون β اسید پالمیتیک ، n مولکولهای استیل-CoA ، هر کدام از آنها ، با احتراق کامل در چرخه اسید تریکاربوکسیلیک ، 12 مولکول ATP می دهد و 8 مولکول ، 12 مولکول ATP 96 \u003d 8 می دهد.
بنابراین ، در مجموع ، با اکسیداسیون کامل اسید پالمیتیک ، 131 \u003d 131 مولکول ATP تشکیل می شود. با این حال ، با در نظر گرفتن یک مولکول ATP ، که به AMP هیدرولیز می شود ، یعنی 2 پیوند با انرژی بالا یا دو ATP هزینه می شود ، در ابتدای کار برای فرآیند فعال سازی (تشکیل palmitoyl-CoA) ، کل انرژی تولیدی با اکسیداسیون کامل یک مولکول اسید پالمیتیک در شرایط بدن یک حیوان 131 خواهد بود -2 \u003d 129 مولکول.
معادله کلی اکسیداسیون اسید پالمیتیک به شرح زیر است:
C 15 H 31 CO - SC o A + 7 FAD + + 7 NAD + + 7 H 2 O + 7 HS - C o A → 8 CH 3 CO - SC o A + 7 FADH 2 + 7 NADH (\\ سبک نمایش (\\ 7NADH)))فرمول محاسبه مقدار کل ATP تولید شده توسط فرآیند اکسیداسیون β:
[(n 2 ⋅ 12) + ((n 2 - 1) 5)] (\\ displaystyle (\\ left [((\\ frac (n) (2)) \\ cdot 12) + (((\\ frac (n) (2)) - 1) \\ cdot 5) \\ راست]))جایی که n - تعداد اتم های کربن در یک مولکول اسید چرب.
محاسبه انرژی اکسیداسیون β برای برخی از اسیدهای چرب به صورت جدول ارائه شده است.
| اسید چرب | تعداد مولکولهای ATP تولید شده در هر 1 مولکول اسید چرب | تعداد مولکولهای ATP مصرف شده | عملکرد کل انرژی مولکولهای ATP |
|---|---|---|---|
| اسید کاپریلیک C 7 H 15 COOH | 63 | 2 | 63-2=61 |
| اسید لوریک С 11 Н 23 COOH | 97 | 2 | 97-2=95 |
| اسید میریستیک C 13 H 27 COOH | 114 | 2 | 114-2=112 |
| اسید پنتادسیلیک C 14 H 29 COOH | 122,5 | 2 | 122,5-2=120,5 |
| اسید پالمیتیک C 15 H 31 COOH | 131 | 2 | 131-2=129 |
| اسید مارگاریک C 16 H 33 COOH | 139,5 | 2 | 139,5-2=137,5 |
| اسید استئاریک C 17 H 35 COOH | 148 | 2 | 148-2=146 |
| آراشیدید اسید C 19 H 39 COOH | 165 | 2 | 165-2=163 |
اکسیداسیون اسیدهای چرب خارج سلولی
علاوه بر اکسیداسیون β اسیدهای چرب ، که در میتوکندری اتفاق می افتد ، اکسیداسیون خارج از میتوکندری نیز وجود دارد. اسیدهای چرب با طول زنجیره طولانی تر (از C 20) به دلیل وجود غشای دوگانه متراکم ، که از روند انتقال آنها از طریق فضای بین غشایی جلوگیری می کند ، نمی توانند در میتوکندری اکسید شوند. بنابراین ، اکسیداسیون اسیدهای چرب زنجیره بلند (C 20-C 22 و بیشتر) در پراکسیزوم ها رخ می دهد. در پراکسی زوم ها ، اکسیداسیون β اسیدهای چرب به شکل اصلاح شده رخ می دهد. محصولات اکسیداسیون در این مورد استیل-CoA ، اکتانوئیل-CoA و پراکسید هیدروژن H 2 O 2 است. استیل-CoA در مرحله ای که توسط دهیدروژناز وابسته به FAD کاتالیز می شود ، تشکیل می شود. آنزیم های پراكسیزوم به اسیدهای چرب زنجیره كوتاه حمله نمی كنند و با تشكیل اكتانوئیل-CoA روند اکسیداسیون β متوقف می شود.
این فرآیند با فسفوریلاسیون اکسیداتیو و تولید ATP همراه نیست و بنابراین اکتانوئیل-CoA و استیل-CoA از CoA به کارنیتین منتقل می شوند و به میتوکندری فرستاده می شوند و در آنجا اکسید می شوند تا ATP تشکیل شود.
فعال شدن اکسیداسیون β پراکسیزومی هنگامی رخ می دهد که مقدار زیادی اسیدهای چرب در غذای مصرفی وجود داشته باشد ، از C 20 شروع می شود و همچنین هنگام مصرف داروهای کاهش چربی خون.
مقررات
میزان تنظیم فرآیند اکسیداسیون β شامل چندین فاکتور است:
میزان اکسیداسیون β نیز به فعالیت آنزیم کارنیتین palmitoyltransferase I (CPTI) بستگی دارد. در کبد ، این آنزیم توسط مالونیل-CoA ، ماده ای که در طی بیوسنتز اسیدهای چرب تشکیل شده است ، مهار می شود.
در عضلات ، کارنیتین پالمیتوئیل ترانسفراز I (CPTI) نیز توسط مالونیل-CoA مهار می شود. اگرچه بافت عضلانی اسیدهای چرب را سنتز نمی کند ، اما حاوی ایزوآنزیم استیل CoA کربوکسیلاز است که مالونیل CoA را برای تنظیم اکسیداسیون β ترکیب می کند. این ایزوآنزیم توسط پروتئین کیناز A که در سلولها توسط آدرنالین و توسط پروتئین کیناز وابسته به AMP در سلولها فعال می شود فسفریله می شود و بنابراین مهار می شود. غلظت مالونیل-CoA کاهش می یابد. در نتیجه ، در حین کار فیزیکی ، هنگامی که AMP در سلول ظاهر می شود ، اکسیداسیون β تحت عمل آدرنالین فعال می شود ، با این حال ، سرعت آن نیز به دسترسی اکسیژن بستگی دارد. بنابراین ، اکسیداسیون β تنها 10-20 دقیقه پس از شروع فعالیت بدنی (به اصطلاح ورزش هوازی) ، هنگامی که جریان اکسیژن به بافت ها افزایش می یابد ، به یک منبع انرژی برای عضلات تبدیل می شود.
بی نظمی فرآیند
نقص در سیستم حمل و نقل کارنیتین
نقص در سیستم حمل و نقل کارنیتین در تخمیر و وضعیتهای کمبود کارنیتین در بدن انسان نمایان می شود.
شرایط کمبود کارنیتین
شایع ترین شرایط کمبود مربوط به از دست دادن کارنیتین در طی برخی شرایط خاص بدن:
علائم و نشانه های کمبود کارنیتین حملات هیپوگلیسمی ناشی از کاهش گلوکونئوژنز در نتیجه نقض اکسیداسیون β اسیدهای چرب ، کاهش در تشکیل بدن کتون ، همراه با افزایش محتوای اسیدهای چرب آزاد (FFA) در پلاسمای خون ، ضعف عضلانی (میاستنی گراویس) و همچنین تجمع چربی.
تخمیری
اختلالات ژنتیکی اسید چرب زنجیره متوسط \u200b\u200bاسید- CoA دهیدروژنازها
در میتوکندری ، 3 نوع ازیل-CoA دهیدروژناز وجود دارد که اسیدهای چرب را با یک زنجیره رادیکال بلند ، متوسط \u200b\u200bیا کوتاه اکسید می کند. با کوتاه شدن رادیکال در طی اکسیداسیون β ، می توان اسیدهای چرب را به ترتیب توسط این آنزیم ها اکسید کرد. نقص ژنتیکی در دهیدروژناز اسیدهای چرب با طول رادیکال متوسط \u200b\u200b(EC 1.3.8.7) - MCADD (به اختصار از مادیوم- جهین آcyl-CoA دهیدروژناز دکارآیی) شایعترین در مقایسه با سایر بیماریهای ارثی است - 1:15 000. فراوانی ژن معیوب آکادمکدگذاری برای دهیدروژنازهای acyl-CoA اسیدهای چرب متوسط \u200b\u200bزنجیره ای در میان جمعیت اروپا - 1:40. این یک بیماری اتوزومی مغلوب است که در نتیجه جایگزینی نوکلئوتید T (تیمین) با A (آدنین) در موقعیت 985 ژن ایجاد می شود. این خود را در تجمع اسیدهای چرب متوسط \u200b\u200bزنجیره ای (به ویژه کاپریلیک) و مشتقات آنها در خون و کمبود ثانویه کارنیتین نشان می دهد. علائم معمول عبارتند از حملات استفراغ ، بی حالی ، هیپوگلیسمی شدید غیر کتوتیک ناشی از استفاده زیاد از گلوکز (به خصوص برای نوزادان خطرناک) ، ممکن است کما ایجاد شود و مرگ امکان پذیر است. این بیماری در کودکان بسیار خطرناک است ، زیرا در میان آنها بیشترین مرگ و میر (تا 60٪) مشاهده می شود.
اختلالات ژنتیکی دهیدیل هیدروژنازهای acyl-CoA اسیدهای چرب زنجیره کربن بسیار طولانی
دی کربوکسیلیک اسیدوریا
دی کربوکسیلیک اسیدوریا یک بیماری همراه با افزایش دفع اسیدهای C6-C10-دیکاربوکسیلیک و هیپوگلیسمی ناشی از این زمینه است ، اما با افزایش محتوای اجسام کتون همراه نیست. علت این بیماری MCADD است. در این حالت ، اکسیداسیون β مختل می شود و اکسیداسیون ω اسیدهای چرب با زنجیره بلند افزایش می یابد ، که به اسیدهای دی کربوکسیلیک با زنجیره متوسط \u200b\u200bکوتاه می شوند که از بدن دفع می شوند.
سندرم زلوگر
سندرم زلوگر یا سندرم مغز خون ، یک بیماری ارثی نادر است که توسط پزشک متخصص اطفال آمریکایی هانس زلوگر (انگلیسی H.U. Zellweger) توصیف شده است ، که خود را در غیاب پراکسی زوم ها در تمام بافت های بدن نشان می دهد. در نتیجه ، بدن ، به ویژه مغز ، اسیدهای پلی اونیک (C 26-C 38) را که اسیدهای چرب با زنجیره طولانی هستند ، تجمع می دهد. برآورد میزان بروز اختلالات بیوژنز پراکسیزوم در طیف سندرم زلوگر 1: 50،000 نوزاد در ایالات متحده و 1: 500،000 نوزاد در ژاپن است. این سندرم با موارد زیر مشخص می شود: افت فشار خون عضلانی مشکل مکیدن آرفلکسی dolichocephaly؛ پیشانی بلند صورت صاف گرد پلک های پف کرده؛ هیپرترولیسم بخش چشم مغولوئید ؛
و زنجیره تنفسی برای تبدیل انرژی موجود در اسیدهای چرب به انرژی پیوندهای ATP.
اکسیداسیون اسیدهای چرب (اکسیداسیون β)
طرح ابتدایی اکسیداسیون β.
از آنجا که سومین اتم کربن اسید چرب (موقعیت β) به گروه کربوکسیل اکسید می شود ، این مسیر اکسیداسیون β نامیده می شود ، در حالی که گروه استیل ، از جمله C 1 و C 2 اسید چرب اصلی ، از اسید جدا می شود.
واکنشهای اکسیداسیون Β در میتوکندری اکثر سلولهای بدن (به جز سلولهای عصبی) رخ می دهد. برای اکسیداسیون ، از اسیدهای چرب استفاده می شود که از خون وارد سیتوزول می شود یا در طی لیپولیز TAG های داخل سلول خود ظاهر می شود. معادله کلی اکسیداسیون اسید پالمیتیک به شرح زیر است:
Palmitoyl-SCoA + 7FAD + 7NAD + + 7H 2 O + 7HS-KoA → 8Acetyl-SCoA + 7FADH 2 + 7NADH
مراحل اکسیداسیون اسیدهای چرب

واکنش فعال سازی اسیدهای چرب.
1. قبل از نفوذ به داخل ماتریس میتوکندری و اکسید شدن ، اسید چرب باید در سیتوزول فعال شود. این کار با اتصال کوآنزیم A به آن و تشکیل آسیل-S-CoA انجام می شود. Acyl-S-CoA یک ترکیب پر انرژی است. برگشت ناپذیری واکنش با هیدرولیز دی فسفات به دو مولکول اسید فسفریک حاصل می شود.

انتقال اسیدهای چرب وابسته به کارنیتین به میتوکندری ها.
2. Acyl-S-CoA قادر به عبور از غشای میتوکندری نیست ، بنابراین راهی برای انتقال آن در ترکیب با ماده ویتامین مانند کارنیتین وجود دارد. غشا mit میتوکندری خارجی حاوی آنزیم کارنیتین آسیل ترانسفراز I است.
کارنیتین در کبد و کلیه ها سنتز می شود و سپس به اندام های دیگر منتقل می شود. در دوره قبل از تولد و در سالهای اول زندگی ، ارزش کارنیتین برای بدن بسیار زیاد است. تأمین انرژی سیستم عصبی بدن کودک و به ویژه مغز از طریق دو فرآیند موازی انجام می شود: اکسیداسیون اسیدهای چرب وابسته به کارنیتین و اکسیداسیون هوازی گلوکز. کارنیتین برای رشد مغز و نخاع ، برای تعامل تمام قسمتهای سیستم عصبی مسئول حرکت و تعامل عضلات ضروری است. مطالعاتی وجود دارد که فلج مغزی نوزاد و پدیده "مرگ در گهواره" را با کمبود کارنیتین مرتبط می کند.
3. پس از اتصال به کارنیتین ، اسید چرب توسط ترانسلوکاز از طریق غشا منتقل می شود. در اینجا ، در سمت داخلی غشا ، آنزیم کارنیتین آسیل ترانسفراز II دوباره آسیل-S-CoA را تشکیل می دهد که وارد مسیر اکسیداسیون β می شود.

توالی واکنش اکسیداسیون β اسیدهای چرب.
4- فرآیند اکسیداسیون β خود شامل 4 واکنش است که به صورت چرخشی تکرار می شوند. اکسیداسیون (آسیل-SCoA-دهیدروژناز) ، هیدراتاسیون (انوئیل-SCoA-هیدراتاز) و اکسیداسیون سومین اتم کربن (هیدروکسیاسیل-SCoA-دهیدروژناز) به ترتیب در آنها رخ می دهد. در آخرین واکنش ترانسفراز ، استیل-SCoA از اسید چرب جدا می شود. HS-CoA به اسید چرب باقیمانده (با دو کربن کوتاه شده) اضافه می شود و به اولین واکنش برمی گردد. همه چیز تکرار می شود تا اینکه در آخرین چرخه دو استیل-SCoA تشکیل می شود.
محاسبه تعادل انرژی اکسیداسیون β
هنگام محاسبه مقدار ATP تشکیل شده در طی اکسیداسیون β اسیدهای چرب ، توجه به موارد زیر ضروری است:
- مقدار استیل-SCoA تشکیل شده توسط تقسیم معمول تعداد اتمهای کربن در یک اسید چرب به 2 تعیین می شود.
- تعداد چرخه های اکسیداسیون β. تعداد چرخه های اکسیداسیون β را می توان بر اساس مفهوم اسید چرب به عنوان زنجیره ای از واحدهای دو کربنی به راحتی تعیین کرد. تعداد وقفه ها بین واحدها مربوط به تعداد چرخه های اکسیداسیون β است. همان مقدار را می توان با فرمول (n / 2 − 1) محاسبه کرد ، جایی که n تعداد اتم های کربن در اسید است.
- تعداد پیوندهای دوگانه در اسید چرب. در اولین واکنش اکسیداسیون β ، یک پیوند دوگانه با مشارکت FAD تشکیل می شود. اگر قبلاً پیوند مضاعفی در اسید چرب وجود داشته باشد ، دیگر نیازی به این واکنش نیست و FADH 2 تشکیل نمی شود. تعداد FADH 2 اصلاح نشده مربوط به تعداد پیوندهای دوتایی است. بقیه واکنشهای چرخه بدون تغییر می مانند.
- مقدار انرژی ATP صرف شده برای فعال سازی (همیشه مربوط به دو پیوند پرانرژی است).
مثال. اکسیداسیون اسید پالمیتیک
- از آنجا که 16 اتم کربن وجود دارد ، پس طی اکسیداسیون β 8 مولکول استیل-SCoA تشکیل می شود. دومی وارد CTK می شود ، وقتی در یک دور چرخه اکسید شود ، 3 مولکول NADH ، 1 مولکول FADH 2 و 1 مولکول GTP تشکیل می شود که معادل 12 مولکول ATP است (همچنین به روش های به دست آوردن انرژی در سلول نیز مراجعه کنید). بنابراین ، 8 مولکول استیل-S-CoA تشکیل 8 × 12 \u003d 96 مولکول ATP را فراهم می کند.
- برای اسید پالمیتیک ، تعداد چرخه های اکسیداسیون β 7 است. هر چرخه 1 مولکول FADH2 و 1 مولکول NADH تولید می کند. وارد زنجیره تنفسی می شوند ، در مجموع 5 مولکول ATP "می دهند". بنابراین ، در 7 چرخه ، 7 × 5 \u003d 35 مولکول ATP تشکیل می شود.
- هیچ پیوند دوگانه ای در اسید پالمیتیک وجود ندارد.
- 1 مولکول ATP برای فعال سازی یک اسید چرب استفاده می شود ، که با این حال ، به AMP هیدرولیز می شود ، یعنی 2 پیوند با انرژی بالا یا دو ATP مصرف می شود.
بنابراین ، به طور خلاصه ، ما 969 + 35-2 \u003d 129 مولکول ATP به دست می آوریم که در طی اکسیداسیون اسید پالمیتیک تشکیل شده اند.
"اسیدهای چرب آزاد" (FFA) به اسیدهای چرب گفته می شود که به صورت غیر تصفیه شده هستند. گاهی اوقات به عنوان اسیدهای چرب غیراستری (EFA) نامیده می شوند. در پلاسمای خون ، FFA های زنجیره بلند با آلبومین و در سلول - با پروتئینی که اسیدهای چرب را متصل می کند ، که پروتئین Z نامیده می شود ، یک مجموعه را تشکیل می دهند. در واقع ، آنها هرگز آزاد نیستند. اسیدهای چرب با زنجیره کوتاه در آب محلول ترند و یا به صورت اسید غیر یونیزه یا به عنوان آنیون اسید چرب یافت می شوند.
فعال سازی اسیدهای چرب
همانطور که در مورد متابولیسم گلوکز ، اسید چرب قبل از هر چیز باید در نتیجه واکنش شامل ATP به یک مشتق فعال تبدیل شود و فقط پس از آن قادر به تعامل با آنزیم هایی است که تبدیل بیشتر را کاتالیز می کنند. در فرآیند اکسیداسیون اسیدهای چرب ، این مرحله تنها مرحله ای است که به انرژی به شکل ATP نیاز دارد. در حضور ATP و کوآنزیم A ، آنزیم آسیل-کوآ سنتتاز (تیوکیناز) تبدیل یک اسید چرب آزاد به "اسید چرب فعال" یا آسیل-CoA را کاتالیز می کند ، که با تجزیه یک پیوند فسفات غنی از انرژی واحد انجام می شود.
وجود پیرو فسفاتاز غیر آلی ، که پیوند فسفات غنی از انرژی در پیرو فسفات را می شکافد ، کامل بودن فرایند فعال سازی را تضمین می کند. بنابراین ، برای فعال سازی یک مولکول اسید چرب ، در نهایت دو پیوند فسفات غنی از انرژی مصرف می شود.

سنتزهای اسیل-کوآ در شبکه آندوپلاسمی و همچنین در داخل میتوکندری و غشای خارجی آنها یافت می شود. تعدادی از ترکیبات آسیل-CoA در ادبیات شرح داده شده است. آنها مخصوص اسیدهای چرب با طول زنجیره خاص هستند.
نقش کارنیتین در اکسیداسیون اسیدهای چرب
کارنیتین یک ترکیب گسترده است

به خصوص مقدار زیادی از آن در عضلات. این ماده از لیزین و متیونین در کبد و کلیه ها تشکیل می شود. فعال سازی اسیدهای چرب پایین و اکسیداسیون آنها می تواند در میتوکندری به طور مستقل از کارنیتین اتفاق بیفتد ؛ با این حال ، مشتقات زنجیره بلند acyl-CoA (یا FFA) نمی توانند به میتوکندری نفوذ کنند و در صورت عدم تشکیل مشتقات آسیل کارنیتین ، اکسید می شوند. در قسمت خارجی غشای داخلی میتوکندری یک آنزیم کارنیتین palmitoyltransferase I وجود دارد که گروههای اسیل با زنجیره بلند را به کارنیتین منتقل می کند تا آسیل کارنیتین تشکیل دهد. دومی قادر به نفوذ به میتوکندری است ، جایی که آنزیم هایی وجود دارد که روند را کاتالیز می کنند (اکسیداسیون -.
مکانیسم احتمالی توضیح مشارکت کارنیتین در اکسیداسیون اسیدهای چرب در میتوکندری در شکل نشان داده شده است. 23.1 علاوه بر این ، میتوکندری حاوی آنزیم دیگری به نام استیل ترانسفراز کارنیتین است که انتقال گروههای آسیل با زنجیره کوتاه بین CoA و کارنیتین را کاتالیز می کند. عملکرد این آنزیم هنوز مشخص نیست.

شکل: 23.1 نقش کارنیتین در انتقال اسیدهای چرب با زنجیره طولانی از طریق غشای داخلی میتوکندری آسیل-CoA با زنجیره بلند قادر به عبور از غشای داخلی میتوکندری نیست ، در حالی که آسیل کارنیتین ، که در اثر عمل کارنیتین-پالمیتونلنتانسفراز I. کارنیتین-آسیل کارنیتین-طرفداران موقعیت ایجاد می شود ، یک سیستم حمل و نقل است. انجام انتقال یک مولکول آسیل کارنیتین از طریق غشای داخلی میتوکندری ، همراه با آزاد سازی mopscule کارنیتین رایگان. سپس ، تحت تأثیر کارنیتین palmitoyltransferase 11 ، موضعی در سطح داخلی غشا membrane میتوکندری داخلی ، آسیل کارنیتین با CoA برهم کنش می کند. در نتیجه ، آسیل-CoA دوباره در ماتریس میتوکندری تشکیل می شود. و کارنیتین آزاد می شود.
شاید،

حمل و نقل گروههای استیل از طریق غشا mit میتوکندری را تسهیل می کند.
b-اکسیداسیون اسیدهای چرب
ایده کلی در شکل ارائه شده است. 23.2 در طی اکسیداسیون 13 اسیدهای چرب ، 2 اتم کربن به طور همزمان از انتهای کربوکسیل مولکول acyl-CoA شکافته می شود. زنجیره کربن در حال شکستن است

شکل: 23.2 طرح اکسیداسیون اسیدهای چرب.
بین اتمهای کربن در موقعیتهایی که نام از آنها بوجود آمده است - اکسیداسیون. قطعات حاصل از دو کربن ، استیل CoA هستند. بنابراین ، در مورد palmitoyl-CoA ، 8 مولکول استیل-CoA تشکیل می شود.
دنباله واکنش ها
تعدادی از آنزیم ها که در مجموع به عنوان اکسیدازهای اسید چرب شناخته می شوند ، در ماتریس میتوکندری در مجاورت بلافاصله زنجیره تنفسی واقع در غشای داخلی میتوکندری یافت می شوند. این سیستم اکسیداسیون آسیل-CoA به استیل-CoA را که با فسفوریلاسیون ADP به ATP همراه است ، کاتالیز می کند (شکل 23.3).
پس از نفوذ قطعه آسیل از طریق غشا mit میتوکندری با مشارکت سیستم حمل و نقل کارنیتین و انتقال گروه آسیل از کارنیتین ، دو اتم هیدروژن از اتمهای کربن در موقعیت های کاتالیز شده توسط آسیل CoA-دهیدروژنازوئیدها شکافته می شوند. محصول این واکنش است. آنزیم یک فلاوپروتئین است ، گروه پروتز آن FAD است. اکسیداسیون دومی در زنجیره تنفسی میتوکندری با مشارکت فلاوپروتئین دیگر اتفاق می افتد. فلاوپروتئین انتقال دهنده الکترون نامیده می شود [نگاه کنید به. از جانب. 123) علاوه بر این ، پیوند دوگانه هیدراته می شود و در نتیجه 3-هیدروکسی آسیل-CoA تشکیل می شود. این واکنش توسط آنزیم A2-enoyl-CoA-hydratase کاتالیز می شود. سپس 3-هیدروکسی آسیل-OoA در اتم 3 کربن دهیدراته می شود و 3-ketoacyl-CoA را تشکیل می دهد. این واکنش توسط 3-hydroxyacyl-CoA دهیدروژناز ، با مشارکت NAD به عنوان کوآنزیم ، کاتالیز می شود. 3-ketoacyl-CoA توسط 3-کتوتیولاز یا استیل-CoA-استیل ترانسفراز بین اتم های دوم و سوم کربن شکافته می شود و مشتقات استیل-CoA- و آسیل-CoA را تشکیل می دهد ، که 2 اتم کربن کوتاه تر از مولکول اصلی acyl-CoA است. این برش تیولیتیک به مشارکت یک مولکول دیگر نیاز دارد. آسیل-CoA کوتاه شده حاصل مجدداً وارد چرخه اکسیداسیون P می شود و با واکنش 2 شروع می شود (شکل 23.3). به این ترتیب ، اسیدهای چرب با زنجیره طولانی می توانند به طور کامل به استیل-CoA (قطعات C2) تجزیه شوند. دومی در چرخه اسید سیتریک ، که در میتوکندری اتفاق می افتد ، به اکسید می شود
اکسیداسیون اسیدهای چرب با تعداد عجیب اتم های کربن
b-اکسیداسیون اسیدهای چرب با تعداد عجیب و غریب از اتمهای کربن در مرحله تشکیل یک قطعه سه کربنی - پروپیونیل-CoA به پایان می رسد ، که سپس به یک واسطه از چرخه اسید سیتریک تبدیل می شود (شکل 20.2 را نیز ببینید).
انرژی اکسیداسیون اسیدهای چرب
در نتیجه انتقال الکترون ها در طول زنجیره تنفسی از فلاوپروتئین کاهش یافته و NAD ، 5 پیوند فسفات غنی از انرژی برای هر 7 (از هر 8) مولکول استیل-CoA که در طی اکسیداسیون b اسید پالمیتیک تشکیل شده است ، سنتز می شود (به فصل 13 مراجعه کنید) در مجموع 8 مولکول استیل تشکیل می شود -CoA ، و هر یک از آنها ، با عبور از چرخه اسید سیتریک ، سنتز 12 پیوند غنی از انرژی را فراهم می کند. در مجموع ، به ازای هر مولکول پالمیتات ، 8 96 12 \u003d 96 پیوند فسفات غنی از انرژی در طول این مسیر تولید می شود. با توجه به دو پیوند لازم برای فعال سازی
(اسکن را ببینید)
شکل: 23.3 P اکسیداسیون اسیدهای چرب. CoA acyte با زنجیره بلند به طور پی در پی کوتاه می شود و پس از چرخه واکنش های آنزیمی 2-5 از طریق cyt عبور می کند. در نتیجه هر چرخه ، استیل-CoA جدا شده و توسط تیولاز کاتالیز می شود (واکنش 5). وقتی رادیکال آسیل چهار کربنی باقی می ماند ، در نتیجه واکنش 5 ، دو مولکول استیل-CoA از آن تشکیل می شود.
اسید چرب ، ما در مجموع 129 پیوند غنی از انرژی در هر مول یا kJ دریافت می کنیم. از آنجا که انرژی آزاد احتراق اسید پالمیتیک حدود 40٪ انرژی ذخیره شده به صورت پیوندهای فسفاته در طی اکسیداسیون اسیدهای چرب است.
اکسیداسیون اسیدهای چرب در پراکسیزوم ها
در پراکسی زوم ها ، اکسیداسیون β اسیدهای چرب به شکل اصلاح شده رخ می دهد. محصولات اکسیداسیون در این مورد استیل-CoA است و دومی در مرحله ای که توسط دهیدروژناز مرتبط با فلاوپروتئین کاتالیز می شود ، تشکیل می شود. این مسیر اکسیداسیون ارتباط مستقیمی با فسفوریلاسیون و تشکیل ATP ندارد ، اما تخریب اسیدهای چرب زنجیره ای بسیار طولانی را امکان پذیر می کند (به عنوان مثال). با رژیم غذایی غنی از چربی یا داروهای کاهنده چربی مانند کلوفیبرات روشن می شود. آنزیم های پراكسی زوم به اسیدهای چرب زنجیره كوتاه حمله نمی كنند و با تشكیل اكتانوئیل-CoA روند اکسیداسیون P متوقف می شود. سپس گروه های اکتانویل و استیل به شکل اکتانوئیل کارنیتین و استیل کارنیتین از پراکسیزوم ها خارج شده و در میتوکندری اکسید می شوند.
a- و b-اکسیداسیون اسیدهای چرب
اکسیداسیون مسیر اصلی کاتابولیسم اسیدهای چرب است. با این حال ، اخیراً کشف شده است که اکسیداسیون β اسیدهای چرب در بافت های مغز رخ می دهد ، به عنوان مثال ، تجزیه متوالی قطعات یک کربن از انتهای کربوکسیل مولکول. این فرآیند شامل واسطه های حاوی آن است که با تشکیل پیوندهای فسفات غنی از انرژی همراه نیست.
اکسیداسیون اسیدهای چرب در حالت عادی بسیار کم است. این نوع اکسیداسیون توسط هیدروکسیلازها با مشارکت سیتوکروم c کاتالیز می شود. 123) ، در آندوپلاسمی ادامه می یابد -گروپ به یک گروه تبدیل می شود ، سپس به -COOH اکسید می شود. نتیجه یک اسید دیکاربوکسیلیک است. دومی توسط اکسیداسیون P تجزیه می شود ، معمولاً به اسیدهای آدیپیک و زیرآبی تبدیل می شود ، و سپس از طریق ادرار خارج می شوند.
نکات بالینی
کتوز با سرعت بالایی از اکسیداسیون اسیدهای چرب در کبد ایجاد می شود ، به ویژه هنگامی که در مقابل کمبود کربوهیدرات رخ دهد (به صفحه 292 مراجعه کنید). هنگام خوردن غذای غنی از چربی ، گرسنگی ، دیابت شیرین ، کتوز در گاوهای شیرده و سم زدایی بارداری (کتوز) در گوسفندان ، شرایط مشابهی ایجاد می شود. موارد زیر دلایل اختلال در اکسیداسیون اسیدهای چرب است.
کمبود کارنیتین در نوزادان تازه متولد شده ، اغلب نوزادان نارس رخ می دهد. یا ناشی از نقض بیوسنتز کارنیتین است. یا "نشت" آن در کلیه ها. از دست دادن کارنیتین می تواند در طی همودیالیز رخ دهد. بیمارانی که از اسیدوریای آلی رنج می برند مقدار زیادی کارنیتین را از دست می دهند که به صورت مخلوط با اسیدهای آلی از بدن دفع می شود. برای جبران مجدد از دست دادن این ترکیب ، برخی از بیماران به رژیم غذایی ویژه ای شامل غذاهای حاوی کارنیتین نیاز دارند. علائم و نشانه های کمبود کارنیتین حملات هیپوگلیسمی ناشی از کاهش گلوکونئوژنز در نتیجه نقض فرآیند است - اکسیداسیون اسیدهای چرب ، کاهش تشکیل بدن کتون ، همراه با افزایش محتوای FFA در پلاسمای خون ، ضعف عضلانی (میاستنی گراویس) و همچنین تجمع چربی ها. هنگام درمان داخل ، دارو کارنیتین را مصرف کنید. علائم کمبود کارنیتین بسیار شبیه به سندرم ری است ، اما در آن محتوای کارنیتین طبیعی است. علت سندرم ری هنوز مشخص نیست.
کاهش فعالیت carnitine palmitoyltransferase کبد منجر به افت قند خون و کاهش محتوای اجسام کتون در پلاسمای خون می شود و کاهش فعالیت عضله carnitine palmitoyltransferase منجر به نقض اکسیداسیون اسیدهای چرب می شود ، در نتیجه ضعف عضلات به طور دوره ای ایجاد می شود و میوگلوبینوری ایجاد می شود.
بیماری استفراغ جامائیکا پس از خوردن میوه های نارس آکی (Blig-hia sapida) در انسان اتفاق می افتد که حاوی یک سم هیپوگلیسین است که باعث از بین رفتن acyl-CoA دهیدروژناز می شود ، در نتیجه فرآیند اکسیداسیون β مهار می شود.
فرآیند اکسیداسیون اسیدهای چرب از مراحل اصلی زیر تشکیل شده است.
فعال سازی اسیدهای چرب. اسید چرب آزاد ، صرف نظر از طول زنجیره هیدروکربن ، از نظر متابولیکی بی اثر است و تا زمانی که فعال نشود ، نمی تواند تحت هیچ تغییر شیمیایی ، از جمله اکسیداسیون قرار گیرد. فعال سازی اسیدهای چرب با حضور یون های ATP ، کوآنزیم A (HS-KoA) و Mg 2+ در سطح خارجی غشای میتوکندری رخ می دهد. واکنش توسط آنزیم آسیل-کوآ سنتتاز کاتالیز می شود:
در نتیجه واکنش ، آسیل-CoA ایجاد می شود که فرم فعال اسید چرب است.
مرحله اول کمبود آب بدن. آسیل-CoA در میتوکندری در درجه اول دچار کم آبی آنزیمی می شود ، در حالی که آسیل-کوآ 2 اتم هیدروژن را در موقعیت های α- و β از دست می دهد ، و به یک استر CoA یک اسید اشباع نشده تبدیل می شود.

مرحله هیدراتاسیون. آسیل-CoA غیر اشباع (enoyl-CoA) ، با مشارکت آنزیم enoyl-CoA hydratase ، یک مولکول آب را متصل می کند. نتیجه β-hydroxyacyl-CoA (یا 3-hydroxyacyl-CoA) است:

مرحله دوم کمبود آب بدن. β-هیدروکسی آسیل-CoA تشکیل شده (3-هیدروکسی آسیل-CoA) سپس کم آب می شود. این واکنش توسط دهیدروژنازهای وابسته به NAD + کاتالیز می شود:

واکنش تیولاز. رخ 3-اکسوآسیل-CoA با گروه تیول از مولکول CoA دوم است. در نتیجه ، آسیل CoA کوتاه شده توسط دو اتم کربن و یک قطعه دو کربنی به شکل استیل CoA تشکیل می شود. این واکنش توسط استیل-CoA آسیل ترانسفراز (β-ketothiolase) کاتالیز می شود:

استیل-CoA تشکیل شده تحت اکسیداسیون در چرخه اسید تریکاربوکسیلیک قرار می گیرد ، و آسیل-CoA که توسط دو اتم کربن کوتاه می شود ، دوباره چندین بار از کل مسیر اکسیداسیون β عبور می کند تا زمان تشکیل بوتیریل-CoA (ترکیب 4 کربنی) ، که به نوبه خود اکسید می شود حداکثر 2 مولکول استیل-CoA.
تعادل انرژی. هر چرخه اکسیداسیون β یک مولکول FADH 2 و یک مولکول NADH تولید می کند. مورد دوم ، در فرآیند اکسیداسیون در زنجیره تنفسی و فسفوریلاسیون همراه ، می دهد: FADH 2 - 2 مولکول ATP و NADH - 3 مولکول ATP ، یعنی در کل ، 5 مولکول ATP در یک چرخه تشکیل می شود. هنگامی که اسید پالمیتیک اکسید می شود ، 5 x 7 \u003d 35 مولکول ATP تشکیل می شود. در فرآیند اکسیداسیون β اسید پالمیتیک ، 8 مولکول استیل-CoA تشکیل می شود که هر یک از آنها ، "در حال سوزاندن" در چرخه اسید تریکاربوکسیلیک ، 12 مولکول ATP می دهد و 8 مولکول استیل-CoA ، 12 x 8 \u003d 96 مولکول ATP می دهد.
بنابراین ، مجموعاً 351 + \u003d 131 مولکول ATP با اکسیداسیون کامل β اسید پالمیتیک تشکیل می شود. با در نظر گرفتن یک مولکول ATP که در ابتدای کار برای تشکیل فرم فعال اسید پالمیتیک (palmitoyl-CoA) هزینه شده است ، کل بازده انرژی با اکسیداسیون کامل یک مولکول اسید پالمیتیک در شرایط بدن یک حیوان 131 - 1 \u003d 130 مولکول ATP خواهد بود.