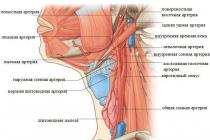
برای تهیه یک الکترولیت، باید تجهیزات زیر را داشته باشید:
مخزن، مقاوم در برابر عمل اسید سولفوریک، با ظرفیت 4-5 لیتر؛
aareometer با یک لوله حصار؛
دماسنج با محدوده از 0 تا 50 درجه سانتیگراد؛
گلابی های لاستیکی (بزرگ و کوچک) با راهنمایی مقاوم در برابر اسید؛
menzurka در هر 1 لیتر و 0.1 - 0.2 لیتر با تقسیمات کوچک؛
شیشه یا Ebonite Wand برای Solven Stirring؛
قیف شیشه ای
اجزای الکترولیت دارای باتری سولفوریک (GOST 667-73) و آب مقطر هستند، مخصوصا برای باتری ها.
تراکم الکترولیت ساخته شده باید مربوط به منطقه آب و هوایی باشد.
در طول آماده سازی الکترولیت، لازم است به شدت اقدامات ایمنی را در هنگام تعمیر و نگهداری باتری انجام دهیم. اسید سولفوریک معمولا در بطری های شیشه ای با شیشه های شیشه ای نگهداری می شود. لازم است که تنها با کمک وسایل، اسید را بچرخانید، اجازه ندهید آن را نفی کنید. یک راه حل 10٪ از نوشیدن نوشابه باید در کنار حالت خنثی کردن اسید ریخته شده اضافه شود.
در ابتدا توصیه می شود یک الکترولیتی را با تراکم 1.4 گرم در سانتی متر آماده کنید. اسید به آب مقطر با یک جت نازک ریخته می شود با یک جرثقیل مستمر یک راه حل با یک لیوان یا یک زاینده Ebonite. پس از اتمام الکترولیت با تراکم 1.4 g / cm3 تهیه می شود، باید به دمای + 25 درجه سانتیگراد خنک شود، دوباره تراکم الکترولیت را بررسی کنید و تنها پس از آن به الکترولیت تراکم مورد نیاز بروید. مقدار اسید سولفوریک و آب مقطر، که خواستار آماده سازی یک الکترولیت با تراکم 1.40 g / cm3 بود، پس از آن پالایش تا 1.26 g / cm3 یا تراکم دیگر، بر اساس جدول منطقه آب و هوایی تعیین می شود.
شارژ باتری مورد نیاز است: شارژر با یک آمپر و ولت متر.
خروجی مثبت باتری را به ترمینال "+" شارژر و منفی به ترمینال "-" اضافه کنید.
باتری را به اتهام 1/10 از ظرفیت اسمی در دمای الکترولیت که بالاتر از 30 درجه سانتیگراد نیست، در شرایط آب و هوایی سرد و معتدل و نه بالاتر از 35 درجه سانتیگراد در هوای گرم و گرم، شارژ باتری انجام نمی شود تا زمانی که تقسیم گاز را در تمام باتری ها تقسیم کنید (باتری "جوش") و به مدت 2 ساعت، ولتاژ و تراکم الکترولیت ثابت باقی می ماند.
در طول شارژ، به صورت دوره ای هر 2 ساعت نیاز به بررسی ولتاژ، تراکم و درجه حرارت الکترولیت را بررسی کنید و اطمینان حاصل کنید که درجه حرارت بیش از 45 درجه سانتیگراد (در منطقه کوره و سطح گرما تا 50 درجه سانتیگراد) افزایش نمی یابد. در این مورد، شما باید دو بار جریان شارژ را برای مدت زمان مورد نیاز برای کاهش دمای 30-35 درجه سانتیگراد کاهش دهید یا به طور موقت شارژر را برای خنک کردن الکترولیت تا 30 درجه سانتیگراد غیرفعال کنید.
میزان شارژ باتری توسط اندازه گیری تراکم الکترولیت تعیین می شود. تراکم الکترولیت توسط محدوده اندازه گیری می شود. هنگامی که تراکم به شهادت منطقه اندازه گیری می شود، اصلاح یا انتقال دما، که 0.01 g / cm3 در دمای 15 درجه سانتیگراد است، برای روشن کردن وضعیت واقعی الکترولیت نسبت به اعمال مناطق اقلیمی، اندازه گیری شود.
در پایان شارژ مجدد، اگر تراکم الکترولیت، با توجه به اصلاح دما، از هنجار این منطقه آب و هوایی متفاوت باشد، تراکم الکترولیت توسط طرح آب مقطر در چگالی بالای هنجار و اسید تنظیم می شود طرح با تراکم 1.4 g / cm3، زمانی که زیر آن است. پس از تنظیم، شارژ باید 30 دقیقه طول بکشد تا مخلوط کامل الکترولیت کامل شود.
در نهایت، سطح الکترولیت سطح 30 دقیقه پس از پایان شارژ انجام می شود. اگر سطح زیر هنجار باشد، الکترولیت همان تراکم به باتری اضافه می شود که باید با یک باتری کاملا شارژ اضافه شود، با بیش از حد اضافی توسط گلابی لاستیکی انتخاب شده است.
چرا باتری را برای مدت طولانی شارژ نمی کنید؟ با افزایش طول عمر باتری، الکترولیز الکترولیت به اکسیژن و هیدروژن متصل می شود. اکسیژن به شدت شبکه ای از صفحات مثبت را اکسید می کند و باعث تخریب آنها می شود. در همان زمان، زمانی که شارژ در منافذ توده های فعال، صفحات مقدار زیادی از گازهای اکسیژن و هیدروژن را جمع می کند که فشار را در منافذ افزایش می دهد، باعث شکستن و نقاشی توده فعال می شود. تخریب صفحات باعث کاهش ظرفیت باتری و اتصال کوتاه صفحات Variepete می شود. علامت مشخص Recharge یک گاز قوی (جوش) از الکترولیت و کاهش سریع در سطح آن است.
باتری های قلیایی در زمان ما استفاده گسترده ای دارند، هر دو در تولید و در زندگی روزمره. البته مصرف کنندگان اصلی، شرکت های مربوط به بهره برداری از سهام نورد هستند راه آهنهمچنین، آنها در لودرهای الکتریکی و لوکوموتیو های الکتریکی معدنی نصب شده اند. در شرکت های معدن، هیچ معدنچی بدون یک فانوس استخراج باتری کار می کند. به طور معمول، در چنین باتری های اجرایی استفاده می شود. چنین انتخابی به طور عمده به این واقعیت است که باتری های قلیایی بر روی دوام، قابلیت اطمینان و بسیاری از پارامترهای دیگر بیش از باتری های اسیدی رایج است. دوره گارانتی استفاده از عناصر قلیایی 5-7 سال است و با بهره برداری صحیح آنها می تواند بیش از ده سال برسد. برای این اهداف، باتری های قابل شارژ باید از زمان به زمان انجام شود نگهداری. اصل این اصل شامل بررسی تراکم الکترولیت در هر عنصر قدرت، در کنترل حضور مدارهای کوتاه درون عناصر، و همچنین اندازه گیری ولتاژ در پایانه های باتری در حضور یک بار است. به عنوان بخشی از این مقاله، ما ویژگی های استفاده شده توسط الکترولیت های قلیایی را در نظر می گیریم، و همچنین ما تکنولوژی خود آماده سازی الکترولیت باتری را توصیف می کنیم.
ویژگی های استفاده از الکترولیت های قلیایی.
الکترولیت قلیایی برای ریختن باتری های قلیایی با ترکیب نیکل کادمیوم یا ترکیب آهن نیکل ضروری است. برای چنین انواع باتری های قلیایی، دو نوع الکترولیت استفاده می شود: سدیم و پتاسیم. میانگین تراکم الکترولیت های قلیایی مورد استفاده در کشور ما در حدود 1.19-1.21g / cm3 است. ترکیب الکترولیت تا حدودی متفاوت از یکدیگر است. بنابراین برای آماده سازی استفاده از الکترولیت سدیم (سودا سودا) و آب مقطر. و برای تولید الکترولیت پتاسیم، به جز قلیایی (پتاسیم سوزاننده) و آب مقطر، 1٪ راه حل هیدروکسید لیتیوم 1٪ اضافه شده است، که به طور قابل توجهی ویژگی های الکترولیت را افزایش می دهد. مواد منبع برای تولید الکترولیت قلیایی عبارتند از:- آب مقطر (GOST 6709-72). در موارد شدید، استفاده از آب تامین آب.
- (GOST 9285-69)، HF (شیمیایی خالص)؛
- هیدروکسید لیتیوم، فنی لی (IT) 3 (GOST 8595-75).
- هنگام استفاده از باتری با دمای اطراف از -19 تا +35، لازم است یک الکترولیت پتاسیم پتاسیم کامپوزیتی داشته باشید، با افزودن 20 گرم. در لیتر لیتیوم سوزاننده. تراکم چنین الکترولیت باید در عرض 1.19-1.21g / cm3 باشد.
- برای باتری ها، بهره برداری از آن در شرایط سردتر، در دمای محیط از -40 تا -20 درجه سانتیگراد فرض می شود، لازم است از یک راه حل پتاسیم سوزان به عنوان الکترولیت استفاده شود، تراکم 1.26 - 1.2821 / cm3.
- برای استفاده از باتری های باتری در دماهای بالا، لازم است از یک الکترولیت متشکل از یک راه حل ناتورا سوزاننده با افزودن 20G استفاده شود. در لیتر لیتیوم سوزان، در حالی که تراکم محصول به پایان رسید باید در 1.17 - 1.19 گرم در سانتی متر باشد.
 گالوانیزه، کنسرو شده، مس، آلومینیوم، سرب، شیشه های معمولی و ظروف سرامیکی.
گالوانیزه، کنسرو شده، مس، آلومینیوم، سرب، شیشه های معمولی و ظروف سرامیکی.
منظور از پخت و پز الکترولیت قلیایی.
توجه! قبل از ادامه تولید مستقل الکترولیت قلیایی - فکر! آیا به آن نیاز دارید؟! ساده تر کردن - خرید در فروشگاه ما آماده برای باتری ها و فقط آب به آن اضافه کنید. ما آن را از طریق ایمیل ارسال خواهیم کرد، و شما به سرعت تصمیم می گیرید.
تکنولوژی آماده سازی الکترولیت باتری به شدت مطابق با توالی های تکنولوژیکی زیر است:- مقدار مورد نیاز آب را به ظروف (مقاوم در برابر حرارت) بریزید.
- با کمک انبساط فولاد یا تیغه، قطعات قلیایی را به آب در بخش های کوچک کاهش دهید؛
- برای سرعت بخشیدن به عبور از انحلال قلیایی در آب، راه حل باید توسط پلاستیک، انتشار، فولاد یا همزن شیشه ای مخلوط شود؛
- تراکم الکترولیت را با اضافه کردن مقدار مورد نیاز آب یا قلیایی تنظیم کنید.
- جداسازی ظروف با الکترولیت از دسترسی هوا و آن را به خنک کردن و ایستادن برای 3-6 ساعت تا روشن شدن کامل؛
- بخشی از الکترولیت را به دقت ادغام کنید. راه حل های قلیایی به دست آمده برای ریختن باتری های شفاف، مایعات کمی زرد، بی بو است. در پایین راه حل، مجاز به مقدار کمی از رسوب تاریکی است.
- باتری و باتری نیکل کادمیوم KCSLراهنمای فنی و دستورالعمل فنی)
- دستورالعمل برای آماده سازی الکترولیت قلیایی (گزیده ای از توضیحات فنی) - 1 لیم، 2 لیم.
- دست زدن به کتابچه راهنمای کاربر منحصر به فرد (شارژ باتری 3 VSKP-10M.05، کار خاص)
______________________________________________________________________________________________________________
تراکم الکترولیت قلیایی.
عمر مفید باتری های قلیایی بستگی به ترکیب الکترولیت و تراکم آن دارد. بسته به شرایط دما باتری (استفاده) باتری ها، توصیه می شود با آن کار کنید الکترولیت های مختلف. ترکیب مطلوب الکترولیت:
الکترولیت های مختلف. ترکیب مطلوب الکترولیت:
- دما: -15 ... + 35 ° C (افزایش کوتاه مدت دما الکترولیت تا 45 درجه سانتیگراد)ترکیب: KON + LIOH تراکم: 1،19 -1.21 G / CM3 +20 G / L (LIOH)
- دما: -25 ... -15 درجه سانتی گراد ترکیب: تراکم Con: 1.25 گرم / سانتی متر
- دما: -40 ... -25 درجه سانتی گراد ترکیب: Con Tagy: 1.27 G / CM3
- دما: ≥ + 40 ... + 60 درجه سانتیگراد ترکیبات: Naon + Liohتراکم: 1.17 -1.19 g / cm3 + از 10 تا 15 گرم در لیتر (LIOH)شارژ باید با جریان 0.25 ثانیه در عرض 8 ساعت انجام شود.
- دما: + 10 ... + 60 درجه سانتی گراد ترکیب: Naone تراکم: 1.17 -1.19 g / cm3
- دما: -15 ... + 15 ° C ترکیبات: تراکم Con: 1.19 -1.21 G / CM3
- دما: + 10 ... + 30 درجه سانتی گراد ترکیب: تراکم Naone: 1.17 -1.19 G / CM3
 تعریف تراکم الکترولیت، که با اندازه گیری گرانش خاص آن به دست می آید.بیشتر غلظت ماده اصلی (اسید یا قلیایی)، چگال تر الکترولیت می شود.تراکم بالاتر، سطح شارژ بالاتر است. هنگام اندازه گیری تراکم الکترولیت، باید قوانین زیر را دنبال کنید:
تعریف تراکم الکترولیت، که با اندازه گیری گرانش خاص آن به دست می آید.بیشتر غلظت ماده اصلی (اسید یا قلیایی)، چگال تر الکترولیت می شود.تراکم بالاتر، سطح شارژ بالاتر است. هنگام اندازه گیری تراکم الکترولیت، باید قوانین زیر را دنبال کنید:
- هنگام بررسی وضعیت شارژ، لازم است اندازه گیری ها را در چندین سلول باتری انجام دهیم؛
- انتظار نداشته باشید خواندن دقیق از خواندن بخار (A) بلافاصله پس از خلیج الکترولیت در باتری (ب)، نقاشی را ببینید؛
- دمای باتری بر دقت خواندن تاثیر می گذارد. الکترولیت باید در دمای اتاق معمولی باشد؛
- هنگام کار با مواد سوزاننده، قوانین ایمنی را مشاهده کنید؛
- الکترولیت، که در ریمومتر باقی می ماند، یک ماده خورنده است. فراموش نکنید پس از استفاده آن را بشویید.
- هنگام حرکت از حالت تابستان به زمستان و بالعکس؛
- در صورت سوء عملکرد؛
- برای حذف انباشت ناخالصی های مضر (کربنات) باتری های بدتر شده.
- غلظت LIOH: 5 گرم در لیتر، افزایش ظرفیت: 10٪
- غلظت LIOH: 20 G / L، افزایش ظرفیت: 18٪
- LIOH: غلظت 50 گرم / L، افزایش ظرفیت: 22٪.
شما می توانید الکترولیت قلیایی را خریداری کنید
شما همچنین می توانید در فروشگاه ما. ______________________________________________________________ اگر مقاله را دوست دارید، اطلاعاتی که در آن تعیین شده بود برای شما مفید بود، بر روی مدالها زیر کلیک کنید تا آن را با دوستان خود در شبکه های اجتماعی به اشتراک بگذارید.
به طور دقیق در مورد کدام اسید با باتری ماشین شما پر شده است و برای آنچه که نیاز دارد
بسیاری از رانندگان از خود سوال می کنند که کدام اسید در یک باتری ماشین سیل می شود. مفروضات نادرست مختلف توسط جهل بیان می شود. کسی می گوید اسید هیدروکلریک وجود دارد. برخی معتقدند که آب وجود دارد. وقت آن است که این سوال را روشن کنیم. در یک ماشین باتری سرب اسید سیل اسید سولفوریک سیل. اگر شما کاملا دقیق بیان شده اید، راه حل اسید سولفوریک در آب مقطر پوشیده شده است. این راه حل به نام الکترولیت نامگذاری شد.
به طور کلی، می توان آن را به عنوان یک الکترولیت در برخی از انواع باتری های خودرو استفاده کرد. به عنوان مثال، نیکل کادمیوم یا نوع نیکل آهن نوع. گروه دیگری AGM و ژل وجود دارد، جایی که الکترولیت در حالت مرتبط است. اما این همان راه حل اسید سولفوریک است. این به سادگی با کمک افزودنی ها (ژل) به حالت ژل مانند ترجمه شده است یا با فایبرگلاس (AGM) آغشته می شود. باتری های ماشین Twist-acid با الکترولیت مایع امروز شایع ترین هستند. بنابراین، دقیقا در مورد یک محلول آبی اسید سولفوریک در نظر گرفته شده برای پر کردن باتری است.


اسید سولفوریک در بخش های مختلف اقتصاد ملی استفاده می شود. به عنوان مثال، قبل از استفاده از پوشش، توسط سطح فلز تمیز می شود، آن را در آماده سازی رنگ های مختلف مصنوعی استفاده می شود. علاوه بر این، اسید سولفوریک در زمینه تولید کود، مواد منفجره، صنایع دارویی، پردازش نفت تقاضا می شود.
اسید سولفوریک به طور گسترده ای در تولید باتری های سرب اسید برای اتومبیل استفاده شده است. غلظت اسید در الکترولیت 30-35 درصد (وزن) است. بقیه آب مقطر. از آب های معمولی آب استفاده نمی شود، زیرا حاوی نمک های فلزات مختلف است. ضربه آنها در باتری خودرو به طور قابل توجهی عمر مفید آن را کاهش می دهد.
در حوزه خانوار غلظت H 2 SO 4، 30 درصد کافی است، اما اسید سولفوریک غلظت بالاتر اغلب در تولید استفاده می شود. اسید سولفوریک متمرکز در دو مرحله به دست می آید. در مرحله اول، غلظت به 70 درصد افزایش می یابد و سپس به 98 درصد افزایش می یابد. اسید سولفوریک چنین غلظت مناسب برای ذخیره سازی بعدی است. ممکن است غلظت 99 درصد را بدست آورید، اما در آینده به دلیل از دست دادن SO 3 به 98.3 درصد کاهش می یابد.
ارقام اسید سولفوریک اصلی وجود دارد که در زیر ذکر شده اند:
- برج یا نیتروز. غلظت 75 درصد. تراکم این نوع 1.67 گرم / سانتی متر است. نام این نوع به دلیل روش تولید در برج های دوم به روش نیتروژن به دست آمد. گاز سرخ کردن با دی اکسید گوگرد (SO 2) توسط نیتروز (H 2 SO 4 با مواد افزودنی اکسید نیتروژن) پردازش می شود. در طول واکنش شیمیایی، اکسید نیتروژن و اسید به دست می آید. در این مورد، اکسید ها به طور مداوم در چرخه تولید پخش می شوند؛
- مخاطب. غلظت 92.5 تا 98 درصد. تراکم تنوع 1.837 GY / cm 3 است. این گونه ها نیز از گاز شلیک ساخته شده است که حاوی 2 دی اکسید است. در طول واکنش، اکسیداسیون به SO 3، هنگام تماس با کاتالیزور جامد از وانادیوم؛
- OLEUM مرتب کردن غلظت 104.5 درصد. تراکم 1.897 گرم / سانتی متر است. تنوع یک راه حل SO 3 در اسید سولفوریک (H 2 SO 4) است. بنابراین نسبت 3 تا 20 درصد، H 2 SO 4 - 104.5 درصد؛
- منافع بالا غلظت 114.6 درصد و تراکم 2.002 GY / cm 3؛
- قابل شارژ غلظت 92 تا 94 درصد و تراکم 1.835 گرم در سانتی متر 3.
فرآیندهای موجود در باتری شامل الکترولیت است
بهره برداری از باتری باتری اسید سرب بر اساس فرایندهای الکتروشیمیایی است که با مشارکت الکترولیت ادامه می یابد. باتری خودرو شامل صفحات مثبت و منفی غوطه ور شده است راه حل آب اسید سولفوریک. صفحات مثبت و منفی دارای کوره های سرب فعلی با افزودنی های مختلف بسته به نوع باتری هستند.
دی اکسید سرب سرخ مایل به قرمز (PBO 2) بر روی شبکه های الکترودهای مثبت (PBO 2) اعمال می شود. بر روی الکترودهای منفی - پودر سرب سولکی (PB). ویژگی های الکتریکی باتری به طور مستقیم به تراکم الکترولیت بستگی دارد. برای درک هدف الکترولیت، لازم است که فرآیندهای اصلی موجود در باتری خودرو را در نظر بگیریم.
هنگامی که تخلیه، باتری بر روی یک الکترود مثبت (آند) واکنش زیر است:
PBO 2 + SO 4 2- + 4H + + 2E - -\u003e PBSO 4 + 2H 2 O
بر روی الکترود منفی (کاتد) این فرآیند را جریان می دهد:
PB + SO 4 2- - 2E - -\u003e PBSO 4
هنگام شارژ باتری، این واکنش ها در جهت مخالف ادامه می یابد.
الکترولیت در باتری باتری سرب اسید، بسته به درجه اتهامات باتری، تراکم متفاوت دارد. همانطور که در بالا ذکر شد، اسید متمرکز از تنوع باتری دارای تراکم 1.835 گرم در سانتی متر است. تراکم الکترولیت بر روی باتری شارژ در محدوده 1.127 تا 1300 گرم در سانتی متر قرار دارد. هنگامی که باتری خودرو به عنوان یک نتیجه از واکنش الکتروشیمیایی از الکترولیت تخلیه می شود، اسید سولفوریک مصرف می شود و قطره آن کاهش می یابد. در حالی که جریان تخلیه اسید از طریق باتری در کنار مواد مصرفی الکترود به عنوان یک نتیجه از واکنش های فوق، عبور می کند. انتشار H 2 SO 4 از حجم به الکترودها وجود دارد. بنابراین، ولتاژ بر روی خروجی های باتری حفظ می شود.
در ابتدای تخلیه، فرآیند انتشار اسید به الکترودها. این به این واقعیت توضیح داده شده است که در توده فعال الکترودهای منافذ، سولفات هنوز مسدود نشده است. همانطور که لایه سولفات بر روی آنها شکل می گیرد و منافذ را مسدود می کند، فرآیند انتشار کاهش می یابد. در تئوری، روند تخلیه می تواند تا زمانی که الکترولیت به آب تبدیل شود. اما در عمل، تخلیه رخ می دهد تا زمانی که تراکم به مقدار 1.15 گرم در سانتی متر برسد. در زمان کاهش تراکم به 1.15 GY / cm 3، سولفات سرب بسیار متمایز است، که به اندازه کافی برای صعود توده فعال صفحات به اندازه کافی است. با تراکم الکترولیت، می توان در مورد میزان شارژ باتری قضاوت کرد. برای انجام این کار، می توانید از جدول زیر نشان داده شده استفاده کنید.
| درجه حساب،٪ | ||||
|---|---|---|---|---|
| تراکم الکترولیت، g / cm. مکعب (+15 گرم Celsius) | ولتاژ، در (در صورت عدم بار) | ولتاژ، در (با بار 100 A) | درجه حساب،٪ | دمای یخ زده الکترولیت، GR. سلسله |
| 1,11 | 11,7 | 8,4 | 0 | -7 |
| 1,12 | 11,76 | 8,54 | 6 | -8 |
| 1,13 | 11,82 | 8,68 | 12,56 | -9 |
| 1,14 | 11,88 | 8,84 | 19 | -11 |
| 1,15 | 11,94 | 9 | 25 | -13 |
| 1,16 | 12 | 9,14 | 31 | -14 |
| 1,17 | 12,06 | 9,3 | 37,5 | -16 |
| 1,18 | 12,12 | 9,46 | 44 | -18 |
| 1,19 | 12,18 | 9,6 | 50 | -24 |
| 1,2 | 12,24 | 9,74 | 56 | -27 |
| 1,21 | 12,3 | 9,9 | 62,5 | -32 |
| 1,22 | 12,36 | 10,06 | 69 | -37 |
| 1,23 | 12,42 | 10,2 | 75 | -42 |
| 1,24 | 12,48 | 10,34 | 81 | -46 |
| 1,25 | 12,54 | 10,5 | 87,5 | -50 |
| 1,26 | 12,6 | 10,66 | 94 | -55 |
| 1,27 | 12,66 | 10,8 | 100 | -60 |
یک عنصر کاملا شارژ شده از باتری ماشین، ولتاژ 2.5 تا 2.7 ولت را بدون بار بر روی خروجی ها تولید می کند. هنگامی که بار متصل می شود، ولتاژ چند دقیقه به 2.1 ولت ارسال می شود. در طول این مدت، آن زمان برای تشکیل یک لایه PBSO4 بر روی سطح الکترودهای منفی است. به عبارت دیگر، ولتاژ یک عنصر در AKB متصل به ماشین تقریبا 2.15 ولت است.
اگر باتری خودروی را با یک جریان کوچک (10 درصد از کانتینر امتیاز) تخلیه کنید، سپس یک ولتاژ عنصر پس از یک ساعت تخلیه به 2 ولت کاهش می یابد. این به خاطر این واقعیت است که در این لحظه مقدار زیادی از PBSO 4 به سرعت شکل گرفته است، که منافذ توده های فعال را مسدود می کند. در نتیجه، مقاومت داخلی عناصر باتری در حال رشد است و غلظت الکترولیت قطره می شود. پس از مدتی، روند تخلیه به جلو می رود (نگاه کنید به برنامه).

این مستقیم مربوط به تعادل تراکم الکترولیت در نزدیکی الکترود ها و در بقیه حجم است. به تدریج، اسید از حجم به الکترود می آید و با انتشار سولفات سرب واکنش نشان می دهد. تراکم الکترولیت به تدریج کاهش می یابد و ولتاژ کاهش می یابد از مرحله اولیه. و در مرحله پایان، زمانی که جرم فعال توسط سولفات سرب حاصل شده مسدود می شود، واکنش کاهش می یابد و ولتاژ به سرعت کاهش می یابد.
خواندن زمان:الکترولیت یکی از اجزای اصلی باتری است که راه اندازی خودرو را فعال می کند. این اتفاق می افتد چند گونه است که در ترکیب آن متفاوت است. کنترل به موقع بر میزان و کیفیت الکترولیت در باتری از خروجی باتری زودرس جلوگیری می کند و در خرید یک دستگاه جدید ذخیره می شود.
در حال حاضر سه نوع الکترولیت برای باتری ها وجود دارد، برای باتری های قلیایی - قلیایی، و اسید اسیدی، اما الکترولیت اصلاح، که لازم است زمانی که تعمیر باتری ها نیز متمایز است.
چگونه می توان باتری اسید یا قلیایی را تعیین کرد؟ ساده ترین راه برای انجام این کار، علامت گذاری بدنه و مواد حاصل از آن است. بدن ACB اسید همیشه از پلاستیک خاصی ساخته شده است، در حالی که باتری های قلیایی می توانند از فلز ساخته شوند. شما همچنین می توانید یک الکترولیت را از باتری آزمایش کنید: الکترولیت اسید به یک واکنش با سودا یا گچ وارد می شود.
اسید
این مخلوطی از اسید سولفوریک است که سی و پنج درصد کل ترکیب و آب مقطر است که شصت و پنج سال باقی مانده را اشغال می کند.  این ترکیب در باتری در مخازن با صفحات سرب است، در هنگام تماس با این عناصر و جریان کار می کند.
این ترکیب در باتری در مخازن با صفحات سرب است، در هنگام تماس با این عناصر و جریان کار می کند.
مزایای الکترولیت اسید:
- سطح بالایی از کارایی
- ضرر و زیان ضعیف در هنگام بی عملی
- شروع کنجکاو بالا
- کم هزینه
معایب:
- حساسیت به قطرات درجه حرارت
- عدم انطباق
- نیاز به کنترل چگالی کنترل منظم
لازم به ذکر است که الکترولیت اسید در اکثر مدل های باتری برای اتومبیل ها استفاده می شود، زیرا تنها قادر به ارائه مقدار کافی جریان برای شروع موتور است. در عین حال، باتری های ساخته شده با استفاده از این راه حل به دو گروه تقسیم می شوند:
- خدمتکار
- نه بنده
نمایش اول دسترسی آسان به محتویات قوطی ها را فراهم می کند. شما می توانید تراکم الکترولیت را اندازه گیری کنید، در صورت لزوم، آب مقطر و الکترولیت را به سادگی با کشیدن درب ها با قوطی ها اندازه گیری کنید. 
در مورد مدل های غیر قابل نگهداری نیز ممکن است اقدامات مشابهی را انجام دهد، اما لازم است که دستگاه را به طور مستقل باز کنیم تا اقدامات لازم را انجام دهیم و سپس آنها را محکم ببندیم. در چنین مواردی، دستگاه مته و جوشکاری می تواند مورد استفاده قرار گیرد.
برای جایگزینی الکترولیت در مدل های غیر خدمت تنها در مواردی است که دوره گارانتی آنها منقضی شده است. اغلب صرفا برای به دست آوردن تجربیات چنین عملیاتی ساخته شده است.
قلیایی
الکترولیت آلکالین شامل هیدروکسید پتاسیم، سدیم، لیتیوم یا تمام این اجزا در یک مجتمع پیچیده در آب است.
مزایای این گونه عبارتند از:

معایب:
- ارزش کمتر نیروی الکترومغناطیسی نسبت به اسید
- عدم شروع امکان عرضه فعلی برای شروع موتور
- هزینه بالاتر
با وجود عمر طولانی، بی تکلف و مزایای دیگر استفاده از این نوع الکترولیت در صنعت خودرو محدود است. ناتوانی در تولید سطح کافی از شروع جریان لازم برای شروع موتور. معایب نیز شامل ابعاد چشمگیر آنها می شود.
با این حال، دستگاه های الکترولیت قلیایی با موفقیت در ارائه کشش و جریان لوکوموتیو استفاده می شود.
مهم! قبل از جایگزینی، اطمینان حاصل کنید که باتری قلیایی است. در غیر این صورت، AKB می تواند به طور کامل مشخص شود.
اصلاحی
این الکترولیت یک ترکیب خاص با محتوای بالایی از مواد فعال است که برای افزایش تراکم الکترولیت باتری استفاده می شود. در نظر گرفته شده است تا غلظت مواد فعال در باتری را افزایش دهد. 
شما می توانید انواع زیر Electrolyte اصلاحی را پیدا کنید:
- لیتیوم پتاسیم جامد
- لیتیوم پتاسیم مایع با تراکم مختلف
- اسید مایع
الکترولیت اصلاح شده را می توان به طور مستقل انجام دادبا توجه به دست لازم برای این ترکیب، با این حال اغلب آن را خریداری می کند، زیرا ارزش آن بیش از دسترس است.
نحوه استفاده از الکترولیت اصلاحی:
- برخی از الکترولیت را از قوطی ها حذف کنید
- همان مقدار مایع اصلاح شده را در آنها اضافه کنید.
- باتری را بر روی شارژ جریان داده شده نصب کنید تا فرآیند مخلوط کردن آن را برای نیم ساعت شروع کنید
- برای چند ساعت باتری را ترک کنید
- اندازه گیری تراکم و تنظیم آن را دوباره در صورت لزوم تنظیم کنید
هنگامی که اصلاح مجدد، مقدار الکترولیت قابل تعویض باید کاهش یابد.
چگونه خود را طبخ کنید
قبل از اینکه شما به طور مستقل الکترولیت را برای باتری جایگزین کنید، باید اقدامات امنیتی مناسب را انجام دهید و اشیاء حفاظت فردی را آماده کنید:

- دستکش
- پیشبند
- عینک محافظ
- محلول سودا در مورد باسن بر روی پوست یا لباس های لباس
- سرکه یا اسید لومونیک - برای خنثی سازی قلیایی
اقدامات انجام شده را در یک اتاق تهویه مناسب با دمای هوا بالاتر از +25 درجه سانتیگراد انجام دهید. لازم است پیش از این بدانیم که مقدار الکترولیت به پایان رسید برای پر کردن باتری ها مورد نیاز است. میانگین، در باتری مدرن، مقدار راه حل از 2.6 تا 3.7 لیتر متغیر است.بنابراین، لازم است بلافاصله به حداکثر تعداد حرکت کند. به عنوان پایه، شما می توانید 4 لیتر ملات نهایی را مصرف کنید.
برای آماده سازی الکترولیت، باید موارد زیر را پیش از آن آماده کنید:
- ظروف ظرفیت کافی از مواد مقاوم در برابر مواد اسید و قلیایی ساخته شده است
- یک جادوگر کوچک برای مخلوط کردن الکترولیت
- ابزار اندازه گیری تراکم، دما و سطح ملات
- برای اسید الکترولیت اسید - مایع گوگرد، برای قلیایی - قلیایی در فرم جامد یا مایع، لیتیوم یا ژل سیلیکا
مهم! تمام مواد مورد استفاده باید از لحاظ شیمیایی خنثی باشند تا از وقوع واکنش های غیر ضروری در هنگام تماس آنها حذف شوند. به عنوان ظرفیت، شیشه های شیشه ای معمولی کاملا مناسب خواهد بود.
فرآیند پخت و پز الکترولیت قلیایی
مواد تشکیل دهنده آماده سازی این ترکیب می تواند هر دو در فرم مایع و در جامد باشد. اگر همه چیز با اولین بار روشن باشد، قبل از ریختن، الکترولیت قلیایی از جامد لازم است که در آب مقطر حل شود. 
تراکم مورد نیاز بر روی وب سایت تولید کننده باتری نشان داده شده است، شما همچنین می توانید اطلاعات را در راهنمای دستورالعمل متصل کنید. الکترولیت جامد نسبت به مقدار مورد نظر راه حل مایع نهایی گرفته شده است و عبارتند از:
- 1/5 - برای به دست آوردن یک راه حل با تراکم 1.17-1.19 g / m³
- 1/3 - برای یک راه حل با تراکم 1.19-1.21 g / m³
- 1/2 - برای یک راه حل با تراکم 1.25-1.27 g / m³
فرآیند پخت و پز شامل مراحل زیر است:
- آب آشامیدنی را در ظروف بریزید
- اضافه کردن مقدار مناسب قلیایی
- راه حل را هم بزنید
- درب را محکم ببند
- اصرار 6 ساعت
پس از اتمام فرآیند، لازم است یک راه حل نور را تخلیه کنیم. اگر بخشی از ترکیب به رسوب برسد، لازم است به طور منظم متناوب آن باشد. هنگامی که ریختن، شما باید دنبال کنید، به طوری که آن را در پایین باقی می ماند، بدون ضربه زدن به باتری، در غیر این صورت آن را تهدید به شکست Abbus.
آماده سازی راه حل برای باتری های سرب
قبل از رقیق کردن الکترولیت اسید، لازم است که مقادیر لازم را تعیین کنید. آنها به شرایط اقلیمی که در آن دستگاه برنامه ریزی شده بستگی دارد. 
برای به دست آوردن یک الکترولیت با تراکم 1.28 g / m³، که برای شرایط متوسط \u200b\u200bآب و هوایی قابل قبول است، لازم است که 0.36 لیتر اسید سولفوریک را به یک لیتر آب مقطر بریزید. برای مناطق گرم، مقدار اسید سولفوریک به میزان 0.33 لیتر در همان مقدار آب کاهش می یابد.
چگونه برای پرورش اسید قابل شارژ:
- آب مقطر را در ظرفیت آماده آماده کنید
- به طور منظم ریخته گری اسید پور به آن
- تراکم محلول حاصل را اندازه گیری کنید
- راه حل 12 ساعت را ترک کنید
مهم! شما نمی توانید آب را به اسید بریزید! مناسب - اسید را به آب بریزید. عجله نکنید، اسید ریختن، بگذارید بتوانیم به تدریج در آب حل شود.
دستورالعمل برای جایگزینی
جایگزینی الکترولیت در موارد زیر ساخته شده است:

جایگزینی الکترولیت، صرف نظر از اینکه آیا آن قلیایی یا اسیدی است، در چند مرحله تولید می شود:
- تخریب باتری از وسیله نقلیه
- تمیز کردن باتری از آلودگی
- بازگشت مایع موجود با گلابی یا یک سرنگ
- فلاشینگ با آب مقطر می تواند
- ریختن الکترولیت با دستگاه های گلابی یا مشابه
سطح پر شدن توسط برچسب ها در داخل قوطی ها تعیین می شود. اگر آنها از دست رفته باشند، باید از طریق قانون هدایت شود - الکترولیت باید در سطح صفحات 5-7 میلی متر باشد. در عین حال، حداقل دو سانتیمتر باید از سطح آن به پوشش کلاه باقی بماند. 
بسیار مهم است که الکترولیت آن را به سمت پایین بچرخانید و نه بیشتر به نوبه خود. در پایین عروق ممکن است ذرات جامد وجود داشته باشد که در صفحات گیر کرده اند، به طور کامل آنها را رد می کنند. اجازه می دهد تا در طول شستشو کمی آب را از طرف طرف به طرف حرکت دهید، همان اقدامات را می توان پس از اینکه الکترولیت باتری را پر می کند، انجام می شود.
پس از آن، باتری به شارژ می شود، پس از آن چگالی حاصل باید بررسی شود. اندازه گیری ها باید عرصه ای از چند ساعت پس از از بین بردن دستگاه با شارژ، از آنجا که خطر ابتلا به خواندن بیش از حد وجود دارد. اگر تراکم بالا نباشد یا برعکس، مقادیر غیر ضروری داشته باشد، باید با افزودن اسید، قلیایی یا آب مقطر تنظیم شود.
ویدئو مفید
دستورالعمل های ویدئویی برای جایگزینی الکترولیت
نتیجه
صرف نظر از نوع الکترولیت مورد استفاده در باتری عملیاتی، شما می توانید به طور مستقل آن را جایگزین کامل، چگالی چک و شاخص های دیگر. با این حال، لازم است به یاد داشته باشید تکنیک ایمنی، از آنجا که الکترولیت خطرناک است ترکیب شیمیاییقادر به آسیب رساندن به پوست و چشم است.
19 نوامبر 2019.باتری های قابل شارژ با مایع قلیایی یا اسید مبتنی بر اسید، طراحی شده برای کل زندگی محصول طراحی شده اند. هنگامی که تجزیه واکنش نشان می دهد (ابری یا انجماد)، شما می توانید سعی کنید جایگزین راه حل، که طول عمر محصول را گسترش می دهد. در عین حال شما باید بدانید که چگونه یک الکترولیت را برای باتری در خانه آماده کنید.
ترکیب الکترولیت برای ACB
ترکیب الکترولیت بستگی به نوع باتری دارد:
- در باتری های سرب برای اتومبیل ها و موتور سیکلت ها، یک راه حل از آب مقطر و اسید سولفوریک استفاده می شود (فرمول H2SO4).
- در لامپ ها و تاسیسات ثابت - منابع قلیایی جریان مستقیم، توسط محلول آبی 20٪ آبی یا پتاسیم (NaOH یا KOH) دوباره پر شده است. برای افزایش ویژگی های عملکرد، افزودنی ها به مخلوط معرفی می شوند (به عنوان مثال، بر اساس لیتیوم مونوهیدرات).
تراکم و اجزای مورد نیاز
برای جریان طبیعی واکنش های شیمیایی در باتری، لازم است از ترکیب الکترولیتی بدون ناخالصی های خارجی استفاده شود که می تواند ظرفیت باتری را کاهش دهد. برای بهبود کارایی منبع فعلی، لازم است از اجزای شیمیایی شیمیایی استفاده شود. با توجه به مقررات آماده سازی الکترولیت برای باتری های سرب، اسید حاوی بیش از 8٪ آب استفاده می شود. راه حل بر اساس آب مقطر مخلوط شده است، نه حاوی نمک، استفاده از مایع از لوله آب به شدت ممنوع است.
قلیایی تحت فرم خشک شده، در فرآیند ذخیره سازی و حمل و نقل عرضه می شود، مواد نباید پخته و در تعامل با سایر واکنش ها مشغول به کار شوند. گرانول ها به آب مقطر بارگیری می شوند و Stirled، سپس اجزای اضافی به محلول وارد می شوند.
کیفیت الکترولیت برای منابع جریان شیمیایی قابل استفاده مجدد به طور مستقیم وابسته به انطباق با نسبت اجزای اجزای مایع کار است.
امنیت در خانه پخت و پز
قبل از اینکه به طور مستقل الکترولیت را در خانه بسازید، لازم است خود را با قوانین ایمنی آشنا کنید:
- برای حفاظت از پوست، چشم و اندام های تنفسی، ابزار مقاوم در برابر مواد تهاجمی استفاده می شود. لازم است پوشیدن یک دستکش محافظ و دستکش های لاستیکی، عینک چشم.
- برای خنثی سازی اسید ریخته شده، الکل آمونیاک یا یک محلول آبی از نوشابه های نوشابه سودا استفاده می شود.
- اجزای مخلوط در یک ظرف شیشه ای یا پلاستیکی ساخته شده است، مقاوم در برابر مواد تهاجمی. در تولید الکترولیت قلیایی، کانتینر فولاد یا پلاستیک استفاده می شود، استفاده از مخازن از مواد دیگر مجاز نیست.
- اتاق باید تهویه شود زیرا جفت های اسید یا قلیایی منفی بر مسیرهای تنفسی فرد تاثیر می گذارد.
- در تولید الکترولیت برای باتری های سرب، اسید به آب با بخش های کوچک با مخلوط ثابت از راه حل ریخته می شود.

تجهیزات لازم
قبل از تهیه محلول اسید سولفوریک، لازم است آماده شود:
- ظرفیت 2-3 لیتر (نوع ماده بستگی به ترکیب الکترولیت دارد)؛
- ظرفیت ابعاد برای تعیین دوز لازم واکنشگرها؛
- آب مقطر؛
- اسید سولفوریک متمرکز؛
- شیشه ای برای مخلوط کردن؛
- یک سیستم برای اندازه گیری تراکم مخلوط مخلوط.
دستورالعمل برای پخت و پز
پس از تهیه مواد و تجهیزات حفاظتی، می توانید به اجزای مخلوط بروید. روش آماده سازی اسید سولفوریک یا الکترولیت قلیایی با پیچیدگی متمایز نیست. معرفهای دریافت شده توصیه نمی شود که در خانه ذخیره شود: مایع به بانک های باتری ریخته می شود که باید متهم شود. ذخیره سازی باتری در حالت تخلیه مجاز نیست، زیرا الکترودهای و تخریب توده فعال رخ می دهد.
ترکیب اسید
آثار در یک اتاق تهویه در دمای هوا بیش از 25 درجه سانتیگراد انجام می شود. قبل از مخلوط کردن اجزای سازنده، لازم است حجم مایع مورد نیاز برای سوخت گیری باتری را بیابید. باتری های خودرو با ظرفیت 50-60 A * H دارای محوطه هایی هستند که تا 3.7 لیتر الکترولیت قرار دارند. توصیه می شود یک مایع کار کمی بیشتر (توسط 200-300 میلی لیتر) ایجاد کنید. همچنین لازم است که تراکم الکترولیت را تعیین کنیم، بسته به منطقه آب و هوایی. دمای محیط پایین تر، چگالی شروع الکترولیت باید بالاتر باشد.
 به عنوان مثال، برای مناطق شمال شمال با حداقل دمای در زمستان تا -50 درجه سانتیگراد، توصیه می شود که مایع با تراکم 1.27 گرم در سانتی متر (پس از شارژ، پارامتر به 1.29 g / cm³ افزایش یابد) . در نوار میانی، یک محلول از تراکم 1.28 گرم در سانتی متر استفاده می شود. برای به دست آوردن یک الکترولیت، 1 لیتر از آب مقطر و 360 میلی لیتر اسید سولفوریک مصرف می شود.
به عنوان مثال، برای مناطق شمال شمال با حداقل دمای در زمستان تا -50 درجه سانتیگراد، توصیه می شود که مایع با تراکم 1.27 گرم در سانتی متر (پس از شارژ، پارامتر به 1.29 g / cm³ افزایش یابد) . در نوار میانی، یک محلول از تراکم 1.28 گرم در سانتی متر استفاده می شود. برای به دست آوردن یک الکترولیت، 1 لیتر از آب مقطر و 360 میلی لیتر اسید سولفوریک مصرف می شود.
برای به دست آوردن یک راه حل طراحی شده برای کار در مناطق جنوبی، 330 میلی لیتر اسید مورد نیاز است (تراکم محاسبه شده 1.24 گرم در سانتی متر است).
الگوریتم آماده سازی راه حل خلاصه:
- آب مقطر را به ظرف اضافه کنید.
- حجم لازم را از اسید سولفوریک با یک جت نازک پرتاب کنید، به طور همزمان راه حل را با یک شیشه ی شیشه ای تکان دهید. مخلوط کردن اجزای شتابنده ممنوع است.
- اندازه گیری تراکم تعیین شده، و سپس مقاومت در برابر مایع بیش از 10-12 ساعت برای مخلوط کامل از اجزای.
- تراکم سنج سنج را دوباره اندازه گیری کنید. اگر پارامتر از مقدار دلخواه به یک جهت کوچکتر متفاوت باشد، اسید اضافی به مخلوط معرفی می شود. با تراکم بالا، الکترولیت باید با آب مقطر رقیق شود.
- راه حل را به بانک های باتری بریزید که از مایع اگزوز از قبل تمیز شده است. پس از شارژ، کنترل تراکم مورد نیاز است، در حالی که مقدار با معرفی اسید سولفوریک اضافی یا طرح آب مقطر تنظیم می شود. باید به یاد داشته باشید که اندازه گیری تراکم تنها با یک باتری کاملا شارژ درست خواهد بود.
قلیایی مبتنی بر
هنگام تهیه یک راه حل قلیایی، لازم است که در نظر گرفته شود وضع تجمع قلیایی، که به شکل گرانول ها یا در یک حالت مایع (در مخلوط با آب) می آید. مواد جامد در آب می خوابند (تقطیر) و با مخلوط با یک چوب شیشه ای حل می شود. نسبت اجزای محلول بر روی برچسب کارخانه در کنار منبع تغذیه نشان داده شده است.
 تراکم راه حل بستگی به منطقه آب و هوایی دارد، دمای محیط پایین تر، تراکم بیشتر باید الکترولیت داشته باشد. به عنوان مثال، در درجه حرارت تا -19 درجه سانتیگراد، یک الکترولیت به 1.21 گرم / سانتی متر استفاده می شود تا ویژگی ها را بهبود بخشد، معرفی 20 گرم در هر لیتر لیتیوم سوزان، استفاده می شود.
تراکم راه حل بستگی به منطقه آب و هوایی دارد، دمای محیط پایین تر، تراکم بیشتر باید الکترولیت داشته باشد. به عنوان مثال، در درجه حرارت تا -19 درجه سانتیگراد، یک الکترولیت به 1.21 گرم / سانتی متر استفاده می شود تا ویژگی ها را بهبود بخشد، معرفی 20 گرم در هر لیتر لیتیوم سوزان، استفاده می شود.
ترکیب مشابهی از راه حل در باتری هایی که تحت دمای بالا قرار دارند استفاده می شود. هنگام استفاده از یک باتری در دمای -40 درجه سانتیگراد، چگالی باید به 1.28 گرم بر سانتی متر برسد.
مقادیر مشترک از قلیایی خشک و آب:
- برای تشکیل یک راه حل با تراکم 1.17 تا 1.19 g / cm³، لازم است 1/5 جزء خشک را در 4/5 آب معرفی کنید.
- هنگام ساخت 1/3 قلیایی در 2/3 آب، تراکم مخلوط به 1.19-1.21 g / cm³ افزایش می یابد؛
- برای به دست آوردن یک راه حل با حداقل دمای یخ زده، لازم است که قلیایی خشک و آب را در نسبت مساوی ترکیب کنید (چگالی به 1.27 گرم در سانتی متر).
واکنش حاصل باید در اتاق 6 ساعت باقی بماند، ظرفیت با یک درب هرمی بسته شده است. هنگام تماس با هوا، تخریب الکترولیتی رخ می دهد، خواص الکتروشیمیایی راه حل را بدتر می کند. بخشی از قلیایی به رسوب می رسد، یک کسر روشن برای پر کردن بانک های باتری (واقع در بالای مخزن) بدون ناخالصی استفاده می شود. ذرات جامد حفره های قوطی ها را وارد می کنند که باعث بسته شدن الکترودهای منفی و مثبت می شود، که منجر به تخلیه شتاب دهنده منبع DC می شود.
انواع دیگر الکترولیت ها
آماده سازی انواع دیگر الکترولیت ها در شرایط داخلی انجام نمی شود. اگر باتری از مخلوط ضخیم از اسید و آب (AGM فن آوری یا باتری های ژل) استفاده کند، به طور مستقل راه حل را با پارامترهای دلخواه آماده نخواهد کرد. برای بازگرداندن چنین دستگاهی، لازم است که آب را به بانک ها پر کنید، که به تدریج واشر اسفنجی را افزایش می دهد. سپس چندین دوره شارژ با جریانهای کوچک وجود دارد که به شما اجازه می دهد ظرف را بازگردانید.