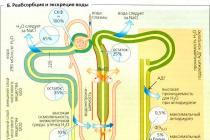
بازجذب لوله ای فرآیند جذب مجدد آب و مواد از ادرار موجود در مجرای لوله ها به لنف و خون است.
بخش عمده ای از مولکول ها در نفرون پروگزیمال بازجذب می شوند. در اینجا اسیدهای آمینه، گلوکز، ویتامینها، پروتئینها، عناصر ریز، مقدار قابل توجهی Na+، C1-، HCO3- و بسیاری از مواد دیگر تقریباً به طور کامل جذب میشوند.
حلقه هنله، لوله دیستال و مجاری جمع کننده الکترولیت ها و آب را جذب می کنند.
آلدوسترون بازجذب Na+ و دفع K+ و H+ را در لولههای کلیوی تحریک میکند. در نفرون دیستال، در لوله دیستال و مجاری جمع کننده قشر مغز.
وازوپرسین باعث جذب مجدد آب می شود از لوله های پیچیده دیستال و مجاری جمع آوری.
با کمک انتقال غیرفعال، بازجذب آب، کلر و اوره انجام می شود.
انتقال فعال عبارت است از انتقال مواد در برابر شیب الکتروشیمیایی و غلظت. علاوه بر این، بین حمل و نقل فعال اولیه و ثانویه تمایز قائل شد. حمل و نقل فعال اولیه با صرف انرژی سلول اتفاق می افتد. به عنوان مثال انتقال یون های Na+ با استفاده از آنزیم Na+/K+-ATPase است که از انرژی ATP استفاده می کند. در انتقال فعال ثانویه، انتقال یک ماده به دلیل انرژی انتقال ماده دیگر انجام می شود. گلوکز و اسیدهای آمینه توسط مکانیسم انتقال فعال ثانویه دوباره جذب می شوند.
مقدار حداکثر انتقال لوله ای با مفهوم قدیمی "آستانه دفع کلیوی" مطابقت دارد. برای گلوکز این مقدار 10 میلی مول در لیتر است.
موادی که بازجذب آنها به غلظت آنها در پلاسمای خون بستگی ندارد، غیر آستانه نامیده می شوند. اینها شامل موادی هستند که یا اصلاً بازجذب نمی شوند (اینولین، مانیتول) و یا به نسبت تجمع آنها در خون (سولفات ها) ضعیف جذب می شوند و از طریق ادرار دفع می شوند.
به طور معمول، مقدار کمی پروتئین وارد فیلتر شده و دوباره جذب می شود. فرآیند بازجذب پروتئین با استفاده از پینوسیتوز انجام می شود. پروتئین با ورود به سلول توسط آنزیم های لیزوزوم هیدرولیز شده و به اسیدهای آمینه تبدیل می شود. همه پروتئین ها تحت هیدرولیز قرار نمی گیرند، برخی از آنها بدون تغییر وارد خون می شوند. این فرآیند فعال است و نیاز به انرژی دارد. ظاهر شدن پروتئین در ادرار پروتئینوری نامیده می شود. پروتئینوری همچنین می تواند تحت شرایط فیزیولوژیکی، به عنوان مثال، پس از کار سنگین عضلانی رخ دهد. اساساً، پروتئینوری در پاتولوژی با نفریت، نفروپاتی و میلوما رخ می دهد.
اوره نقش مهمی در مکانیسم های غلظت ادرار دارد و آزادانه در گلومرول ها فیلتر می شود. در لوله پروگزیمال، بخشی از اوره به دلیل گرادیان غلظتی که به دلیل غلظت ادرار ایجاد می شود، به طور غیر فعال دوباره جذب می شود. بقیه اوره به مجاری جمع کننده می رسد. در مجاری جمع آوری، تحت تأثیر ADH، آب دوباره جذب می شود و غلظت اوره افزایش می یابد. ADH نفوذپذیری دیواره را برای اوره افزایش می دهد و به داخل بصل النخاع کلیه می رود و تقریباً 50٪ فشار اسمزی را در اینجا ایجاد می کند. از بینابینی، در امتداد گرادیان غلظت، اوره به حلقه هنله منتشر می شود و دوباره وارد لوله های دیستال و مجاری جمع آوری می شود. بنابراین، گردش اوره داخل کلیوی رخ می دهد. در مورد دیورز آب، جذب آب در نفرون دیستال متوقف می شود و اوره بیشتری دفع می شود. بنابراین دفع آن به دیورز بستگی دارد.
بازجذب اسیدها و بازهای ضعیف به یونیزه یا غیریونیزه بودن آنها بستگی دارد. بازها و اسیدهای ضعیف در حالت یونیزه دوباره جذب نمی شوند و از طریق ادرار دفع می شوند. درجه یونیزاسیون بازها در محیط اسیدی افزایش مییابد، بنابراین با سرعت بیشتری در ادرار اسیدی دفع میشوند؛ برعکس اسیدهای ضعیف در ادرار قلیایی سریعتر دفع میشوند. این مهم است زیرا بسیاری از داروها بازهای ضعیف یا اسیدهای ضعیف هستند. بنابراین در صورت مسمومیت با اسید استیل سالیسیلیک یا فنوباربیتال (اسیدهای ضعیف) باید محلول های قلیایی (NaHCO3) تجویز شود تا این اسیدها به حالت یونیزه تبدیل شوند و در نتیجه دفع سریع آنها از بدن تسهیل شود. برای دفع سریع بازهای ضعیف لازم است محصولات اسیدی وارد خون شود تا ادرار اسیدی شود.
به دلیل انتقال مواد فعال اسمزی: گلوکز، اسیدهای آمینه، پروتئین ها، یون های سدیم، پتاسیم، کلسیم، کلر، آب در تمام قسمت های نفرون به طور غیر فعال بازجذب می شود. با کاهش بازجذب مواد فعال اسمزی، جذب مجدد آب نیز کاهش می یابد. وجود گلوکز در ادرار نهایی منجر به افزایش دیورز (پلی یوری) می شود.
یون اصلی تامین کننده جذب غیرفعال آب، سدیم است. همانطور که در بالا ذکر شد، سدیم برای انتقال گلوکز و اسیدهای آمینه نیز ضروری است. علاوه بر این، نقش مهمی در ایجاد یک محیط فعال اسمزی در بینابینی مدولای کلیه ایفا می کند که به دلیل آن ادرار غلیظ می شود.
ورود سدیم از ادرار اولیه از طریق غشای آپیکال به سلول اپیتلیال لوله ای به طور غیرفعال در طول گرادیان های الکتروشیمیایی و غلظت اتفاق می افتد. سدیم از طریق غشاهای قاعده جانبی به طور فعال با استفاده از Na+/K+-ATPase از سلول خارج میشود. از آنجایی که انرژی متابولیسم سلولی صرف انتقال سدیم می شود، انتقال آن در درجه اول فعال است. انتقال سدیم به داخل سلول می تواند از طریق مکانیسم های مختلفی انجام شود. یکی از آنها مبادله Na+ با H+ (انتقال ضد جریان یا ضد بندر) است. در این حالت یون سدیم به داخل سلول و یون هیدروژن به خارج منتقل می شود. راه دیگر انتقال سدیم به داخل سلول با مشارکت آمینو اسیدها و گلوکز انجام می شود. این به اصطلاح cotransport یا simport است. بازجذب نسبی سدیم با ترشح پتاسیم همراه است.
گلیکوزیدهای قلبی (استروفانتین K، oubain) می توانند آنزیم Na+/K+-ATPase را مهار کنند که انتقال سدیم از سلول به خون و انتقال پتاسیم از خون به سلول را تضمین می کند.
کار سیستم ضربی به اصطلاح چرخشی- ضد جریان در مکانیسم های بازجذب آب و یون های سدیم و همچنین غلظت ادرار اهمیت زیادی دارد. پس از عبور از بخش پروگزیمال توبول، فیلتر ایزوتونیک با حجم کاهش یافته وارد حلقه هنله می شود. در این منطقه، بازجذب شدید سدیم با جذب مجدد آب همراه نیست، زیرا دیوارههای این بخش حتی تحت تأثیر ADH نسبت به آب نفوذپذیری ضعیفی دارند. در این راستا رقت ادرار در لومن نفرون و غلظت سدیم در بینابینی رخ می دهد. ادرار رقیق شده در لوله دیستال مایع اضافی را از دست می دهد و به پلاسما ایزوتونیک می شود. حجم کاهش یافته ادرار ایزوتونیک وارد سیستم جمع آوری می شود که در بصل النخاع جریان دارد که فشار اسمزی بالا در بینابینی آن به دلیل افزایش غلظت سدیم است. در مجاری جمع آوری، تحت تأثیر ADH، بازجذب آب مطابق با گرادیان غلظت ادامه می یابد. وازا رکتا که از بصل النخاع می گذرد به عنوان رگ های تبادل جریان مخالف عمل می کند و سدیم را در طول مسیر به پاپیلا می برد و قبل از بازگشت به قشر آزاد می کند. در اعماق بصل النخاع، محتوای سدیم بالایی به این ترتیب حفظ می شود و از جذب آب از سیستم جمع آوری و غلظت ادرار اطمینان می یابد.
در نتیجه جذب فعال بیشتر اجزای فعال اسمزی فیلتر، آب از طریق دیواره لوله ها دوباره جذب می شود و به دلیل انتشار حرکت می کند. منفعلانه
برای تعیین کمی سرنوشت مواد مختلف در نفرون، آنها را با آزاد شدن موادی مقایسه می کنند که به طور کامل در گلومرول ها فیلتر شده و متعاقباً به طور کامل در ادرار ثانویه دفع می شوند.
پاکسازی - ضریب تصفیه خون از مواد مختلف - یک مفهوم تا حدودی دلخواه است. از نظر کمی، با حجم پلاسمای خون مشخص می شود که در 1 دقیقه به طور کامل از یک ماده خاص توسط کلیه ها پاک می شود. پاکسازی توسط مواد به اصطلاح "غیر آستانه" تعیین می شود، یعنی. موادی که در طی یک عبور از کلیه ها به طور کامل دفع می شوند. کلیرانس اینولین حجم فیلتراسیون گلومرولی را تعیین می کند و تقریباً 120 میلی لیتر در دقیقه است. ترخیص کالا از گمرک اسید پاراآمینو هیپوریک برای ارزیابی جریان موثر پلاسمای کلیوی استفاده می شود و برابر با 600-650 میلی لیتر در دقیقه است.
در قسمت پروگزیمال نفرون، عمدتا متابولیت ها ترشح می شوند، در قسمت دیستال - یون های K، H و NH4.
اختلال در جذب مجدد پروتئین
گلوکز فیلتر شده تقریباً به طور کامل توسط سلول های لوله پروگزیمال بازجذب می شود و معمولاً در مقادیر کم از طریق ادرار دفع می شود. در طی بازجذب، گلوکز به ناقل متصل می شود (فسفریله می شود) و از طریق قسمت پایه سلول به داخل خون منتقل می شود. نقش یون های سدیم و بر این اساس پمپ Na ضروری است.
با هیپرگلیسمی همراه با دیابت، محتوای گلوکز در خون از سطح "آستانه کلیوی" 8 میلی مول در لیتر فراتر می رود، مقدار زیادی گلوکز از طریق گلومرول ها فیلتر می شود و سیستم های آنزیمی قادر به تضمین بازجذب کامل نیستند. گلوکوزوری ایجاد می شود. درست است، در موارد پیشرفته دیابت، گلوکوزوری ممکن است به دلیل آسیب کلیه (آنژیوپاتی) و کاهش فیلتراسیون رخ ندهد. نقص ارثی در سیستم های آنزیمی برای بازجذب گلوکز خود را به شکل دیابت شیرین کلیوی نشان می دهد، یک بیماری ارثی غالب که در آن گلوکزوری در پس زمینه سطوح طبیعی یا حتی پایین گلوکز خون ایجاد می شود. گلوکوزوری ممکن است نتیجه آسیب به اپیتلیوم لوله ای در طی ایسکمی کلیوی یا مسمومیت با داروهای حاوی جیوه یا لیزول باشد.
اختلال در جذب مجدد پروتئین
پروتئین در لوله های پروگزیمال توسط پینوسیتوز دوباره جذب می شود، تا حدی تجزیه می شود و سپس اجزای با وزن مولکولی کم وارد خون می شوند. مکانیسم های بازجذب پروتئین کمی مطالعه شده است. به طور خاص، اهمیت اساسی همودینامیک شناخته شده است. ظاهر پروتئین در ادرار را پروتئینوری می گویند (آلبومینوری شایع تر است). پروتئینوری کم موقت تا 1 گرم در لیتر می تواند در افراد سالم پس از کار فیزیکی طولانی مدت رخ دهد. پروتئینوری مداوم و بالاتر نشانه بیماری کلیوی است. با توجه به مکانیسم توسعه، به طور معمول به گلومرولی و لوله ای (گلومرولی و لوله ای) تقسیم می شود. با پروتئینوری گلومرولی، به دلیل افزایش نفوذپذیری غشای فیلتر، پروتئین به مقدار زیادی وارد حفره کپسول شوملیانسکی-بومن می شود که از قابلیت های جذب دستگاه لوله ای فراتر می رود. هنگامی که گلومرول ها آسیب می بینند، پروتئینوری متوسط ایجاد می شود. درست است، درجه پروتئینوری نشان دهنده شدت بیماری کلیوی نیست. پروتئینوری لوله ای با اختلال در جذب مجدد پروتئین به دلیل آسیب به اپیتلیوم لوله ای (آمیلوئیدوز، نکرونفروز سابلیمیت) یا اختلال در زهکشی لنفاوی همراه است. پروتئینوری عظیم در سندرم نفروتیک مشاهده می شود، زمانی که گلومرول ها و لوله ها آسیب دیده اند.
(ماژول direct4)
انتقال الکترولیت ها در نفرون
سلول های نفرون پروگزیمال بیشتر اجزای اولترافیلترات را بازجذب می کنند، اما نقش اصلی در این فرآیند به بازجذب سدیم با آنیون های همراه تعلق دارد. این بازجذب سدیم است که مهمترین عملکرد کلیه ها از نظر حجم و انرژی مصرفی است. بازجذب سدیم تا حد زیادی میزان کل ادرار دفع شده، مشارکت کلیه ها در تنظیم آب در بدن، غلظت اسمزی، ترکیب یونی خون و سایر شاخص های حیاتی را تعیین می کند. کلیه ها روزانه 1200 گرم سدیم را فیلتر می کنند و دفع آن از 10-5 گرم تجاوز نمی کند.بازجذب سدیم در قسمت های مختلف نفرون دارای ویژگی های بارز است. بنابراین، در بخش های پروگزیمال، که تا 75 درصد از سدیم فیلتر شده دوباره جذب می شود، بازجذب آن یک فرآیند فعال است، اما در برابر یک گرادیان کم رخ می دهد. بازجذب سدیم در بخشهای دیستال در برابر یک گرادیان غلظت بالا رخ میدهد که باعث آزاد شدن ادراری میشود که تقریباً هیچ یون سدیمی ندارد. ثابت شده است که بازجذب دیستال سدیم توسط آلدوسترون، هورمون قشر آدرنال، تنظیم می شود. مکانیسم های بیوشیمیایی انتقال فعال یون های سدیم تا حد زیادی نامشخص است. اهمیت خاصی به ATPase، SDH و آلفا کتوگلوتارات دهیدروژناز وابسته به Mg داده شده است.
اختلال در جذب مجدد یون های سدیم زمانی ایجاد می شود که تولید آلدوسترون به دلیل اثر مهارکننده ها (ادرارهای اسمزی) یا زمانی که حساسیت اپیتلیوم کلیه به آلدوسترون کاهش می یابد، ایجاد می شود. در چنین شرایطی، همراه با یون های سدیم، آب نیز با توسعه احتمالی کم آبی از بین می رود.
آزاد شدن یون های پتاسیم حدود 10 درصد از آنچه در گلومرول ها فیلتر می شود را تشکیل می دهد و یون های پتاسیم نه تنها دوباره جذب می شوند، بلکه تا حدی در لوله های انتهایی ترشح می شوند.
رقیق شدن اسمزی و غلظت ادرار
از 120 میلی لیتر فیلتر، 119 میلی لیتر در 1 دقیقه دوباره جذب می شود. تا 85 درصد از این مقدار در لوله های پروگزیمال به دنبال مواد فعال اسمزی (سدیم، گلوکز و غیره) بازجذب می شود که به عنوان "بازجذب اجباری" آب تعریف می شود. حدود 15٪ در مقاطع دیستال و مجاری جمع آوری مجدد جذب می شود - "بازجذب اختیاری".
سطح بازجذب اجباری ممکن است در صورت اختلال در جذب مجدد یون های سدیم یا گلوکز کاهش یابد (پلی یوری در دیابت شیرین، تجویز دیورتیک های اسمزی آلدوکتان). هنگامی که کمبود ADH یا عدم واکنش اپیتلیوم کلیه به دومی (اشکال دیابت بی مزه) وجود دارد، بازجذب اختیاری آب سرکوب می شود.
کلیه ها قادر به دفع ادرار 4 برابر هیپرتونیک و 6 برابر هیپوتونیک بیشتر از پلاسمای خون با نوسانات غلظت اسمزی نسبی 1002-1035 هستند. کاهش توانایی کلیه ها در تمرکز ادرار به صورت هیپوستنوری یا ایزواستنوری بیان می شود.
توقف کامل غلظت اسمزی وجود دارد. حداکثر غلظت اسمزی 270-330 میلی مول در لیتر (نسبی - 1010-1012) است.
دیورز روزانه در بزرگسالان سالم حدود 70 درصد از آب تجویز شده به صورت اگزوژن است. حداقل حجم ادرار مورد نیاز برای دفع مواد زائد 500 میلی لیتر است. پلی یوری - دفع ادرار روزانه بیش از 2000 میلی لیتر، الیگوری - 400-500 میلی لیتر، آنوری - تا 200 میلی لیتر.
در پاتوژنز اختلالات دفع ادرار، وضعیت تنظیم عصبی و هومورال مهم است. عوامل عاطفی می توانند دیورز را تغییر دهند و فعال شدن فرآیندهای تحریک در قشر مغز منجر به پلی اوری و مهار منجر به کولیگوری می شود. پلی یوری و الیگوری را می توان با رفلکس شرطی یا با پیشنهاد هیپنوتیزم به دست آورد.
اغلب در شرایط پاتولوژیک، آنوری درد رفلکس رخ می دهد. مهار رفلکس ادرار از مناطق مختلف رفلکسوژنیک امکان پذیر است. در پاتوژنز، رفلکس کلیوی از اهمیت ویژه ای برخوردار است، زمانی که آسیب یا آسیب دیگری به یکی از کلیه ها باعث آنوری موقتی در دیگری بدون آسیب شود. در همان زمان، به دلیل فعال شدن سیستم سمپاتوآدرنال، تون شریان های کلیوی افزایش می یابد که منجر به کاهش فیلتراسیون گلومرولی می شود.
تأثیرات هورمونی مهم است - تیروکسین فیلتراسیون گلومرولی را افزایش می دهد و مانند گلوکوکورتیکوئیدها دیورز را افزایش می دهد.
بازجذب در کلیه ها جذب معکوس موادی با منشاء مختلف از ادرار توسط بدن است. چنین موادی می تواند پروتئین، گلوکز، آب، سدیم، اجزای آلی و همچنین غیر آلی باشد. فرآیند جذب مجدد مواد شیمیایی و سایر اجزاء شامل لوله های کلیوی و همچنین سلول های اپیتلیال می شود. اگر مواد شیمیایی محصولات تجزیه شده باشند و به مقدار زیاد در بدن باشند، توسط سلول های اپیتلیال فیلتر می شوند. فرآیند جذب در لوله های پروگزیمال فعال می شود.
روش های مختلفی برای جذب مواد مغذی توسط بدن وجود دارد:
- فعال - بازجذب گلوکز، پتاسیم، یون های سدیم، منیزیم، اسیدهای آمینه. فرآیند انتقال در برابر غلظت، گرادیان الکتروشیمیایی انجام می شود.
- غیرفعال - بازجذب آب، بی کربنات، اوره. انتقال در طول یک گرادیان الکتروشیمیایی، اسمزی و غلظت انجام می شود.
- انتقال توسط پینوسیتوز - بازجذب پروتئین.
میزان فیلتراسیون و همچنین میزان انتقال عناصر شیمیایی و مواد مغذی به طور مستقیم به کیفیت تغذیه، ماهیت غذاهای مصرفی، سبک زندگی فعال و وجود بیماری های مزمن بستگی دارد.
انواع
دریافت مواد مغذی از طریق کانال های مختلف انجام می شود. از این نظر بازجذب به 2 نوع تقسیم می شود.
پروگزیمال
در طی فرآیند بازجذب پروگزیمال، پروتئین ها، اسیدهای آمینه، اجزای غنی شده و دکستروز از ادرار اولیه منتقل می شوند. در این صورت جذب کامل مواد مشاهده می شود. فیلتراسیون تنها 1/3 از حجم کل اجزای غذایی را تشکیل می دهد.
- بازجذب آب یک روش غیرفعال است که سرعت و کیفیت آن به وجود هیدروکلراید و قلیایی در محصولات فیلتراسیون بستگی دارد.
- انتقال بی کربنات با استفاده از روش های فعال و غیرفعال انجام می شود. سرعت آن به ناحیه اندام داخلی که ادرار از طریق آن توزیع می شود بستگی دارد. عبور ادرار از لوله ها پویا است. جذب اجزای غذایی از طریق غشاء تدریجی است. با انتقال غیرفعال، حجم ادرار کاهش می یابد و غلظت بی کربنات افزایش می یابد.
- فرآیند جذب مجدد دکستروز و همچنین اسیدهای آمینه با مشارکت مستقیم سلول های اپیتلیال واقع در مرز برس غشای آپیکال اتفاق می افتد. در طی این فرآیند، تشکیل همزمان هیدروکلراید و کاهش غلظت بی کربنات مشاهده می شود.
- هنگامی که گلوکز آزاد می شود، به سلول های انتقال دهنده متصل می شود. اگر غلظت گلوکز افزایش یابد، سلول های انتقال دهنده تحت فشار قرار می گیرند، در نتیجه این جزء به سیستم گردش خون منتقل نمی شود.

در طول عملکرد پروگزیمال، حداکثر جذب پروتئین و همچنین پپتید رخ می دهد.
دیستال
بر ترکیب نهایی ادرار و همچنین غلظت اجزای آلی تأثیر می گذارد. در این مرحله حداکثر جذب قلیایی و انتقال غیرفعال یون های کلسیم، فسفات، پتاسیم و کلرید رخ می دهد.
مشکلات احتمالی
اگر فیلتراسیون ناکافی مشاهده شود یا اختلال عملکرد اندام های فیلتر کننده خود را نشان دهد، این روند می تواند منجر به ظهور آسیب شناسی های مختلف و اختلالات فیزیولوژیکی شود:
- اختلالات بازجذب لوله ای افزایش یا کاهش جذب یون ها، آب یا مواد آلی از مجرای لوله ها. علل اختلال عملکرد ناشی از کاهش فعالیت اجزای حملونقل، کمبود ناقلها و ماکرو ارژها و آسیب به اپیتلیوم است.
- اختلال در فرآیند ترشح سلول های اپیتلیال. آسیب به لوله های انتهایی، آسیب به بافت ها و سلول های مدولا یا قشر کلیه. وجود اختلال عملکرد یک تحریک کننده برای ایجاد سندرم های کلیوی و خارج کلیوی است.
- سندرم های کلیوی - در نتیجه دیورز، اختلال در ریتم ادرار، تغییر در رنگ و ویژگی ادرار رخ می دهد. سندرم های کلیوی منجر به ایجاد نارسایی کلیه، توبولوپاتی، نفریت می شود.
- پلی یوری - دیورز، کاهش وزن مخصوص ادرار.
- الیگوری - کاهش حجم ادرار روزانه، افزایش وزن مخصوص مایع.
- عدم تعادل هورمونی - تولید فعال هورمون آلدوسترون باعث افزایش جذب سدیم و در نتیجه تجمع مایع در بدن می شود که منجر به ادم و کاهش در دسترس بودن پتاسیم می شود.
- آسیب شناسی ساختار سلول های اپیتلیال - این فرآیند علت اصلی اختلال در کنترل غلظت ادرار است.
علت دقیق وضعیت پاتولوژیک را می توان با استفاده از آزمایش ادرار تعیین کرد.

داستان هایی از خوانندگان ما
"من توانستم کلیه هایم را با کمک یک درمان ساده که از مقاله ای توسط یک متخصص اورولوژیست با 24 سال تجربه، پوشکار دی.یو..." در مورد آن فهمیدم، درمان کنم.
ارزیابی آزمایشگاهی
برای تعیین چگونگی ادامه بازجذب پروگزیمال، لازم است غلظت گلوکز در بدن، یعنی بالاترین مقدار آن، مشخص شود.
- برای تعیین بازجذب گلوکز، محلول قندی به صورت داخل وریدی به بیمار تزریق می شود که درصد گلوکز خون را به میزان قابل توجهی افزایش می دهد.
- آزمایش ادرار در حال بررسی است. اگر سطح ترکیب 9.5 - 10 mmol / L باشد، این طبیعی است.
آزمایشات دیگری برای تعیین روند بازجذب دیستال انجام می شود:
- بیمار نباید برای مدت معینی هیچ مایعی بنوشد.
- آزمایش ادرار گرفته می شود و وضعیت مایع و پلاسمای آن بررسی می شود.
- پس از مدت معینی به بیمار وازوپرسین تزریق می شود.
- پس از این، شما مجاز به نوشیدن آب هستید.
پس از مطالعه نتایج واکنش بدن، می توان دیابت بی مزه یا دیابت نفروژنیک را تشخیص داد.
عملکرد طبیعی سیستم ادراری به حذف به موقع و منظم مواد سمی و مواد زائد از بدن کمک می کند. هنگامی که اولین علائم اختلال عملکرد کلیه ظاهر می شود، باید بلافاصله با یک متخصص مشورت کنید. درمان نابهنگام یا عدم وجود کامل آن می تواند منجر به عوارض جدی و ایجاد فرآیندهای پاتولوژیک مزمن شود.
از مبارزه با بیماری کلیوی خسته شده اید؟

تورم صورت و پاها، درد در ناحیه کمر، ضعف و خستگی مداوم، ادرار دردناک؟ اگر این علائم را دارید، 95 درصد احتمال ابتلا به بیماری کلیوی وجود دارد.
اگر به سلامتی خود اهمیت نمی دهید، سپس نظر اورولوژیست با 24 سال سابقه را بخوانید. او در مقاله خود در مورد کپسول RENON DUO.
این یک داروی آلمانی سریع الاثر برای ترمیم کلیه است که سال هاست در سراسر جهان استفاده می شود. منحصر به فرد بودن دارو در موارد زیر است:
- علت درد را از بین می برد و کلیه ها را به حالت اولیه خود می رساند.
- کپسول های آلمانیدرد را از قبل در اولین دوره استفاده از بین ببرید و به درمان کامل بیماری کمک کنید.
- هیچ عارضه جانبی و واکنش های آلرژیک وجود ندارد.
6132 0
در CF بیش از 100 میلی گرم گلوکز در هر دقیقه وارد لومن نفرون می شود، اما به طور کامل توسط سلول های لوله پروگزیمال جذب می شود، بنابراین معمولاً گلوکز در ادرار تشخیص داده نمی شود و دفع روزانه آن از 130 میلی گرم بیشتر نمی شود. . بازجذب گلوکز در خون بر خلاف گرادیان غلظت بالا اتفاق می افتد، زیرا در نهایت هیچ گلوکزی در مایع لوله ای باقی نمی ماند.
فرآیند انتقال گلوکز به دسته فعال ثانویه تعلق دارد. این به دلیل این واقعیت است که انتقال گلوکز از مجرای لوله از طریق غشای مرزی برس با استفاده از یک انتقال دهنده انجام می شود که نیاز به حضور یون سدیم دارد. در غشای مرزی برس، انتقال فعال گلوکز یا سدیم وجود ندارد که برای بازجذب گلوکز ضروری است. انرژی سلولی برای این فرآیند با عملکرد پمپ سدیم ایجاد میشود که سدیم را از سلول خارج میکند و در غشای پلاسمایی قسمتهای جانبی و پایه سلول، یعنی روبروی مایع بین سلولی و مویرگهای خون قرار میگیرد.
در نتیجه انتقال فعال سدیم از سلول در سیتوپلاسم آن، غلظت سدیم کاهش می یابد. این به عنوان یک پیش نیاز برای ورود غیرفعال و گرادیان سدیم به سلول از طریق غشای مرزی قلم مو عمل می کند. انتقال دهنده تنها زمانی می تواند گلوکز را از مایع لوله ای به داخل سلول منتقل کند که با گلوکز و سدیم ترکیب شود که به آن اجازه عبور از غشاء را می دهد و از داخل سلول، گلوکز و سدیم به سیتوپلاسم آزاد می شود.
بنابراین، پمپ سدیم غشاهای قاعده ای به عنوان منبع انرژی عمل می کند. این انتقال سدیم است که انرژی TF را مصرف می کند که برای انتقال همزمان گلوکز به داخل سلول استفاده می شود. بنابراین، انتقال فعال اولیه سدیم، انتقال فعال ثانویه همراه گلوکز را به داخل سلول تضمین می کند. این سیستم بازجذب گلوکز فقط در غشای مرزی برس، یعنی در قسمتی از غشای پلاسمایی سلول که رو به لومن توبول است، قرار دارد. چنین مکانیسم انتقال گلوکز در غشای پلاسمایی پایه و جانبی وجود ندارد. گلوکز وارد شده به سلول در صندوق انتقال تجمع می یابد، جایی که غلظت آن بیشتر از مایع خارج سلولی می شود. غشای سلولی در قسمت پایه دارای نفوذپذیری کم نسبت به گلوکز است. برای اطمینان از جذب مجدد قند، انتقال آن از سلول توسط حامل های خاصی تعیین می شود که گلوکز را در امتداد گرادیان غلظت و بدون صرف انرژی تنفس سلولی به داخل مایع خارج سلولی منتقل می کنند.
در کلینیک، توانایی کلیه برای بازجذب گلوکز به عنوان یکی از شاخص های مهم وضعیت عملکردی سلول های لوله پروگزیمال و تعداد توبول های موثر عمل می کند. ویژگی های بازجذب گلوکز ارتباط نزدیکی با مکانیسم های گلیکوزوری دارد. از داده های فوق در مورد ماهیت فرآیند بازجذب گلوکز، نتیجه می شود که حداکثر تعداد مولکول های گلوکز که از مایع لوله ای به خون بازجذب می شوند به تعداد ناقل گلوکز و سرعت گردش آنها در غشاء بستگی دارد. بدیهی است که تمام گلوکز فیلتر شده دوباره جذب می شود تا زمانی که تعداد حامل ها و سرعت حرکت آنها در غشاء انتقال همه مولکول های گلوکز وارد شده به لومن لوله را تضمین کند.
دفع گلوکز در ادرار تنها زمانی شروع می شود که غلظت آن در پلاسما به طور قابل توجهی افزایش یابد که مقدار گلوکز فیلتر شده از ظرفیت بازجذب لوله ها بیشتر شود (شکل 1). مقدار گلوکز بازجذب شده در حداکثر بار تمام ناقلین غشایی درگیر در انتقال آن، تحت شرایط تحقیقاتی استاندارد، به عنوان یک شاخص عملکردی مهم از فعالیت توبول پروگزیمال عمل می کند. حداکثر انتقال گلوکز (TmG) در مردان 79.7±375 و در زنان - 303±55.3 میلی گرم در دقیقه است که به ازای 1.73 متر مربع از سطح بدن محاسبه می شود.
برنج. 1. رابطه بین غلظت گلوکز در پلاسمای خون، فیلتراسیون، بازجذب و دفع آن [Valint R., 1969]. در محور y در سمت چپ مقدار گلوکز فیلتر شده، بازجذب و استخراج شده، در سمت راست تصفیه گلوکز است. محور آبسیسا غلظت گلوکز در پلاسمای خون است.
مطالعات با استفاده از انفوزیون گلوکز و اندازه گیری TmG در کلینیک بینشی را در مورد تعادل بین CP و بازجذب در لوله پروگزیمال هر نفرون فراهم می کند. هنگامی که محلول گلوکز هیپرتونیک به خون تزریق می شود، هیپرگلیسمی باعث گلوکوزوری نمی شود تا زمانی که محدودیت توانایی آن برای بازجذب گلوکز در هیچ یک از لوله ها نرسد. اگر در همه نفرون ها بین حجم مایع فیلتر شده (و در نتیجه گلوکز) و توانایی بازجذب آن مطابقت وجود داشته باشد، TmG به طور همزمان در همه نفرون ها و با افزایش بیشتر غلظت گلوکز در خون، گلوکوزوری حاصل می شود. رخ می دهد.
اگر فیلتراسیون در دو نفرون یکسان باشد، اما وضعیت لولهها و توانایی بازجذب گلوکز متفاوت باشد، TmG به طور همزمان حاصل نمیشود. هر چه تفاوت بین نفرون های فردی بیشتر باشد، جمعیت نفرون ناهمگن تر، مطابقت کمتری بین سطح گلوکز CP و بازجذب آن، اختلاف بین نفرون ها در زمان شروع TmG با افزایش تدریجی غلظت گلوکز پلاسما بیشتر می شود. در برخی نفرون ها، TmG با غلظت گلوکز پلاسما 11.1 میلی مول در لیتر، در برخی دیگر - 22.2 میلی مول در لیتر به دست می آید. این پدیده را شکافتن منحنی تیتراسیون نفرون با گلوکز می نامند. این بستگی به ناهمگنی مورفولوژیکی و عملکردی جمعیت نفرون در کلیه دارد.
TmG با آکرومگالی، پس از تجویز تیروکسین افزایش می یابد و کاهش آن مشخصه بیماری آدیسون، حساس شدن سرم و افزایش غلظت 1-لیزین و 1-آلانین در فیلتر است. در طول دوره بیماری، رابطه بین حجم CP و بازجذب لوله ای گلوکز ممکن است تغییر کند. در بیماران مبتلا به دیابت، گلیکوزوری ممکن است در پویایی بیماری کاهش یابد، علیرغم سطح بالای دائمی گلوکز در پلاسما، که ناشی از رسوب کمپلکس های پروتئین-موکوپلی ساکارید در مویرگ های گلومرولی با تشکیل گلومرولواسکلروز مویرگ در افراد مسن است. با دیابت طولانی مدت این باعث کاهش CF در نفرونها میشود، بار گلوکز روی لولهها را کاهش میدهد و آنها زمان دارند تا گلوکز فیلتر شده را دوباره جذب کنند که منجر به کاهش گلوکزوری میشود.
نفرولوژی بالینی
ویرایش شده توسط بخور تاریوا
حذف محصولات متابولیک از بدن از طریق تشکیل ادرار انجام می شود که بر اساس بازجذب ترکیبات فیلتر شده قبلی است. از طریق بازجذب است که هموستاز خون حفظ می شود و ادرار نهایی با محصولات تجزیه مواد پروتئینی، یون ها، سموم و اجزای دارو تشکیل می شود.
بازجذب فرآیند مهمی در کلیه ها برای بازجذب ذرات خون و تشکیل ادرار نهایی با مواد غیر ضروری و اضافی است که سپس از بدن انسان دفع می شود.بازجذب چیست؟
برای درک بهتر فرآیند، لازم است مکانیسم عملکرد ساختارهای کلیوی و. در واحد ساختاری و عملکردی اندام، نفرون، سه فرآیند به طور مداوم رخ می دهد که ثبات یونی خون را حفظ می کند و باعث حذف محصولات متابولیک از بدن انسان می شود. در طی فیلتراسیون، ادرار اولیه تشکیل می شود که از پلاسمای خون به کپسول بومن می رود. در مرحله بعد، فرآیند بازجذب خود رخ می دهد - جذب مجدد آب، مولکول های پروتئین، گلوکز و برخی ترکیبات آلی و معدنی در لوله های کلیه به داخل عروق خونی، همراه با ترشح. یعنی مرحله دوم تشکیل ادرار به دنبال دارد - انتقال مواد لازم برای حفظ هموستاز از ادرار اولیه به لنف و پلاسما.
انواع بازجذب در کلیه ها
در نفرون، سلول های هر ناحیه به دلیل ساختار متفاوت لوله های کلیوی، وظایف متفاوتی را انجام می دهند. بر اساس ویژگی های آناتومیکی سیستم فیلتراسیون، دو نوع جذب معکوس متمایز می شود که در انواع و مقادیر مواد منتقل شده و همچنین در مکانیسم های تنظیم فرآیندها که توسط فشار اسمزی، محتوا تعیین می شود، تفاوت دارند. وجود یون های خاص در ادرار و هورمون های ضد ادرار.
مکش پروگزیمال
در اپیتلیوم لوله ای، بازجذب شدید آب با یک روش غیرفعال تحت تأثیر محتوای قلیایی و هیدروکلراید رخ می دهد و در نتیجه حجم عناصر اولیه ادرار را 1/3 کاهش می دهد. عبور مواد از دیواره های لوله ای بسیار نفوذپذیر انجام می شود. در طی بازجذب پروگزیمال، یون های سدیم، کلر، پتاسیم، بی کربنات ها، پروتئین ها با اسیدهای آمینه، فرآورده های اوره، دکستروز و ویتامین ها منتقل می شوند. بر اساس درجه حمل و نقل لوله ای، طبقه بندی اجزای ادرار متمایز می شود:
- آستانه. بازجذب گلوکز، پروتئین ها، اسیدهای آمینه نیاز به حضور مولکول های ناقل کلیوی ویژه ای دارد که با آن ها امکان عبور مجموعه تشکیل شده از غشای سلول های اپیتلیال لوله ای وجود دارد. اگر محتوای ماده در ادرار تشکیل شده پس از فیلتراسیون بیشتر از تعداد مولکول های لازم باشد، آستانه دفع کلیوی فراتر رفته و حمل و نقل بیشتر غیرممکن می شود.
- ترکیبات غیر آستانه ای در حجم بسیار کمتری (اوره) بازجذب می شوند یا به طور کامل جذب نمی شوند، بنابراین حداکثر آستانه خود را ندارند.
بازجذب دیستال
حجم مواد جذب شده به میزان قابل توجهی کاهش می یابد، اما این فرآیند است که ترکیب و غلظت ادرار نهایی را تعیین می کند.
بازجذب سدیم، کلسیم، پتاسیم و فسفات ها به طور فعال رخ می دهد، در حالی که کلر با انتقال غیرفعال مشخص می شود. نفوذپذیری غشاهای لوله های انتهایی نفرون توسط وازوپرسین تنظیم می شود که مستقیماً بر قابلیت هضم مقدار اوره و ورود آن به ماده بین سلولی تأثیر می گذارد.
مکانیسم فرآیند چیست و به چه چیزی بستگی دارد؟
 مکانیسم بازجذب در کلیه ها به دلیل قوانین فیزیک، شیمی و انرژی بدن اتفاق می افتد.
مکانیسم بازجذب در کلیه ها به دلیل قوانین فیزیک، شیمی و انرژی بدن اتفاق می افتد. سرعت و کیفیت بازجذب تحت تأثیر محتوای پروتئین های پلاسما، گلوکز، برخی یون ها و سایر ترکیبات، کیفیت تغذیه، شیوه زندگی، وضعیت سیستم دفع و وجود بیماری های خاص است. روش های مختلفی برای انتقال مواد از طریق دیواره لوله های کلیوی وجود دارد که بر اساس آنها انواع انتقال زیر مشخص می شود:
| چشم انداز | مواد منتقل شده | فرآیندها در هسته |
|---|---|---|
| فعال | گلوکز، پتاسیم، منیزیم | مواد از ناحیه غلظت پایینتر خود به منطقه با غلظت بالا بازجذب میشوند و انرژی بدن صرف میشود. |
| منفعل | آب، اوره، بی کربنات | مواد از ناحیه ای با غلظت کم به ناحیه با غلظت زیاد حرکت می کنند |
| پینوسیتوز | سنجاب ها | این ماده با گیرنده ها تعامل می کند و توسط غشای اپیتلیال در لوله های کلیوی جذب می شود. |
با چه تخلفاتی می توانید مواجه شوید؟
بسته به علت و مکانیسم فرآیند پاتولوژیک، می توان گروه های اصلی زیر را از علل اختلالات بازجذب تشخیص داد:
- نارسایی کلیه، فرآیندهای التهابی و دیستروفی در اندام، آسیب شناسی مستقیماً در لوله ها.
- سندرم نفروتیک و نفریت همراه با اختلال در ادرار.
- آسیب شناسی سیستم غدد درون ریز و به ویژه اختلال در سنتز هورمون هایی که بر تبادل یون تأثیر می گذارد.
- تغییر در غلظت برخی از ترکیبات (گلوکز، هیدروژن) در ادرار.